初中科学浙教版九年级上册期中复习02:碱
试卷更新日期:2020-10-21 类型:复习试卷
一、碱的性质
-
1. ①酸奶:②肥皂水;③食盐水是生活中常见的三种物质。酸奶能使紫色石蕊试液变红,肥皂水显碱性,食盐水的pH=7。它们的pH由小到大排列,正确的是( )A、①②③ B、①③② C、②①③ D、③②①2. 在一定质量的NaOH溶液中逐滴加入蒸馏水,如图中能正确表示溶液pH变化的是(横坐 标表示加入蒸馏水的质量,纵坐标表示溶液的pH)( )A、
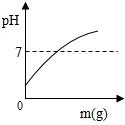 B、
B、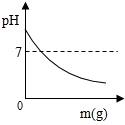 C、
C、 D、
D、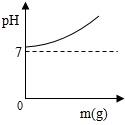 3. 下列是生活中常见物质的pH范围,显碱性的是( )A、葡萄汁(3.5~4.5) B、鸡蛋清(7.6~8.0) C、纯牛奶(6.3~6.6) D、苹果汁(2.9~3.3)4. 图示为某些物品对应的pH范围,其中显弱碱性的是( )
3. 下列是生活中常见物质的pH范围,显碱性的是( )A、葡萄汁(3.5~4.5) B、鸡蛋清(7.6~8.0) C、纯牛奶(6.3~6.6) D、苹果汁(2.9~3.3)4. 图示为某些物品对应的pH范围,其中显弱碱性的是( ) A、小苏打 B、杨梅 C、栗子 D、菠萝5. 小华将一张滤纸在某指示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图)放置一盛有某溶液的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂和烧杯中的溶液分别是( )
A、小苏打 B、杨梅 C、栗子 D、菠萝5. 小华将一张滤纸在某指示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图)放置一盛有某溶液的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂和烧杯中的溶液分别是( )
选项
A
B
C
D
滤纸上的指示剂
酚酞试液
酚酞试液
石蕊试液
石蕊试液
烧杯中的溶液
浓氨水
浓盐酸
浓氨水
浓盐酸
A、A B、B C、C D、D6. 下列有关氢氧化钠的说法,错误的是( )A、氢氧化钠俗称烧碱 B、氢氧化钠有强烈的腐蚀性 C、氢氧化钠水溶液能使紫色石蕊试液变红 D、氢氧化钠能去油污,厨房碱性清洁剂中含有氢氧化钠7. 物质性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体②有腐蚀性③易吸收水分而潮解④易溶于水,溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )A、①② B、③⑤ C、①②③ D、②③④8. 小柯同学取下列生活中的物质,测得其pH如下表所示:物质 肥皂水 雨水 糖水 柠檬汁 洗发剂 pH 10.2 5.2 7.0 2.5 12.2 (1)、酸性最强的物质是。(2)、弱酸性有益于头发的健康,所以我们洗发时应先用洗发剂,后用护发剂,由此我们可以知道护发剂的pH 7(填“=”或“<”或“>”)。9. 火力发电站附近农作物产量急剧下降。经科技人员检测发现:附近雨水pH约为5.0,土壤pH约为5.4。已知一些主要农作物适宜生长的土壤pH如下:农作物
玉米
小麦
马铃薯
pH
6~7
6.3~7.5
4.8~5.5
(1)、根据数据,该土壤最适合种植的农作物是。(2)、要改良酸性土壤应选择一种适合的碱,这种碱是(填化学式)。二、碱+某些非金属氧化物
-
10. 下面是某同学进行碱的性质实验时记录的实验现象,其中与事实不相符的是( )A、在NaOH溶液中加入稀盐酸,无明显变化 B、在NaOH溶液中通入CO2气体,有白色沉淀生成 C、在Ca(OH)2溶液中加入几滴石蕊试液,溶液呈蓝色 D、在Ca(OH)2溶液中加入Na2CO3溶液,有白色沉淀生成11. 为研究二氧化碳与氢氧化钠是否发生反应,王新兴同学设计的下列方案不可行的是( )A、
 B、
B、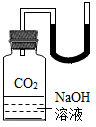 C、
C、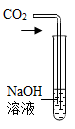 D、
D、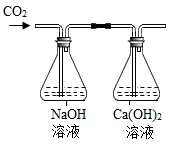 12. 下列四个实验中,不能体现碱的通性的是( )A、
12. 下列四个实验中,不能体现碱的通性的是( )A、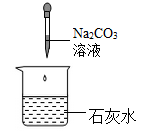 B、
B、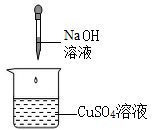 C、
C、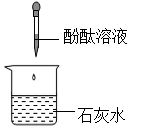 D、
D、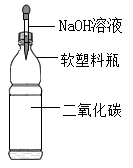 13. 如图装置可以制造非常有趣的“化学喷泉”,将胶头滴管中的NaOH溶液挤入烧瓶内,在导管的尖嘴处就会形成美丽的“喷泉”。
13. 如图装置可以制造非常有趣的“化学喷泉”,将胶头滴管中的NaOH溶液挤入烧瓶内,在导管的尖嘴处就会形成美丽的“喷泉”。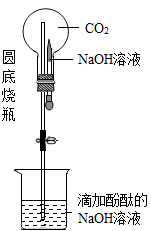 (1)、该现象的出现,原因是瓶内发生化学反应而使瓶内气压减小,请写出反应的化学方程式: 。(2)、若将烧瓶中的CO2换成下面的四种气体,仍可产生“喷泉”现象的瓶是 。A、SO2 B、H2 C、O2 D、HCl14. 化学活动小组的同学用右图所示装置进行实验(装置的气密性良好):先关闭止水夹,将足量氢氧化钠溶液滴入锥形瓶中,充分反应后,再打开止水夹.
(1)、该现象的出现,原因是瓶内发生化学反应而使瓶内气压减小,请写出反应的化学方程式: 。(2)、若将烧瓶中的CO2换成下面的四种气体,仍可产生“喷泉”现象的瓶是 。A、SO2 B、H2 C、O2 D、HCl14. 化学活动小组的同学用右图所示装置进行实验(装置的气密性良好):先关闭止水夹,将足量氢氧化钠溶液滴入锥形瓶中,充分反应后,再打开止水夹.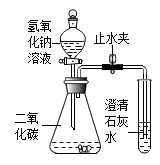 (1)、锥形瓶中能观察到的现象是 ;(2)、根据上述现象,能否得出“二氧化碳与氢氧化钠能反应”的结论?为什么?答:15. 某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,用图1总结了NaOH的四条化学性质。
(1)、锥形瓶中能观察到的现象是 ;(2)、根据上述现象,能否得出“二氧化碳与氢氧化钠能反应”的结论?为什么?答:15. 某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,用图1总结了NaOH的四条化学性质。 (1)、为了验证反应③能够发生,你选择的物质是( )A、Na2CO3 B、HCl C、FeCl3 D、Ba(NO3)2(2)、依据反应④,NaOH溶液可以吸收工业尾气中的SO2气体,其化学方程式为: 。
(1)、为了验证反应③能够发生,你选择的物质是( )A、Na2CO3 B、HCl C、FeCl3 D、Ba(NO3)2(2)、依据反应④,NaOH溶液可以吸收工业尾气中的SO2气体,其化学方程式为: 。三、碱+某些盐
-
16. 氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应。氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O。下列有关说法错误的是( )A、氢氧化铝属于碱 B、NaAlO2中铝元素的化合价为+3价 C、向氯化铝溶液中逐滴加入过量的氢氧化钠溶液,先产生白色沉淀,后沉淀不消失 D、向稀盐酸中加入氢氧化铝,发生中和反应17. 将某氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。根据实验事实绘制如图所示曲线。其中说法正确的是( )
 A、a至b段有蓝色沉淀生成 B、a至d段硫酸钠质量不断增大 C、c至d段,溶液pH不断减小 D、c点比a点所含的溶质种类少18. 现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示,则你认为X可能是下列物质中的( )
A、a至b段有蓝色沉淀生成 B、a至d段硫酸钠质量不断增大 C、c至d段,溶液pH不断减小 D、c点比a点所含的溶质种类少18. 现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示,则你认为X可能是下列物质中的( ) A、水 B、澄清石灰水 C、碳酸钙 D、纯碱溶液
A、水 B、澄清石灰水 C、碳酸钙 D、纯碱溶液四、碱+酸
-
19. 以下是日常生活中常用的清洗剂。
产品名称
洁厕灵
炉具清洁剂
有效成分
盐酸
氢氧化钠
若将洁厕灵滴入含有酚酞的炉具清洁剂中,pH值变化如图所示,则下列说法正确的是( )
 A、a点对应的溶液只含有盐酸 B、b点对应的溶液含有氢氧化钠 C、a、b点对应的溶液,酚酞均呈红色 D、a、b、c点对应的溶液均含有氯化钠20. 从微观视角看物质的变化是化学特有的思维方式。如图描述了NaOH溶液与盐酸反应的微观实质,C处应填入的物质化学式( )
A、a点对应的溶液只含有盐酸 B、b点对应的溶液含有氢氧化钠 C、a、b点对应的溶液,酚酞均呈红色 D、a、b、c点对应的溶液均含有氯化钠20. 从微观视角看物质的变化是化学特有的思维方式。如图描述了NaOH溶液与盐酸反应的微观实质,C处应填入的物质化学式( ) A、NaCl B、NaOH C、HCl D、H2O21. 用图甲装置进行实验,先将NaOH溶液,后将盐酸快速全部推入,用压强传感器测得一段时间内变化如图乙所示,下列推断正确的是( )
A、NaCl B、NaOH C、HCl D、H2O21. 用图甲装置进行实验,先将NaOH溶液,后将盐酸快速全部推入,用压强传感器测得一段时间内变化如图乙所示,下列推断正确的是( )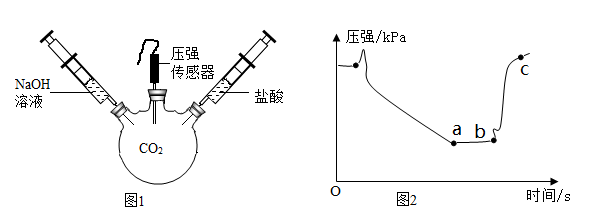 A、两种溶液先后推入目的是先后与CO2反应 B、气压变小的原因是CO2和NaOH溶液发生反应 C、ab段压强不变时因为一定没有发生化学反应 D、bc段压强变大是因为中和反应是放热反应22. 有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下。请分析并回答下列问题:
A、两种溶液先后推入目的是先后与CO2反应 B、气压变小的原因是CO2和NaOH溶液发生反应 C、ab段压强不变时因为一定没有发生化学反应 D、bc段压强变大是因为中和反应是放热反应22. 有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下。请分析并回答下列问题:加入NaOH溶液的体积/mL
0
2
4
6
8
10
12
14
烧杯中溶液的pH
1.1
1.2
1.4
1.6
2.0
7.0
11.0
12.2
(1)、当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应;(2)、当加入氢氧化钠溶液的体积为13mL时,溶液显色;(3)、当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?(填化学式表示)23. 向NaOH溶液中滴入HCl溶液至恰好完全反应。 (1)、如图表示该反应前后溶液中存在的主要离子,在横线上写出每种图形表示的离子(填离子符号)。(2)、发生反应的化学方程式是 。(3)、下列物质中只有一种能与KOH溶液发生上述类似反应,应是(填序号)
(1)、如图表示该反应前后溶液中存在的主要离子,在横线上写出每种图形表示的离子(填离子符号)。(2)、发生反应的化学方程式是 。(3)、下列物质中只有一种能与KOH溶液发生上述类似反应,应是(填序号)①HNO3②CusO4③CaCl2