广东省广州市白云区2019-2020学年九年级上学期化学期末考试试卷
试卷更新日期:2020-10-19 类型:期末考试
一、单选题
-
1. 垃圾分类人人有责。下列属于厨余垃圾的是( )A、易拉罐 B、旧报纸 C、塑料瓶 D、瓜果皮2. 中国诗词、成语和谚语中有些蕴含着化学知识。下列说法正确的是( )A、“好酒不怕巷子深”说明分子在不断地运动 B、“只要功夫深,铁杵磨成针”描述的是化学变化 C、“爆竹声中一岁除”描述的只有物理变化 D、“釜底抽薪”体现的灭火原理是隔绝氧气 ( 或空气 )3. 燃烧前常将汽油 ( 含C8H18等 ) 喷成雾状,可以( )A、减少O2消耗量 B、增大汽油与空气的接触面 C、降低汽油着火点 D、使C8H18等分子变得更小4. 物质的性质决定其用途。下列物质的用途与性质对应关系正确的是( )
物质
用途
性质
A
干冰
制造舞台烟雾效果
二氧化碳不燃烧,也不支持燃烧
B
氮气
食品防腐
空气中含量最多
C
生石灰
食品防潮剂
能与水反应
D
一氧化碳
冶炼金属单质
具有可燃性
A、A B、B C、C D、D5. 下列操作正确的是( )



A溶解
B过滤
C加热液体
D用胶皮管塞塞住试管
A、A B、B C、C D、D6. 提升“中国芯”的性能是我国信息产业的当务之急。“中国芯”的核心材料是高纯度的单质硅,工业上制取粗硅的化学方程式为:SiO2+2C Si+2CO↑,下列说法正确的是( )A、单质硅结构和金刚石类似,由分子构成 B、该反应的基本类型为分解反应 C、在此反应中硅元素的化合价降低 D、硅元素在地壳中的含量最多7. 科学家日前研制出一种名叫“干水”的物质 ( 如图 ) ,每个“干水”粒子是由小水滴、外层包上沙质硅膜组成的。这种糖粉状物质的最大特点是具有强力吸收二氧化碳的能力,具有极高的商业价值。下列有关“干水”的叙述正确的是( ) A、“干水”属于纯净物 B、“干水”的化学式为H2O C、“干水”可用于降低温室效应 D、“干水”吸收二氧化碳只发生物理变化8. 下列有关实验现象的描述,正确的是( )A、红磷在空气中燃烧,产生大量白烟 B、硫在氧气中燃烧,发出淡蓝色火焰 C、镁条在空气中燃烧,生成氧化镁 D、铁丝在氧气中燃烧,火星四射,生成红色固体9. 空气是一种宝贵的自然资源。下列对空气的相关叙述正确的是( )A、空气是由空气分子构成的 B、空气中的氧气可以作燃料 C、稀有气体化学性质很不活泼 D、化石燃料的使用不会污染空气10. 关于下列粒子结构示意图的说法中错误的是( )
A、“干水”属于纯净物 B、“干水”的化学式为H2O C、“干水”可用于降低温室效应 D、“干水”吸收二氧化碳只发生物理变化8. 下列有关实验现象的描述,正确的是( )A、红磷在空气中燃烧,产生大量白烟 B、硫在氧气中燃烧,发出淡蓝色火焰 C、镁条在空气中燃烧,生成氧化镁 D、铁丝在氧气中燃烧,火星四射,生成红色固体9. 空气是一种宝贵的自然资源。下列对空气的相关叙述正确的是( )A、空气是由空气分子构成的 B、空气中的氧气可以作燃料 C、稀有气体化学性质很不活泼 D、化石燃料的使用不会污染空气10. 关于下列粒子结构示意图的说法中错误的是( ) A、②和④属于同种元素 B、③是阳离子 C、①是阴离子 D、④用X代表,硝酸根与X构成物质的化学式为XNO311. 下列微观模拟图中的●和○分别表示氧原子和氢原子,则有关说法错误的是( )
A、②和④属于同种元素 B、③是阳离子 C、①是阴离子 D、④用X代表,硝酸根与X构成物质的化学式为XNO311. 下列微观模拟图中的●和○分别表示氧原子和氢原子,则有关说法错误的是( )



①
②
③
④
A、①表示混合物 B、②表示能保持H2O化学性质的最小微粒 C、③表示化合物 D、由③和④可知双氧水和水不是同一种物质12. 燃煤会影响环境。下列环境问题与燃煤没有直接关系的是( )A、酸雨 B、温室效应 C、臭氧层破坏 D、可吸入颗粒物增加13. 下列关于实验室制取二氧化碳的认识,正确的是( )A、常用炭在氧气中燃烧获得 B、不用浓盐酸的原因是反应过快不利于收集 C、不用稀硫酸的原因是成本高 D、不采用高温加热的反应是为了节能14. 电解水实验装置如图所示。下列说法正确的是( ) A、电解前后元素种类不变 B、实验说明水由H2和O2组成 C、电解水制取氢气得到广泛应用 D、a管收集的气体能使燃着的木条燃烧更旺15. 在实验室中,下列实验操作能达到实验目的的是( )
A、电解前后元素种类不变 B、实验说明水由H2和O2组成 C、电解水制取氢气得到广泛应用 D、a管收集的气体能使燃着的木条燃烧更旺15. 在实验室中,下列实验操作能达到实验目的的是( )选项
实验目的
实验操作
A
除去混在二氧化碳中的一氧化碳
点燃
B
鉴别软水和硬水
加入水,搅拌
C
除去混在木炭粉中的氧化铜
在空气中灼烧
D
鉴别空气、氮气、氧气
燃着的木条分别伸入集气瓶
A、A B、B C、C D、D16. “化学棋”游戏规则:①每粒棋子代表一种物质:②吃子:所选棋子能与棋盘 ( 如图 ) 中的某棋子发生反应,则棋盘中的该棋子被吃掉;③连吃:前一次反应的生成物能与另一棋子发生反应时,则该棋子也该吃掉・若一次就可连续吃掉棋盘上的所有棋子,应选择的棋子是 ( 反应条件可忽路 )( ) A、
A、 B、
B、 C、
C、 D、
D、 17. 硫代硫酸钠化学式是Na2S2O3 , 硫代硫酸钠中硫元素的化合价是( )A、0 B、+2 C、+4 D、+618. 乙酸化学式C2H4O2 , 是食醋的主要成分,在我国有杜康的儿子因酸酒时间过长而得到醋的说法。下列说法正确的是( )A、1个乙酸分子中含有2个碳原子、4个氢原子和1个氧分子 B、乙酸中碳、氢、氧三种元素的质量比为1:2:1 C、乙酸是氧化物 D、乙酸中碳元素的质量分数为19. 根据如图所示的实验现象分析,下列说法错误的是( )
17. 硫代硫酸钠化学式是Na2S2O3 , 硫代硫酸钠中硫元素的化合价是( )A、0 B、+2 C、+4 D、+618. 乙酸化学式C2H4O2 , 是食醋的主要成分,在我国有杜康的儿子因酸酒时间过长而得到醋的说法。下列说法正确的是( )A、1个乙酸分子中含有2个碳原子、4个氢原子和1个氧分子 B、乙酸中碳、氢、氧三种元素的质量比为1:2:1 C、乙酸是氧化物 D、乙酸中碳元素的质量分数为19. 根据如图所示的实验现象分析,下列说法错误的是( )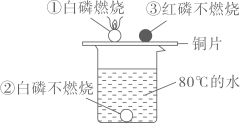 A、①②对比说明物质燃烧需要与空气接触 B、①中使温度达到白磷着火点是利用了铜的导热性 C、烧杯中的热水只起提高温度的作用 D、①③对比说明红磷着火点高于白磷20. 下图所示的实验能达到实验目的的是( )
A、①②对比说明物质燃烧需要与空气接触 B、①中使温度达到白磷着火点是利用了铜的导热性 C、烧杯中的热水只起提高温度的作用 D、①③对比说明红磷着火点高于白磷20. 下图所示的实验能达到实验目的的是( ) A、实验一:验证空气的密度大于CO2 B、实验二:验证空气中氧气含量 C、实验三:验满O2 D、实验四:验证反应前后质量相等
A、实验一:验证空气的密度大于CO2 B、实验二:验证空气中氧气含量 C、实验三:验满O2 D、实验四:验证反应前后质量相等二、填空题
-
21. 如图为价类图表示元素的化合价与物质类别关系。若它表示氮元素的部分关系图,B点标示+2价的氮的氧化物,则
 (1)、A点对应的物质类别是;(2)、D点表示物质的化学式为;(3)、査资料可知:元素处于最高价,只有氧化性;元素处于最低价,只有还原性,则C可能具有的性质是。常温下C与水反应能生成B和E(硝酸),反应的化学方程式是。22. 建立“宏观—微观—符号”之间的联系,是化学学习的重要方法。根据图示回答下列问题:(1)、二氧化碳和氢气在一定条件下转換为化工原料乙烯(C2H4),是我国科学研究的又一重大突破,其反应微观过程如下图所示,用化学方程式表示为 , 由下图得到启示。请用微观的观点解释化学变化的实质。
(1)、A点对应的物质类别是;(2)、D点表示物质的化学式为;(3)、査资料可知:元素处于最高价,只有氧化性;元素处于最低价,只有还原性,则C可能具有的性质是。常温下C与水反应能生成B和E(硝酸),反应的化学方程式是。22. 建立“宏观—微观—符号”之间的联系,是化学学习的重要方法。根据图示回答下列问题:(1)、二氧化碳和氢气在一定条件下转換为化工原料乙烯(C2H4),是我国科学研究的又一重大突破,其反应微观过程如下图所示,用化学方程式表示为 , 由下图得到启示。请用微观的观点解释化学变化的实质。 (2)、微观角度我国研制的一种新型催化剂可将CO2和H2转化为甲醇(CH3OH)和H2O。若用“○”表示氢原子,“
(2)、微观角度我国研制的一种新型催化剂可将CO2和H2转化为甲醇(CH3OH)和H2O。若用“○”表示氢原子,“ ”表示氧原子,“
”表示氧原子,“  ”表示碳原子,该反应的微观示意图(已经配平)如下:
”表示碳原子,该反应的微观示意图(已经配平)如下: 
画出X的微观示意图:。
(3)、结构决定性质。研究发现含有“过氧基”(—O—O—)的物质具有很强的氧化性,可以作为杀菌消毒剂。据此推测,下列物质中,可用作杀菌消毒剂的是(填数字序号) (4)、通过分析组成和结构,我们可以预测物质的某些性质。在你目前的知识储备范围内,关于NaHSO4的性质,你的推测是:(只写一条)。23. 2019年是元素周期表发现150周年,该表是学习化学的重要工具。硒元素有防癌抗癌作用。硒在周期表中的信息如图所示。
(4)、通过分析组成和结构,我们可以预测物质的某些性质。在你目前的知识储备范围内,关于NaHSO4的性质,你的推测是:(只写一条)。23. 2019年是元素周期表发现150周年,该表是学习化学的重要工具。硒元素有防癌抗癌作用。硒在周期表中的信息如图所示。 (1)、X的数值是。硒原子的中子数是。(2)、硒阴离子的符号表示为。(填名称)原子的化学性质与硒原子相似。(3)、已知:Se+2HClO+H2O=H2SeO3+2HCl,H2SeO3+2ROH=R2SeO3+2H2O(R的相对原子质量为Y)消耗79g硒需要ROH的质量是g。(用含有Y的数值表示)
(1)、X的数值是。硒原子的中子数是。(2)、硒阴离子的符号表示为。(填名称)原子的化学性质与硒原子相似。(3)、已知:Se+2HClO+H2O=H2SeO3+2HCl,H2SeO3+2ROH=R2SeO3+2H2O(R的相对原子质量为Y)消耗79g硒需要ROH的质量是g。(用含有Y的数值表示)三、科学探究题
-
24. 小明对金属钠产生了好奇
(查阅资料)Na性质活泼,常温下,与氧气反应,也可以与水反应产生遇火发出爆鸣声的气体,同时生成氢氧化钠。
(实验与分析)①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下ー小块,投入蒸馏水中,发现钠块立刻熔化成银白色小球,在水面上到处游动,冒出气泡;③往硫酸铜溶液中,投入一小块钠,出现蓝色沉淀,但没有红色物质析出。
(1)、根据推理,你认为金属钠的密度比煤油(填“小”或“大”或“无法判断”),保存在煤油中的原因是。(2)、从实验②中,你能得出钠的性质的哪些信息?(任写三条):;;。(3)、写出钠与水反应的化学方程式。25. 小明不小心把硫酸铜溶液滴加到盛有5%H2O2的溶液中,发现立即有大量的气泡产生。硫酸铜溶液中含有三种粒子(H2O、SO42-、Cu2+),小明设计了下列实验,探究硫酸铜溶液中的哪种粒子能使双氧水分解的速率加快。 (1)、小明认为最不可能的粒子是 , 理由是。(2)、要证明另外两种粒子能否加快双氧水分解的速率,还需要进行实验②和③;在实验②中加入稀硫酸后,无明显变化,证明不起催化作用:在实验③中加入硝酸铜或氯化铜溶液后,观察到大量的气泡,证明起催化作用的是。(3)、小明如果要确定硫酸铜是催化剂,还须通过实验确认它在化学反应前后。(4)、小明为研究双氧水溶液的浓度对反应速率的影响,做了以下实验:每次均用30mL30%的双氧水稀释成不同浓度的溶液(室温20℃,其他实验条件均相同),结果如表:
(1)、小明认为最不可能的粒子是 , 理由是。(2)、要证明另外两种粒子能否加快双氧水分解的速率,还需要进行实验②和③;在实验②中加入稀硫酸后,无明显变化,证明不起催化作用:在实验③中加入硝酸铜或氯化铜溶液后,观察到大量的气泡,证明起催化作用的是。(3)、小明如果要确定硫酸铜是催化剂,还须通过实验确认它在化学反应前后。(4)、小明为研究双氧水溶液的浓度对反应速率的影响,做了以下实验:每次均用30mL30%的双氧水稀释成不同浓度的溶液(室温20℃,其他实验条件均相同),结果如表:序号
1
2
3
4
5
6
7
8
H2O2溶液浓度
1%
3%
5%
10%
15%
20%
25%
30%
MnO2用量/g
0.2
0.2
0.2
0.2
0.2
0.2
0.2
0.2
收集到500mL气体需要的时间/s
660
220
205
80
25
9
4
3
反应后液体的温度/℃
24
34
39
56
65
67
69
70
①写出上述反应的化学方程式:。
②H2O2溶液浓度对反应速率的影响是。
③该反应是反应(填“吸热”或“放热”)
26. 实验探究(1)、定性检测(已知:无水CuSO4遇水变蓝色)
实验操作
实验现象
结论
连接装置,先① , 再装入试剂并按如图进行实验,通入O2 , 一段时间后,点燃J处酒精灯。
装置K中无水CuSO4变②色
塑料燃烧产物中有水
装置L中③。
塑料燃烧产物中有二氧化碳
④由上述实验可知,该塑料一定含有的元素是(填元素符号)。
(2)、定量测定为进一步确定组成,将1.4g该塑料在足量氧气中完全燃烧,共产生了4.4g二氧化碳和1.8g水,依据质量守恒定律,可判断消耗氧气的质量是g,该塑料是否含有除上述结论④之外的元素呢?请列出计算过程并给出结论。
四、流程题
-
27. 氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分为碳酸钡,化学性质与碳酸钙类似)制备氯化钡晶体工艺流程如下:
 (1)、毒重石要进行粉碎的目的是;气体X的化学式为。(2)、操作Y的名称是 , 滤液2中可循环利用的物质除水外还有。
(1)、毒重石要进行粉碎的目的是;气体X的化学式为。(2)、操作Y的名称是 , 滤液2中可循环利用的物质除水外还有。五、实验题
-
28. 根据下列实验装置改进,回答问题
 (1)、实验室有如图所示装置,连接装置时,需根据导管的高度调节处的高度,再确定处的高度。(填“甲”或“乙”)(2)、下图中一段时间后,瓶内气体的黄绿色消失,原因是。
(1)、实验室有如图所示装置,连接装置时,需根据导管的高度调节处的高度,再确定处的高度。(填“甲”或“乙”)(2)、下图中一段时间后,瓶内气体的黄绿色消失,原因是。 29. 气体的实验室制取是学生必备的基本实验技能,请根据下列装置回答问题:
29. 气体的实验室制取是学生必备的基本实验技能,请根据下列装置回答问题: (1)、写出图中标数字的仪器名称① , ②。(2)、实验室用加热高锰酸钾制取氧气的化学方程式为 , 若用D装置收集氧气,气体应从管口(填“a”或“b”)进入。(3)、图中的E装置可用来测量生成氧气的体积。进行操作时,在水量足够的前提下,集气瓶未装满水是否会影响实验结果(填“是”或“否”)。(4)、加热氯化铵和熟石灰的固体混合物可制取NH3 , 氨气极易溶于水。
(1)、写出图中标数字的仪器名称① , ②。(2)、实验室用加热高锰酸钾制取氧气的化学方程式为 , 若用D装置收集氧气,气体应从管口(填“a”或“b”)进入。(3)、图中的E装置可用来测量生成氧气的体积。进行操作时,在水量足够的前提下,集气瓶未装满水是否会影响实验结果(填“是”或“否”)。(4)、加热氯化铵和熟石灰的固体混合物可制取NH3 , 氨气极易溶于水。①制取氨气应选用的发生装置为(填字母序号)。氨气只能用法收集。
②振荡如图中的试管可观察到的现象是:。
 (5)、下列加热高酸钾制取氧气的部分操作示意图中,正确的是(填序号)。
(5)、下列加热高酸钾制取氧气的部分操作示意图中,正确的是(填序号)。
-