内蒙古鄂尔多斯市2020年中考化学试卷
试卷更新日期:2020-09-23 类型:中考真卷
一、单选题
-
1. 规范化学实验操作是实验成败的关键。下列实验操作正确的是( )A、量取液体
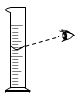 B、检查装置气密性
B、检查装置气密性 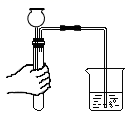 C、蒸发结晶
C、蒸发结晶 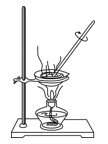 D、给液体加热
D、给液体加热 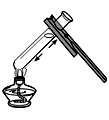 2. 物质变化是化学研究的重要内容。下列变化中与其他三种变化有本质区别的是( )A、活性炭净水 B、工业制氧气 C、干冰制冷 D、工业炼铁3. 归纳和总结是学习化学的有效方法。下列对各主题知识的有关归纳有错误的是( )
2. 物质变化是化学研究的重要内容。下列变化中与其他三种变化有本质区别的是( )A、活性炭净水 B、工业制氧气 C、干冰制冷 D、工业炼铁3. 归纳和总结是学习化学的有效方法。下列对各主题知识的有关归纳有错误的是( )选项
主题
归纳
A
化学与健康
①牛奶、鸡蛋为人体提供蛋白质
②人体缺碘易患贫血病
B
化学与环境
①垃圾分类回收,节约又环保
②城市道路洒水减少扬尘污染
C
化学与能源与资源
①“乙醇汽油”的推广可以缓解石油资源短缺
②氢气是极具开发前景的新能源
D
化学与材料
①“复兴号”高铁车轮用到的“高速钢”属于金属材料
②华为手机屏用到“聚酰亚胺塑料”属于有机合成材料
A、A B、B C、C D、D4. 化学用语是学习化学的基本工具。下列化学用语书写正确的是( )A、两个氮原子: B、两个乙酸分子: C、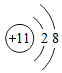 表示的微粒:
D、过氧化氢中氧元素的化合价:
5. 推理是一种重要的化学思维方法。以下推理合理的是( )A、铝比铁活泼,所以铝制品更易腐蚀 B、许多物质能在氧气中燃烧,所以氧气可以作燃料 C、水通电生成氢气和氧气,所以水由氢气和氧气组成 D、常温下碱溶液的 ,所以该温度下 的溶液一定显碱性6. 2020年世界海洋日的主题是:保护红树林,保护海洋生态。“红树”本是绿色的,当其树干、树枝断裂后,其中所含的单宁酸 就被氧化变红,故称“红树”。下列有关单宁酸的说法正确的是( )A、单宁酸中 三种元素的质量比为 B、由76个碳原子、52个氢原子和46个氧原子构成 C、化学性质稳定,不需要密封保存 D、是一种有机化合物7. 化学是一门以实验为基础的科学。下列实验设计能达到实验目的的是( )
表示的微粒:
D、过氧化氢中氧元素的化合价:
5. 推理是一种重要的化学思维方法。以下推理合理的是( )A、铝比铁活泼,所以铝制品更易腐蚀 B、许多物质能在氧气中燃烧,所以氧气可以作燃料 C、水通电生成氢气和氧气,所以水由氢气和氧气组成 D、常温下碱溶液的 ,所以该温度下 的溶液一定显碱性6. 2020年世界海洋日的主题是:保护红树林,保护海洋生态。“红树”本是绿色的,当其树干、树枝断裂后,其中所含的单宁酸 就被氧化变红,故称“红树”。下列有关单宁酸的说法正确的是( )A、单宁酸中 三种元素的质量比为 B、由76个碳原子、52个氢原子和46个氧原子构成 C、化学性质稳定,不需要密封保存 D、是一种有机化合物7. 化学是一门以实验为基础的科学。下列实验设计能达到实验目的的是( )选项
实验目的
实验设计
A
分离NaCl和KNO3的固体混合物
将混合物先加水制成饱和溶液,再冷却
B
除去CO2中的少量CO
将混合气体通过足量的灼热的氧化铜粉末
C
制备MgSO4
将Mg(OH)2和CuSO4溶液混合后过滤
D
检验Cl-
滴加AgNO3溶液,观察是否有沉淀生成。
A、A B、B C、C D、D8. 读图识图是学习化学的重要手段。下列四个图像中不能正确反映对应变化关系的是( )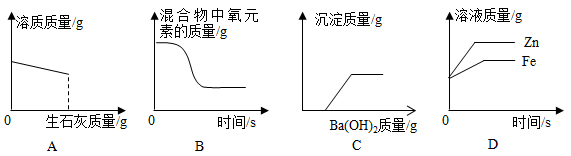 A、图A是向一定量的饱和石灰水中加入少量生石灰 B、图B是加热氯酸钾和二氧化锰的混合物制取氧气 C、图C是向一定量的稀盐酸和硫酸钠的混合溶液中加入 溶液 D、图D是将形状相同质量相等的铁和锌分别加入到足量的质量和浓度都相等的稀硫酸中
A、图A是向一定量的饱和石灰水中加入少量生石灰 B、图B是加热氯酸钾和二氧化锰的混合物制取氧气 C、图C是向一定量的稀盐酸和硫酸钠的混合溶液中加入 溶液 D、图D是将形状相同质量相等的铁和锌分别加入到足量的质量和浓度都相等的稀硫酸中二、填空题
-
9. 化学源于生活又服务于生活。(1)、“众志成城、全民抗疫”必须依靠科学。下列是小浩一家人日常的抗疫措施,其中有科学依据且利用乳化原理的是 (填序号)。
① 爷爷每天喝酒消毒② 奶奶靠吃保健品提高免疫力③ 爸爸将“84”消毒液稀释拖地④ 妈妈用汽油清洗衣服上的油污⑤ 姐姐用沐浴露洗澡⑥ 小浩用洗手液洗手
(2)、低碳生活从细节做起,你的一个低碳举措是 。(3)、安全是永恒的主题。消防员用高压水枪灭火,主要依据的灭火原理是 。(4)、沼气可以作燃料,在大棚中燃烧沼气还可以提高作物产量,沼气的主要成分燃烧的微观示意图如下:
下列说法正确的是 _______ (填字母序号)。
A、该反应过程中 与
与  的分子个数比为1:1
B、该反应属于氧化反应
C、点燃沼气前需要检验其纯度防止发生爆炸
D、生成的
的分子个数比为1:1
B、该反应属于氧化反应
C、点燃沼气前需要检验其纯度防止发生爆炸
D、生成的  可做气肥
10. 下表是元素周期表中第二、三周期的元素信息。结合表回答有关问题:
可做气肥
10. 下表是元素周期表中第二、三周期的元素信息。结合表回答有关问题: (1)、氩的相对原子质量为 。(2)、由第12号元素与第17号元素组成的化合物属于 (填“氧化物”或“酸”或“碱”或“盐”)。(3)、下列各组中的元素化学性质相似的是 (填序号)。
(1)、氩的相对原子质量为 。(2)、由第12号元素与第17号元素组成的化合物属于 (填“氧化物”或“酸”或“碱”或“盐”)。(3)、下列各组中的元素化学性质相似的是 (填序号)。① ② ③
11. 金属在生产、生活中应用广泛,金属的回收利用有利于保护环境、节约资源。(1)、用体温计测量体温时,水银柱会上升。用微观知识解释产生该现象的原因 。(2)、我国古代典籍中有“银针验毒”的记载。“银针验毒”的反应原理之一是: , 的化学式为 。(3)、某工厂欲从溶质是 和 的生产废液中回收 和 。实验员取样,向其中加入一定量的锌,充分反应后过滤,得到滤渣和滤液。①若所得滤液为蓝色,则滤液中一定含有金属离子 (填离子符号)。
②若向所得滤渣中加入一定量稀硫酸产生气泡,则滤渣中一定含有 。
12. 如图是甲、乙、丙三种固体的溶解度曲线图。据图回答下列问题: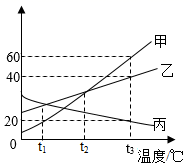 (1)、乙、丙两物质在 ℃时溶解度相等。(2)、将 t2℃时甲的饱和溶液变为不饱和溶液,在保证溶液质量不改变的前提下可采取的方法是 。(3)、t2℃时欲配制 的乙物质的溶液,需量取水 。(水的密度为 )(4)、t3℃时,将三种物质各 分别加入 水中,充分溶解后,只有一种物质形成不饱和溶液,则 的取值范围是 。
(1)、乙、丙两物质在 ℃时溶解度相等。(2)、将 t2℃时甲的饱和溶液变为不饱和溶液,在保证溶液质量不改变的前提下可采取的方法是 。(3)、t2℃时欲配制 的乙物质的溶液,需量取水 。(水的密度为 )(4)、t3℃时,将三种物质各 分别加入 水中,充分溶解后,只有一种物质形成不饱和溶液,则 的取值范围是 。三、推断题
-
13. 图中 是初中化学常见的物质。在通常情况下, 和 为气态, 通入无色酚酞溶液中,溶液变红;胃液中含适量的 ,可帮助消化; 与 发生中和反应。(图中“ ”表示两端的物质之间能发生化学反应,“ ”表示物质间存在转化关系,部分反应物和生成物已略去。)回答下列问题:
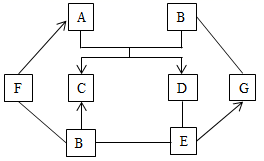 (1)、 的化学式为 。(2)、 反应的基本反应类型是 。(3)、 反应的化学方程式为 。(4)、图中属于化合反应的一个化学方程式为 。
(1)、 的化学式为 。(2)、 反应的基本反应类型是 。(3)、 反应的化学方程式为 。(4)、图中属于化合反应的一个化学方程式为 。四、实验题
-
14. 走进化学实验室会给你带来无限乐趣。现有如下装置,结合装置图回答问题:
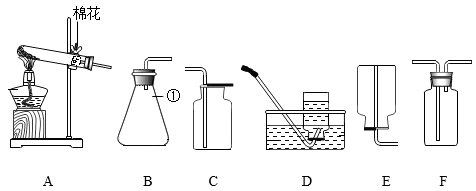 (1)、写出图中带标号①的仪器名称 。(2)、连接装置 和 ,可制取一种熟悉的气体,反应的化学方程式是 。要干燥制得的气体,可将气体通入 装置, 装置中应该装入的试剂名称是 。(3)、实验室制取气体发生装置的选择依据是 。选择装置 制取二氧化碳时,虽然操作简单,但无法控制反应速率。将该装置进行简单改进后就可达到控制反应速率的目的,改进措施是 。
(1)、写出图中带标号①的仪器名称 。(2)、连接装置 和 ,可制取一种熟悉的气体,反应的化学方程式是 。要干燥制得的气体,可将气体通入 装置, 装置中应该装入的试剂名称是 。(3)、实验室制取气体发生装置的选择依据是 。选择装置 制取二氧化碳时,虽然操作简单,但无法控制反应速率。将该装置进行简单改进后就可达到控制反应速率的目的,改进措施是 。五、科学探究题
-
15. 实验室有一瓶常用无色液体的标签模糊了(如图)。为确定该瓶溶液的溶质是什么,同学们进行了如下探究:
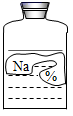
(提出问题)这瓶溶液的溶质是什么?
(作出猜想)猜想1: 猜想2: 猜想3: 猜想4:
(查阅资料) 溶液显碱性, 溶液不与 溶液反应。
(1)、(实验探究)实验步骤
实验现象
实验结论
小亮取2mL该无色溶液于试管中,滴加2滴无色酚酞溶液
溶液变红
猜想1、3成立
猜想2、4不成立
小丽取2mL该无色溶液于试管中,加入3mL稀盐酸
立即产生气泡
猜想不成立。
(2)、(交流讨论)同学们一致认为小亮的实验结论不正确,理由是 。
(3)、为了确定该无色溶液到底是什么,小强继续进行如下实验:①取 该无色溶液于试管中,滴加 溶液,边加边振荡,观察到产生白色沉淀。由此得出猜想 成立,反应的化学方程式为 。
②另取 该无色溶液于试管中,逐滴加入稀盐酸,一段时间后才观察到有气泡产生。
(4)、(拓展思考)小丽和小强都向无色溶液中加入稀盐酸,为什么现象不同?(延伸探究)同学们查阅资料发现:向 溶液中逐滴加入稀盐酸时,反应分两步进行:
; 。
故出现小强的实验现象。
(应用提升)现有两瓶失去标签的无色溶液,已知它们分别是碳酸钠溶液和稀盐酸中的一种,若不另加任何试剂要将二者鉴别开,你的鉴别方案是 (写出操作方法、现象和结论)。
六、计算题
-
16. 某兴趣小组取 和 的固体混合物 ,加入到盛有一定质量某浓度稀盐酸的烧杯中,恰好完全反应,气体全部逸出后,所得不饱和溶液的质量为 。
烧杯及烧杯内物质质量随反应时间变化如下表。
反应时间
0
t2
t3
t4
烧杯及烧杯内物质质量
64
62.9
61.8
61.8
计算:
(1)、生成 的质量为 。(2)、烧杯中原有稀盐酸的溶质质量分数是多少?
-
-
-