福建省龙岩市永定区2019-2020学年九年级上学期化学期中考试试卷
试卷更新日期:2020-09-01 类型:期中考试
一、单选题
-
1. 我们每天生活在不断变化的物质世界里,下列厨房里发生的变化属于物理变化的是( )A、液化气燃烧 B、铁锅生锈 C、开水沸腾 D、蔬菜腐烂2. 下列物质中,含有金属元素的是( )A、H2SO4 B、SiO2 C、KCl D、C2H5OH3. 下列物质的用途中,主要利用其物理性质的是( )A、氢气用于填充探空气球 B、红磷用于测空气中氧气含量 C、二氧化碳用于灭火 D、氮气用作食品保护气4. 分类法是化学学习的重要方法之 一。下列各组物质按照单质、 氧化物、混合物的顺序排列的是( )A、铁、二氧化碳、冰水混合物 B、液氧、高锰酸钾、洁净的空气 C、红磷、水、海水 D、稀有气体、五氧化二磷、食盐水5. 下列实验操作正确的是( )A、
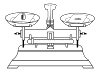 称量氯化钠
B、
称量氯化钠
B、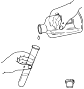 倾倒液体
C、
倾倒液体
C、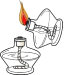 点燃酒精灯
D、
点燃酒精灯
D、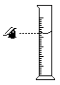 读取液体体积
6. 下列推理或归纳中正确的是( )A、某气体不能使带火星木条复燃,则该气体中一定不含氧气 B、单质是同种元素组成的纯净物,所以由同种元素组成的纯净物一定是单质 C、离子是带电荷的粒子,所以带电荷的粒子一定是离子 D、催化剂能增大化学反应速率,所以化学反应速率增大一定是因为加入了催化剂7. 两个集气瓶中分别集满氧气和二氧化碳。下列方法不能用于鉴别这两瓶气体的是( )A、分别闻两种气体的气味 B、分别加入紫色石蕊试液 C、分别伸入带火星的木条 D、分别通入澄清石灰水中8. “书香”中含有多种成分。随着时间推移,书籍中会释放出越来越多的糖醛(C5H4O2), 测它的含量可以检测书籍年代。下列关于糖醛的说法错误的是( )A、从宏观角度看: C5H4O2由三种元素组成 B、从微观角度看: C5H4O2中含有11 个原子 C、从质量角度看: C5H4O2中氢、 氧元素质量比为2:1 D、从变化角度看: C5H4O2 在氧气中完全燃烧生成水和二氧化碳9. 下列关于如图所示反应(条件已省略)的说法中,正确的是( )
读取液体体积
6. 下列推理或归纳中正确的是( )A、某气体不能使带火星木条复燃,则该气体中一定不含氧气 B、单质是同种元素组成的纯净物,所以由同种元素组成的纯净物一定是单质 C、离子是带电荷的粒子,所以带电荷的粒子一定是离子 D、催化剂能增大化学反应速率,所以化学反应速率增大一定是因为加入了催化剂7. 两个集气瓶中分别集满氧气和二氧化碳。下列方法不能用于鉴别这两瓶气体的是( )A、分别闻两种气体的气味 B、分别加入紫色石蕊试液 C、分别伸入带火星的木条 D、分别通入澄清石灰水中8. “书香”中含有多种成分。随着时间推移,书籍中会释放出越来越多的糖醛(C5H4O2), 测它的含量可以检测书籍年代。下列关于糖醛的说法错误的是( )A、从宏观角度看: C5H4O2由三种元素组成 B、从微观角度看: C5H4O2中含有11 个原子 C、从质量角度看: C5H4O2中氢、 氧元素质量比为2:1 D、从变化角度看: C5H4O2 在氧气中完全燃烧生成水和二氧化碳9. 下列关于如图所示反应(条件已省略)的说法中,正确的是( ) A、该反应的化学方程式为 B、反应前后,分子的种类一定发生改变 C、反应前后,元素的化合价都不会发生改变 D、反应物中的氧元素,在反应后完全转移到O2中10. 拉瓦锡曾做过著名的“20天实验”-------利用汞与氧气的反应研究空气的成分。他使用如图所示装置,将汞放在密闭容器里连续加热12天,最终观察到容器内气体体积减少了约1/5;再升高温度持续加热了8天,直到汞槽内液面不再变化为止,观察到曲颈甑内物质颜色与汞槽内的液面都恢复到实验前的样子。下列分析不合理的是( )
A、该反应的化学方程式为 B、反应前后,分子的种类一定发生改变 C、反应前后,元素的化合价都不会发生改变 D、反应物中的氧元素,在反应后完全转移到O2中10. 拉瓦锡曾做过著名的“20天实验”-------利用汞与氧气的反应研究空气的成分。他使用如图所示装置,将汞放在密闭容器里连续加热12天,最终观察到容器内气体体积减少了约1/5;再升高温度持续加热了8天,直到汞槽内液面不再变化为止,观察到曲颈甑内物质颜色与汞槽内的液面都恢复到实验前的样子。下列分析不合理的是( ) A、实验过程中,汞槽内的汞会倒吸入曲颈甑中 B、实验过程中,装置内至少发生两个化学反应 C、实验过程中汞的用量可能会影响实验结果 D、需待装置冷却至室温才能测量容器中气体的体积变化量
A、实验过程中,汞槽内的汞会倒吸入曲颈甑中 B、实验过程中,装置内至少发生两个化学反应 C、实验过程中汞的用量可能会影响实验结果 D、需待装置冷却至室温才能测量容器中气体的体积变化量二、填空题
-
11. 空气中含有多种成分,如图是空气成分示意图(按体积计算)。
 (1)、图中气体a是指。(2)、酥脆的饼干在空气中会逐渐变软,说明空气中含有。(3)、进入久未开启地客前,需用燃着的蜡烛做烛火实验(如图所示)。若蜡烛燃烧变弱甚至熄灭,说明地窖中氧气含量(填 “高于”或“低于”)正常值。
(1)、图中气体a是指。(2)、酥脆的饼干在空气中会逐渐变软,说明空气中含有。(3)、进入久未开启地客前,需用燃着的蜡烛做烛火实验(如图所示)。若蜡烛燃烧变弱甚至熄灭,说明地窖中氧气含量(填 “高于”或“低于”)正常值。 (4)、自然界中的碳循环(部分)如图所示。
(4)、自然界中的碳循环(部分)如图所示。
①“碳循环” 中循环的是 (填序号)。
A 碳单质 B 碳元素 C 碳酸钙 D 二氧化碳
②空气中二氧化碳持续增多易导致。
③二氧化碳由大气进入海水生成H2CO3的化学方程式为。
12. 天然水净化为自来水的主要流程如下: (1)、天然水中含有的部分杂质如下表所示,请根据表中内容回答问题。
(1)、天然水中含有的部分杂质如下表所示,请根据表中内容回答问题。溶解物质
悬浮物质
主要气体
主要离子
细菌、藻类、
泥沙、黏土
氧气(O2)、二氧化碳(CO2)硫化氢(H2S)
钙离子、 氯离子、硫酸根、铝离子
①上表“主要气体”中含有氧分子的有。
②写出“主要离子”中任意一种离子的符号。
(2)、下列说法错误的是(填序号)A 过滤池可以除去难溶性杂质
B 活性炭吸附池可以除去水中的色素和臭味
C 清水池中一定是软水
D 投药消毒环节发生了化学变化
(3)、常用的鉴别硬水和软水的方法是往水样中加入。(4)、电解水实验揭示了水的组成,装置如图所示。
①闭合开关后,收集到氧气的试管是(填“1”或“2”),反应的化学方程式为。
②该实验得出的关于水的组成的结论是。
13. 页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。(1)、页岩气的主要成分甲烷(CH4), 其完全燃烧的的产物为二氧化碳和水。甲烷在空气中完全燃烧的化学方程式为。(2)、页岩气做燃料,对于降低空气中SO2含量,解决酸雨污染具有重要作用。酸雨形成过程中,其中部分SO2会在一定条件下与O2反应转化成SO3 , 其微观示意图如下:
①该反应属于基本反应类型中的(填 “化合”或“分解”)反应。
②反应消耗的O2与生成的SO3的分子数之比为。
三、简答题
-
14. 物质都是由有微粒构成的,分子、原子、离子是构成物的基本微粒。(1)、找一个大小合适的瓶子,将燃着的纸条扔进瓶中,待燃烧结束后迅速将去壳的熟鸡蛋放在瓶口处,发现鸡蛋慢慢挤入瓶口。请从微观角度解释产生上述现象的原因。(2)、浓氨水可以使酚酞试液变成红色,它具有挥发性。往如图试管口的棉花滴浓氨水,再往滤纸条上从右往左依次滴上A、B、C三滴酚酞试液,可观察到的现象是; 此现象说明分子具有的性质。
 (3)、氮化镓(GaN)是“蓝色发光二极管”中的重要材料。已知镓元素(Ga)的原子结构示意图如图所示,则镓原子的质子数为 , 最外层电子数为 , 在化学反应中该原子容易(填“得到”或“失去”)电子形成(填“阴”或“阳”)离子。
(3)、氮化镓(GaN)是“蓝色发光二极管”中的重要材料。已知镓元素(Ga)的原子结构示意图如图所示,则镓原子的质子数为 , 最外层电子数为 , 在化学反应中该原子容易(填“得到”或“失去”)电子形成(填“阴”或“阳”)离子。
四、流程题
-
15. 氨气(NH3)的合成是人类科学技术上的重大突破。合成氨工艺的主要流程如下:
 (1)、合成塔中的反应必须在高温、高压并使用催化剂的条件下进行。该反应的化学方程式为。(2)、生产过程中可循环使用的物质是。(3)、将沸点不同的气体分离开来,常采用液化分离法。如:控制温度在-195.8℃ 至-183℃之间时,可将空气中N2与O2分离。根据下表中物质的沸点判断,要将产物NH3与N2、H2 分离开来,最适宜的温度应该控制在之间。
(1)、合成塔中的反应必须在高温、高压并使用催化剂的条件下进行。该反应的化学方程式为。(2)、生产过程中可循环使用的物质是。(3)、将沸点不同的气体分离开来,常采用液化分离法。如:控制温度在-195.8℃ 至-183℃之间时,可将空气中N2与O2分离。根据下表中物质的沸点判断,要将产物NH3与N2、H2 分离开来,最适宜的温度应该控制在之间。物质
H2
N2
O2
NH3
沸点
-252℃
-195.8℃
-183℃
-33.35℃
五、实验题
-
16. 用下图所示实验装置可以制取多种气体。
 (1)、写出仪器a、b的名称: a是、b是。(2)、向气体发生装置内加入药品前,应该先进行的操作是。(3)、实验室制取二氧化碳时,发生装置应选用(填序号,下同),写出发生反应的化学方程式。(4)、收集二氧化碳可以选择的装置为(填一种),依据是。(5)、实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水。制取氨气的化学方程式为 , X的化学式为。制取并收集氨气应该从图中选择的发生装置是 , 收集装置是 。
(1)、写出仪器a、b的名称: a是、b是。(2)、向气体发生装置内加入药品前,应该先进行的操作是。(3)、实验室制取二氧化碳时,发生装置应选用(填序号,下同),写出发生反应的化学方程式。(4)、收集二氧化碳可以选择的装置为(填一种),依据是。(5)、实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水。制取氨气的化学方程式为 , X的化学式为。制取并收集氨气应该从图中选择的发生装置是 , 收集装置是 。六、科学探究题
-
17. 为加深对燃烧条件的认识,化学研究性学习小组设计并进行了如下实验。
 (1)、实验一: 用棉花分别蘸酒精和水,放到酒精灯火焰上加热片刻,观察到蘸酒精的棉花燃烧,蘸水的棉花不燃烧,可以得出燃烧的条件之一是。(2)、实验二:已知乒乓球的材料和滤纸都是可燃物。如图所示,将同样大小的乒乓球碎片和滤纸碎片放在薄铜片的两侧,用酒精灯加热铜片中部。此实验的目的是; 取同样大小的乒乓球碎片和滤纸碎片,是为了。(3)、实验三:用如图所示装置进行镁条在空气中燃烧的实验。镁条燃烧、冷却后打开止水夹,进入集气瓶中的水的体积约占集气瓶容积的70%。
(1)、实验一: 用棉花分别蘸酒精和水,放到酒精灯火焰上加热片刻,观察到蘸酒精的棉花燃烧,蘸水的棉花不燃烧,可以得出燃烧的条件之一是。(2)、实验二:已知乒乓球的材料和滤纸都是可燃物。如图所示,将同样大小的乒乓球碎片和滤纸碎片放在薄铜片的两侧,用酒精灯加热铜片中部。此实验的目的是; 取同样大小的乒乓球碎片和滤纸碎片,是为了。(3)、实验三:用如图所示装置进行镁条在空气中燃烧的实验。镁条燃烧、冷却后打开止水夹,进入集气瓶中的水的体积约占集气瓶容积的70%。
[查阅资料]
①镁条在氧气中燃烧的反应化学方程式为。
②镁条在氮气中能燃烧,产物为氮化镁固体。氮化镁中氮元素显-3价,则氮化镁的化学式为。
③镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁。
(4)、[交流讨论]通过该实验,你对燃烧有了什么新的认识? (写出一点即可)七、计算题
-
18. 今年9月30日正式上映的影片<攀登者>讲述了1960年5月25日中国登山队成功完成人类首次北坡登顶珠峰的故事。据统计:每位登山运动员在攀登珠穆朗玛峰冲顶时至少消耗自带的液氧4.8kg.求:(1)、这些氧气在标准状况下的体积是升(计算结果保留一位小数,下同:标准状况下氧气密度为1.43g/L).(2)、若用高锰酸钾为原料制取相同质量的氧气,需要多少千克的高锰酸钾?(反应的化学方程式为 )
-
-
-
-