专题02:电离
试卷更新日期:2020-08-24 类型:一轮复习
一、单选题
-
1. 反应NH4Cl+NaNO2=NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列化学用语错误的是( )A、N2的电子式:
 B、NH4Cl的电离方程式:NH4Cl=NH4++Cl-
C、Cl原子的结构示意图:
B、NH4Cl的电离方程式:NH4Cl=NH4++Cl-
C、Cl原子的结构示意图:  D、H2O的结构式:
D、H2O的结构式:  2. 下列化学用语书写正确的是( )A、次氯酸的电离方程式:HClO=H++ClO- B、硫化钠水解的离子方程式:S2-+2H2O H2S+2OH- C、电解精炼铜的阴极反应式:Cu-2e-=Cu2+ D、碳酸钙的溶解平衡:CaCO3(s) Ca2+(aq)+CO32-(aq)3. 下列化学用语表示正确的是( )A、乙醇的分子式:CH3CH2OH B、NH3的电子式:
2. 下列化学用语书写正确的是( )A、次氯酸的电离方程式:HClO=H++ClO- B、硫化钠水解的离子方程式:S2-+2H2O H2S+2OH- C、电解精炼铜的阴极反应式:Cu-2e-=Cu2+ D、碳酸钙的溶解平衡:CaCO3(s) Ca2+(aq)+CO32-(aq)3. 下列化学用语表示正确的是( )A、乙醇的分子式:CH3CH2OH B、NH3的电子式: C、Cl-的结构示意图:
C、Cl-的结构示意图:  D、NaHCO3的电离方程式:NaHCO3 = Na+ + HCO
4. 常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示,混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,不正确的是( )
D、NaHCO3的电离方程式:NaHCO3 = Na+ + HCO
4. 常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示,混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,不正确的是( )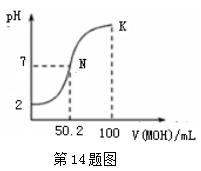 A、HA的电离方程式为:HA=H++A- B、MOH为一元弱碱 C、K点对应的溶液中有:c(MOH)+c(M+)=0.02mol
A、HA的电离方程式为:HA=H++A- B、MOH为一元弱碱 C、K点对应的溶液中有:c(MOH)+c(M+)=0.02mol L-1
D、N点对应的溶液中有:c(M+)=c(A-)
5. 下列物质溶于水的电离方程式正确的是( )A、Al2(SO4)3 = 2Al3+ + 3SO42- B、NaHCO3 = Na+ + H++ CO32- C、NaHSO4= Na+ + HSO4- D、 KClO3 = K+ + Cl-+ 3O2-6. 下列方程式书写错误的是( )A、HCO3-的电离方程式:HCO3-+H2O
L-1
D、N点对应的溶液中有:c(M+)=c(A-)
5. 下列物质溶于水的电离方程式正确的是( )A、Al2(SO4)3 = 2Al3+ + 3SO42- B、NaHCO3 = Na+ + H++ CO32- C、NaHSO4= Na+ + HSO4- D、 KClO3 = K+ + Cl-+ 3O2-6. 下列方程式书写错误的是( )A、HCO3-的电离方程式:HCO3-+H2O H3O++CO32-
B、Cu2+的水解方程式:Cu2++2H2O
H3O++CO32-
B、Cu2+的水解方程式:Cu2++2H2O  Cu(OH)2+2H+
C、NH4+的水解方程式:NH4++2H2O
Cu(OH)2+2H+
C、NH4+的水解方程式:NH4++2H2O  NH3·H2O+H3O+
D、CaCO3的电离方程式:CaCO3
NH3·H2O+H3O+
D、CaCO3的电离方程式:CaCO3  Ca2++CO32-
7. 下列说法正确的是( )A、碳酸氢钠在水溶液中的电离方程式为:NaHCO3 = Na+ + H+ + CO32- B、可溶性盐在水中完全电离是强电解质,难溶性盐在水中溶解度很小是弱电解质 C、强电解质的水溶液导电性不一定强于弱电解质的水溶液 D、强电解质都是离子化合物,在水溶液或熔融状态下完全电离,以离子形式存在
Ca2++CO32-
7. 下列说法正确的是( )A、碳酸氢钠在水溶液中的电离方程式为:NaHCO3 = Na+ + H+ + CO32- B、可溶性盐在水中完全电离是强电解质,难溶性盐在水中溶解度很小是弱电解质 C、强电解质的水溶液导电性不一定强于弱电解质的水溶液 D、强电解质都是离子化合物,在水溶液或熔融状态下完全电离,以离子形式存在二、填空题
-
8. 写出下列物质在水溶液中的电离方程式:(1)、硫酸铝。(2)、碳酸氢铵。9. 有以下几种物质①碳酸氢钠晶体②液态氯化氢③铁④蔗糖⑤酒精⑥熔融的K2SO4⑦干冰⑧石墨填空回答:(填序号)(1)、以上物质能导电的是(2)、以上物质中属于电解质的是(3)、以上物质中属于非电解质的是(4)、以上物质中溶于水后水溶液能导电的是(5)、分别写出物质①、⑥在水溶液中的电离方程式、 .10. 按要求填空。(1)、①石墨②盐酸③胆矾④KOH固体⑤Fe⑥氨水⑦乙醇⑧醋酸⑨NaCl溶液⑩CO2⑪熔融BaSO4 , 能导电的是电解质是(2)、写出下列物质的电离方程式:①NaHSO4 , ②NaHCO3。(3)、写出下列反应的离子方程式:①氢氧化铜与稀盐酸反应 , ②氢氧化钡与稀硫酸反应 , ③碳酸钙与硝酸反应 , ④氧化铁与稀盐酸反应。
三、综合题
-
11. 现有下列六种物质:①Al②熔融KHSO4 ③Ba(OH)2固体④CO2 ⑤盐酸⑥Fe(OH)3胶体,请回答下列问题。(1)、上述物质中,属于强碱的是(填写物质的序号,下同),属于非电解质的是。在题中状态下既是电解质又能导电的是。(2)、①投入③的溶液中反应的离子方程式为。(3)、对物质⑥进行通电,观察到与电源负极相连的电极附近的现象是 , 可证明Fe(OH)3胶粒带电荷(填“ 正 ”或“ 负 ”) 。(4)、写出②在该状态下的电离方程式为。(5)、在③的水溶液中通入过量的④,请写出该反应的离子方程式为。12.(1)、元素的种类由决定。(2)、19 g 某二价金属的氯化物 ACl2 中含有 0.4mol Cl- , 则 A 的摩尔质量为。(3)、molSO2中含有的O原子数与标准状况下4.48L的NH3的氢原子数相同。(4)、NaHSO4在熔化状态下的电离方程式:。13. 根据已经学过的化学知识,回答下列问题。(1)、I.现有下列十种物质:①蔗糖 ②熔融KNO3 ③石墨 ④铜丝 ⑤NaOH固体 ⑥SO3 ⑦BaSO4固体 ⑧K2O固体 ⑨液态H2SO4 ⑩液氯 上述物质中可导电的是(填序号,下同);上述物质中不能导电,但属于电解质的是。(2)、NaHSO4是一种酸式盐,请填写下列空白:
①写出NaHSO4在水中的电离方程式 。
②与0.1 mol·L-1的NaHSO4溶液的导电能力相同的硫酸钠溶液的物质的量浓度为:。
③NaHSO4溶液与NaHCO3溶液反应的离子方程式为。
(3)、粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用,①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序依次是。(4)、II.A,B,C,X均为中学常见物质,它们在一定条件下有如下转化关系(副产物已略去)。
若X是氧气,则A不可能 (填序号)
A.C B.Si C.Na D.Mg
(5)、若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生了不溶于稀HNO3的白色沉淀,则B的化学式为;C溶液在贮存时应加入少量X,理由是(用离子方程式表示)。检验B溶液中阳离子的操作方法是。(6)、若X是氢氧化钠溶液,A、B、C均为含铝元素的化合物,则反应②的离子方程式为。