初中化学人教版九年级上册 第三单元课题3 元素
试卷更新日期:2020-08-20 类型:同步测试
一、单选题
-
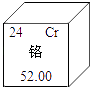
1. 下列微粒中不能直接构成物质的是( )A、分子 B、原子 C、中子 D、离子2. 铬元素在元素周期表中信息如图所示,下列有关铬元素的说法错误的是( )
 A、原子序数是24 B、属于金属元素 C、一个铬原子核外有28个电子 D、相对原子质量为52.003. 下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )A、O B、Cu C、N2 D、CO24. 如图摘自元素周期表,据此判断下列叙述错误的是( )
A、原子序数是24 B、属于金属元素 C、一个铬原子核外有28个电子 D、相对原子质量为52.003. 下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )A、O B、Cu C、N2 D、CO24. 如图摘自元素周期表,据此判断下列叙述错误的是( ) A、氧的相对原子质量为16.00 B、硫原子的核外电子数为16 C、氧和硫都属于非金属元素 D、氧和硫位于元素周期表同一周期5. 决定元素种类的是( )A、质子数 B、中子数 C、最外层电子数 D、电子数6. 下列物质由离子构成的是( )A、氢气 B、氯化钾 C、金刚石 D、二氧化碳7. Mg和Mg2+这两种粒子具有相同的( )A、核外电子数 B、化学性质 C、质子数 D、电子层数8. 生活中人们使用碘盐,其中的“碘”指的是( )A、分子 B、原子 C、离子 D、元素9. “富硒猕猴桃”中的“硒”是指( )A、硒原子 B、硒元素 C、硒单质 D、硒分子10. 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是最小的粒子,不可再分 D、氯化钠是由钠离子和氯离子构成的
A、氧的相对原子质量为16.00 B、硫原子的核外电子数为16 C、氧和硫都属于非金属元素 D、氧和硫位于元素周期表同一周期5. 决定元素种类的是( )A、质子数 B、中子数 C、最外层电子数 D、电子数6. 下列物质由离子构成的是( )A、氢气 B、氯化钾 C、金刚石 D、二氧化碳7. Mg和Mg2+这两种粒子具有相同的( )A、核外电子数 B、化学性质 C、质子数 D、电子层数8. 生活中人们使用碘盐,其中的“碘”指的是( )A、分子 B、原子 C、离子 D、元素9. “富硒猕猴桃”中的“硒”是指( )A、硒原子 B、硒元素 C、硒单质 D、硒分子10. 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是最小的粒子,不可再分 D、氯化钠是由钠离子和氯离子构成的二、填空题
-
11. 、 、 分别表示氢元素的三种原子,可简写成 ,2H,3H。制造燃料电池常用1H,制造氢弹要用2H,3H,请据下图回答:
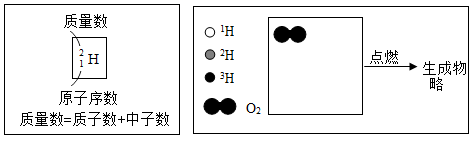 (1)、1H,2H,3H三种原子中,数目不等(填“质子”或“中子”或“电子”)。(2)、2H2与O2反应生成的重水可表示为2H2O。写出3H2在O2中燃烧的化学方程式。12. 元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
(1)、1H,2H,3H三种原子中,数目不等(填“质子”或“中子”或“电子”)。(2)、2H2与O2反应生成的重水可表示为2H2O。写出3H2在O2中燃烧的化学方程式。12. 元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:族
周期
I A
II A
IIIA
IVA
VA
VIA
VIIA
0
2
3 Li
锂
6.941
4 Be
铍
9.012
5 B
硼
10.81
6 C
碳
12.01
7 N
氮
14.01
8 O
氧
16.00
9 F
氟
19.00
10 Ne
氖
20.18
3
11 Na
钠
22.99
12 Mg
镁
24.31
13 Al
铝
26.98
14 Si
硅
28.09
15 P
磷
30.97
16 S
硫
32.06
17 Cl
氯
35.45
18 Ar
氩
39.95
(1)、请从上表中查出关于氟元素的一条信息:。(2)、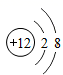 写出该结构简图的微粒符号。 (3)、第13号元素与第17号元素组成的化合物的化学式是 。(4)、在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是____________(填字母序号)。A、Be和Mg B、C和Ne C、Al和Si D、F和Cl
写出该结构简图的微粒符号。 (3)、第13号元素与第17号元素组成的化合物的化学式是 。(4)、在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是____________(填字母序号)。A、Be和Mg B、C和Ne C、Al和Si D、F和Cl三、综合题
-
13. 如图是元素周期表的一部分
 (1)、请你写出其中一种与氖原子(Ne)核外电子数相同的阴离子的符号;(2)、11号元素和17号元素形成化合物的化学式是。写出镓的氧化物的化学式;(3)、第三周期原子元素原子核外电子排布的变化规律是;(4)、请根据图2推断嫁元素在周期表中位于第周期.14.(1)、硫元素的质子数是 , 它属于(填“金属”或“非金属”)元素,在化学反应中容易(填“得到”或“失去”)电子.
(1)、请你写出其中一种与氖原子(Ne)核外电子数相同的阴离子的符号;(2)、11号元素和17号元素形成化合物的化学式是。写出镓的氧化物的化学式;(3)、第三周期原子元素原子核外电子排布的变化规律是;(4)、请根据图2推断嫁元素在周期表中位于第周期.14.(1)、硫元素的质子数是 , 它属于(填“金属”或“非金属”)元素,在化学反应中容易(填“得到”或“失去”)电子. (2)、表中不同种元素最本质的区别是_____(填序号);A、质子数不同 B、中子数不同 C、相对原子质量不同(3)、在第三周期中,各原子结构的共同之处是;该周期中,各原子核外电子排布的变化规律是 .(4)、在第三周期中,元素类型的变化情况是:从左到右由元素过渡到元素,并以稀有气体元素结尾.(5)、纵列的原子核外电子排布的共同之处是 .(6)、研究表明,第二周期从3号-9号元素的原子随着核电荷数逐渐增大,原子核对核外电子的引力逐渐增大,因此原子半径逐渐减小,从而可以推断出第三周期11号-17号元素的原子半径变化规律是 .
(2)、表中不同种元素最本质的区别是_____(填序号);A、质子数不同 B、中子数不同 C、相对原子质量不同(3)、在第三周期中,各原子结构的共同之处是;该周期中,各原子核外电子排布的变化规律是 .(4)、在第三周期中,元素类型的变化情况是:从左到右由元素过渡到元素,并以稀有气体元素结尾.(5)、纵列的原子核外电子排布的共同之处是 .(6)、研究表明,第二周期从3号-9号元素的原子随着核电荷数逐渐增大,原子核对核外电子的引力逐渐增大,因此原子半径逐渐减小,从而可以推断出第三周期11号-17号元素的原子半径变化规律是 .