高中化学人教版(新课标)选修4 第二章第一节 化学反应速率
试卷更新日期:2020-08-20 类型:同步测试
一、单选题
-
1. 下列生产生活中需要增大化学反应速率的是( )A、铁桥生锈
 B、牛奶变质
B、牛奶变质  C、塑料老化
C、塑料老化  D、高炉炼铁
D、高炉炼铁  2. 在一定温度下,向2L密闭容器中加入2molHI(g),发生反应2HI(g) H2(g)+I2(g),4s时生成0.2molH2 , 则以HI表示该时段的化学反应速率是( )A、0.05mol·L-1·s-1 B、0.1mol·L-1·s-1 C、0.2mol·L-1·s-1 D、0.8mol·L-1·s-13. 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
2. 在一定温度下,向2L密闭容器中加入2molHI(g),发生反应2HI(g) H2(g)+I2(g),4s时生成0.2molH2 , 则以HI表示该时段的化学反应速率是( )A、0.05mol·L-1·s-1 B、0.1mol·L-1·s-1 C、0.2mol·L-1·s-1 D、0.8mol·L-1·s-13. 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( ) A、反应开始到10s,用Z表示的反应速率为0.158mol(Ls)-1 B、反应开始到10s,X的物质的量浓度减少了0.79mol·L-1 C、反应开始到10s时,Y的转化率为79.0% D、反应的化学方程式为:X(g)+Y(g) Z(g)4. 已知某反应的各物质浓度数据如下:
A、反应开始到10s,用Z表示的反应速率为0.158mol(Ls)-1 B、反应开始到10s,X的物质的量浓度减少了0.79mol·L-1 C、反应开始到10s时,Y的转化率为79.0% D、反应的化学方程式为:X(g)+Y(g) Z(g)4. 已知某反应的各物质浓度数据如下:aA(g)+
bB(g)
2C(g)
起始(mol/L)
3.0
1.0
0
2 s末浓度(mol/L)
1.8
0.6
0.8
据此可推算出上述反应化学方程式中,各物质的化学计量数之比是( )
A、9∶3∶4 B、3∶1∶2 C、2∶1∶3 D、3∶2∶15. 在密闭容器里,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知3v(B)=2v(A)、2v(C)=3v(B),则此反应可表示为( )A、2A+3B=2C B、A+3B=2C C、3A+2B=3C D、A+B=C6. 对于可逆反应A(g)+3B(g) 2C(g)+D(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )A、v(A)=0.1mol·L-1·s-1 B、v(B)=0.6mol·L-1·s-1 C、v(C)=0.9 mol·L-1 min-1 D、υ(D)=1.2mol·L-1·min-17. 某温度时,在2L容器中三种物质的物质的量随时间的变化曲线如下图所示。由图中数据分析,该反应的化学方程式和反应开始至2min末Z的平均反应速率为( )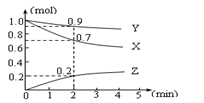 A、3X + Y 2Z;0.05mol·L-1·min-1 B、2X + Y 2Z;0.1mol·L-1·min-1 C、X + 2Y =Z;0.1mol·L-1·min-1 D、X + 3Y =2Z;0.05mol·L-1·min-18. 把3molX气体和1moY气体混合于容积为1L的容器中,使其发生如下反应:
A、3X + Y 2Z;0.05mol·L-1·min-1 B、2X + Y 2Z;0.1mol·L-1·min-1 C、X + 2Y =Z;0.1mol·L-1·min-1 D、X + 3Y =2Z;0.05mol·L-1·min-18. 把3molX气体和1moY气体混合于容积为1L的容器中,使其发生如下反应:3X(g)+Y(g) nZ(g)+2W(g)。2min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.1mol·L-1·min-1 , 则n的值为( )
A、1 B、2 C、3 D、4二、综合题
-
9. 向体积为V L的恒容容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下图所示。已知在反应过程中混合气体的总的物质的量没有变化。请回答:
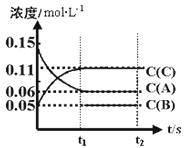 (1)、V =。(2)、若t1=15s时,则0-t1阶段以C物质浓度变化表示的反应速率v(C)=。(3)、写出反应的化学方程式:。10. 某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
(1)、V =。(2)、若t1=15s时,则0-t1阶段以C物质浓度变化表示的反应速率v(C)=。(3)、写出反应的化学方程式:。10. 某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: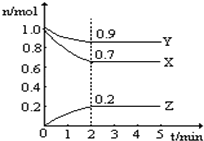 (1)、该反应的化学方程式为;(2)、反应开始至2min,以气体Z表示的平均反应速率为;(3)、混合气体的平均相对分子质量比起始时;(填“大”,“小”或“相等”)
(1)、该反应的化学方程式为;(2)、反应开始至2min,以气体Z表示的平均反应速率为;(3)、混合气体的平均相对分子质量比起始时;(填“大”,“小”或“相等”)平衡时容器内混合气体密度比起始时(填“大”,“小”或“相等”)
(4)、将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b= .