安徽省淮北市相山区2019-2020学年九年级上学期化学第四次月考试卷
试卷更新日期:2020-08-19 类型:月考试卷
一、单选题
-
1. 人类生活中的衣、食、住、行都离不开化学.下列涉及化学变化的是( )A、衣:棉布制成衣服 B、食:大豆制成豆浆 C、住:石块砌成房屋 D、行:燃油驱动汽车2. 联合国气候变化大会于2015年11月30日~12月11日在巴黎举行,会议旨在通过限制人类活动减少对环境的破坏。下列有关做法错误的是( )
 A、禁止农作物秸秆燃烧,减轻对雾霾影响 B、用二氧化碳和水等合成新型燃油,有利于减缓温室效应 C、减少燃煤发电,增加太阳能发电,减少酸雨 D、大量使用化肥、农药,提高农作物产量3. 实验操作有误或不规范,很可能造成失败甚至酿成事故。下列实验操作正确的是( )A、
A、禁止农作物秸秆燃烧,减轻对雾霾影响 B、用二氧化碳和水等合成新型燃油,有利于减缓温室效应 C、减少燃煤发电,增加太阳能发电,减少酸雨 D、大量使用化肥、农药,提高农作物产量3. 实验操作有误或不规范,很可能造成失败甚至酿成事故。下列实验操作正确的是( )A、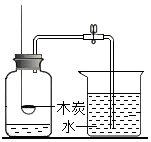 测量氧气含量
B、
测量氧气含量
B、 检验装置气密性
C、
检验装置气密性
C、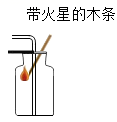 验满氧气
D、
验满氧气
D、 存放氧气
4. 中国科学家屠呦呦因从青蒿中提取到了对疟原虫有100%的抑制率的青蒿素(C15H22O5)而获2015年诺贝尔生理学或医学奖,成为第一个获得诺贝尔自然科学奖的中国人。下列关于青蒿素的说法错误的是( )A、青蒿素由碳、氢、氧三种元素组成 B、青蒿素中碳、氢、氧原子的个数比为15︰22︰5 C、青蒿素中碳元素质量分数最大 D、青蒿素属于氧化物5. 铁、钴、镍是化学性质相似的三种元素,它们在元素周期表中的位置如下图所示。据此判断下列说法中错误的( )
存放氧气
4. 中国科学家屠呦呦因从青蒿中提取到了对疟原虫有100%的抑制率的青蒿素(C15H22O5)而获2015年诺贝尔生理学或医学奖,成为第一个获得诺贝尔自然科学奖的中国人。下列关于青蒿素的说法错误的是( )A、青蒿素由碳、氢、氧三种元素组成 B、青蒿素中碳、氢、氧原子的个数比为15︰22︰5 C、青蒿素中碳元素质量分数最大 D、青蒿素属于氧化物5. 铁、钴、镍是化学性质相似的三种元素,它们在元素周期表中的位置如下图所示。据此判断下列说法中错误的( )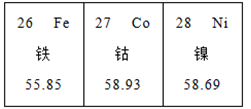 A、镍元素的符号为Ni B、钴元素的相对原子质量是58.93g C、各元素都属于金属元素 D、从左到右各元素的原子序数依次增大6. 我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破,其成果在最近的美国《科学》杂志上发表。该转化的微观示意图如下,有关转化的说法错误的是( )
A、镍元素的符号为Ni B、钴元素的相对原子质量是58.93g C、各元素都属于金属元素 D、从左到右各元素的原子序数依次增大6. 我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破,其成果在最近的美国《科学》杂志上发表。该转化的微观示意图如下,有关转化的说法错误的是( )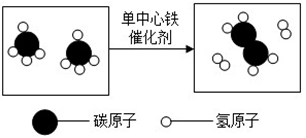 A、催化剂改变了反应速率 B、反应前后原子的种类发生了变化 C、生成物之一为 C2H4 D、该反应为分解反应7. 科学家发现火星大气层中含有一种称为硫化羰的物质,化学式为COS。已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧。下列有关硫化羰的说法错误的是( )A、硫化羰可作为理想燃料 B、硫化羰是由分子构成的 C、硫化羰完全燃烧会生成CO2和SO2两种氧化物 D、硫化羰不能用作灭火剂8. 如图是某个化学反应的微观示意图,从示意图中获取的信息错误的是( )
A、催化剂改变了反应速率 B、反应前后原子的种类发生了变化 C、生成物之一为 C2H4 D、该反应为分解反应7. 科学家发现火星大气层中含有一种称为硫化羰的物质,化学式为COS。已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧。下列有关硫化羰的说法错误的是( )A、硫化羰可作为理想燃料 B、硫化羰是由分子构成的 C、硫化羰完全燃烧会生成CO2和SO2两种氧化物 D、硫化羰不能用作灭火剂8. 如图是某个化学反应的微观示意图,从示意图中获取的信息错误的是( )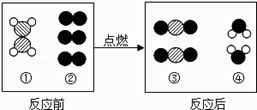 A、图①分子中两种原子的个数比为1:2 B、图②对应的物质是单质 C、参加反应的分子个数比为2:3 D、反应后生成的物质都是化合物9. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、化合物是含有不同元素的纯净物,则含有不同种元素的纯净物一定是化合物 B、铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用 C、化学反应常常伴有能量变化一—有能量改变的变化都是化学反应 D、分子、原子可以构成物质,则物质一定都是由分子、原子构成的10. 有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快;再将甲投入含丁的化合物的溶液中,甲的表面有丁析出,则这四种金属活动性顺序为( )A、甲>乙>丙>丁 B、丙>乙>甲>丁 C、丙>乙>丁>甲 D、丁>甲>乙>丙
A、图①分子中两种原子的个数比为1:2 B、图②对应的物质是单质 C、参加反应的分子个数比为2:3 D、反应后生成的物质都是化合物9. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、化合物是含有不同元素的纯净物,则含有不同种元素的纯净物一定是化合物 B、铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用 C、化学反应常常伴有能量变化一—有能量改变的变化都是化学反应 D、分子、原子可以构成物质,则物质一定都是由分子、原子构成的10. 有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快;再将甲投入含丁的化合物的溶液中,甲的表面有丁析出,则这四种金属活动性顺序为( )A、甲>乙>丙>丁 B、丙>乙>甲>丁 C、丙>乙>丁>甲 D、丁>甲>乙>丙二、填空题
-
11. 高速铁路可以加快出行步伐.2015年12月6日,南京至安庆高铁将正式开通运营,使苏、皖、赣、鄂四省连为一体.结合所学化学知识,回答下列问题:(1)、图中标示的物质中为金属材料的是(填序号),动车电路中的导线大多是用铜制的,这是利用了铜的延展性和性.
 (2)、动车表面喷漆主要是为了防止外壳生锈,其原理是 .(3)、修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得.写出一氧化碳和赤铁矿炼铁的化学反应方程式 .(4)、高铁列车车厢是密闭的空间,因此提供清洁的空气、保持车厢卫生非常重要.高铁酸钠(Na2FeO4)是高铁列车上常用的一种“绿色环保高效”消毒剂,其中高铁酸钠中铁元素化合价为 .12.
(2)、动车表面喷漆主要是为了防止外壳生锈,其原理是 .(3)、修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得.写出一氧化碳和赤铁矿炼铁的化学反应方程式 .(4)、高铁列车车厢是密闭的空间,因此提供清洁的空气、保持车厢卫生非常重要.高铁酸钠(Na2FeO4)是高铁列车上常用的一种“绿色环保高效”消毒剂,其中高铁酸钠中铁元素化合价为 .12.通过一年的化学学习,相信你已经掌握了一些化学知识与技能.请结合下列实验装置图回答问题.
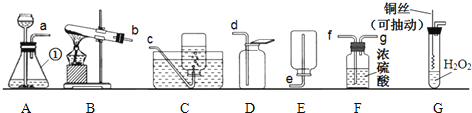 (1)、写出图中①的仪器名称: ;
(1)、写出图中①的仪器名称: ;
(2)、实验室用过氧化氢制取氧气的化学方程式为 ,实验室用此反应原理制取并收集一瓶干燥的氧气,应选用的装置连接顺序为 (选填小写字母).(3)、实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过加热处理.改进后的发生装置如图H所示(已略去夹持装置).①铜丝绕成螺旋状的作用是 .
A.收集到更多的氧气 B.加快反应速率 C.没有影响
②与装置A比较,改进后装置的优点是 .
(4)、实验室常用锌粒和稀硫酸反应制取氢气,应选用的发生和收集装置为 (选填字母).三、流程题
-
13. 素有“铜都”之称的安徽铜陵有许多黄铜矿(主要成分为CuFeS2)。黄铜矿经初步处理后,所得溶液甲中含有Fe2(SO4)3、CuSO4及H2SO4.某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如下图所示
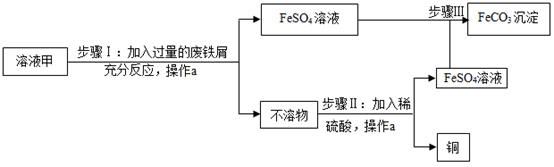 (1)、Fe2(SO4)3与铁反应的化学方程式如下,请配平:xFe2(SO4)3+yFe=zFeSO4 , 其中x、y、z为化学计量数,z的值为。(2)、步骤I中,生成铜的化学方程式。废铁屑要求过量,原因是。(3)、操作a名称为。实验室中操作a要用到玻璃棒、烧杯和等玻璃仪器。(4)、不溶物的成分为(填化学式)。
(1)、Fe2(SO4)3与铁反应的化学方程式如下,请配平:xFe2(SO4)3+yFe=zFeSO4 , 其中x、y、z为化学计量数,z的值为。(2)、步骤I中,生成铜的化学方程式。废铁屑要求过量,原因是。(3)、操作a名称为。实验室中操作a要用到玻璃棒、烧杯和等玻璃仪器。(4)、不溶物的成分为(填化学式)。四、科学探究题
-
14. 人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使叮咬处又痛又痒。化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究。
(提出问题)蚁酸的成分是什么?它有什么性质?
(查阅资料)Ⅰ.蚁酸是一种有机酸,化学名称叫做甲酸,化学式为 HCOOH。
Ⅱ.蚁酸在隔绝空气条件下加热会分解生成两种氧化物
(实验探究)
(1)、向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到石蕊试液颜色变成色,说明蚁酸溶液显酸性。(2)、小芳同学根据蚁酸中含有元素,推测出乙酸热分解的一种生成物是水。(3)、另一种生成的氧化物是气体,小敏提出两种猜想:①猜想Ⅰ:该气体是CO2;猜想Ⅱ:该气体是。
他们将蚁酸分解产生的气体通过下图的装置:
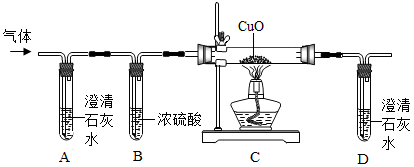
②实验时装置A中无明显变化,则猜想Ⅰ(填“成立”或“不成立”).
(讨论交流)从环保角度看,该装置存在明显的缺陷,处理方法是。
(拓展延伸)由以上信息可知,蚁酸和碳酸虽然组成元素相同,但是他们的化学性质却不相同原因。
15. 资料显示:炭还原四氧化三铁制得铁的温度在700℃-800℃。某校化学兴趣小组在探究用炭冶炼铁的原理的实验时,取一定质量的炭粉和四氧化三铁粉的混合物,在700℃-800℃的高温条件下使其充分反应,设计的实验装置如图: (1)、写出炭还原四氧化三铁的化学方程式。该实验中观察到的实验现象是:。对反应后试管中剩余的固体是什么,兴趣小组的同学做出了如下猜想:甲同学认为是铁粉,乙同学认为是炭粉和铁粉的混合物,丙同学的猜想。(2)、乙同学设计一个用化学方法证明自己的猜想是否正确,他的方法是。理由是。(3)、丙同学认为要验证自己的猜想是否正确可用磁铁去吸引,你认为丙同学的实验方案是否可行: , 理由是。请你设计一个实验证明丙同学的猜想。
(1)、写出炭还原四氧化三铁的化学方程式。该实验中观察到的实验现象是:。对反应后试管中剩余的固体是什么,兴趣小组的同学做出了如下猜想:甲同学认为是铁粉,乙同学认为是炭粉和铁粉的混合物,丙同学的猜想。(2)、乙同学设计一个用化学方法证明自己的猜想是否正确,他的方法是。理由是。(3)、丙同学认为要验证自己的猜想是否正确可用磁铁去吸引,你认为丙同学的实验方案是否可行: , 理由是。请你设计一个实验证明丙同学的猜想。五、计算题
-
16. 欲测定某锌 铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数
第一次
第二次
第三次
加入稀硫酸质量
20
20
20
生成气体质量
m
请回答下列问题并计算:
(1)、第二次实验时生成气体质量 克;(2)、计算该合金样品中铜的质量分数 .
-