辽宁省锦州市2020年中考化学试卷
试卷更新日期:2020-08-17 类型:中考真卷
一、单选题
-
1. 下列变化不属于化学变化的是( )A、动物呼吸 B、金属生锈 C、食物腐烂 D、海水晒盐2. 下列实验操作正确的是( )A、熄灭酒精灯
 B、称量氯化钠
B、称量氯化钠 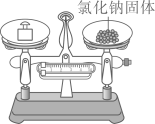 C、取用固体粉末
C、取用固体粉末 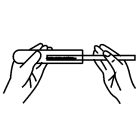 D、测溶液pH
D、测溶液pH 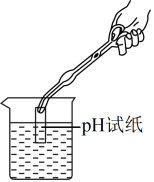 3. 化学在健康、能源、材料、生活等方面有广泛的应用。下列说法正确的是( )A、装修材料挥发出来的甲醛对人体有害 B、化石燃料属于可再生能源,太阳能、风能、氢能属于新能源 C、合成材料包括塑料、合金和合成橡胶 D、涤纶衣服的优点是吸湿性、透气性好4. 下列说法错误的是( )A、氧气能支持燃烧,可作燃料 B、活性炭可除去冰箱中的异味 C、二氧化碳可用于灭火 D、食品包装中充入氮气防腐5. 某消毒液标签的部分内容如图所示,下列说法正确的是( )
3. 化学在健康、能源、材料、生活等方面有广泛的应用。下列说法正确的是( )A、装修材料挥发出来的甲醛对人体有害 B、化石燃料属于可再生能源,太阳能、风能、氢能属于新能源 C、合成材料包括塑料、合金和合成橡胶 D、涤纶衣服的优点是吸湿性、透气性好4. 下列说法错误的是( )A、氧气能支持燃烧,可作燃料 B、活性炭可除去冰箱中的异味 C、二氧化碳可用于灭火 D、食品包装中充入氮气防腐5. 某消毒液标签的部分内容如图所示,下列说法正确的是( ) A、该消毒液为纯净物 B、NaClO是由钠原子、氯原子、氧原子组成的 C、NaClO的相对分子质量为74.5g D、NaClO中钠、氯、氧元素的质量比为46:71:326. 下列客现事实对应的微观解释错误的是( )A、酒香不怕巷子深——分子在不断运动 B、金属很难被压缩——分子间没有间隔 C、过氧化氢溶液是混合物——由不同种分子构成 D、金刚石、石墨的物理性质差异较大——碳原子的排列方式不同7. 向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。下列液体X和固体Y的组合,正确的是( )
A、该消毒液为纯净物 B、NaClO是由钠原子、氯原子、氧原子组成的 C、NaClO的相对分子质量为74.5g D、NaClO中钠、氯、氧元素的质量比为46:71:326. 下列客现事实对应的微观解释错误的是( )A、酒香不怕巷子深——分子在不断运动 B、金属很难被压缩——分子间没有间隔 C、过氧化氢溶液是混合物——由不同种分子构成 D、金刚石、石墨的物理性质差异较大——碳原子的排列方式不同7. 向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。下列液体X和固体Y的组合,正确的是( )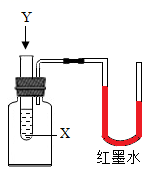 A、X是水,Y是氧化钙 B、X是水,Y是氢氧化钠 C、X是水,Y是硝酸铵 D、X是水,Y是氯化钠8. 把一定量甲、乙、丙、丁四种物质放入一个密闭容器中,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
A、X是水,Y是氧化钙 B、X是水,Y是氢氧化钠 C、X是水,Y是硝酸铵 D、X是水,Y是氯化钠8. 把一定量甲、乙、丙、丁四种物质放入一个密闭容器中,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )物质
甲
乙
丙
丁
反应前质量/g
10
5
12
16
反应后质量/g
8
5
30
x
A、反应中甲和丙的质量比为1:8 B、x=0 C、该反应是分解反应 D、乙一定是该反应的催化剂9. 将一定量的锌粉加入到硝酸镁和硝酸铜的混合液中,充分反应后过滤,得到滤渣和滤液。下列判断正确的是( )A、若滤液为蓝色,则滤渣中一定有锌、镁、铜 B、若向滤渣中加入稀盐酸有气泡产生,则滤液中一定有硝酸镁、硝酸锌、硝酸铜 C、若向滤液中加入氢氧化钠溶液,则一定有氢氧化铜生成 D、滤渣中一定含有铜,滤液中一定含有硝酸镁和硝酸锌10. 除去下列物质中的少量杂质,所用操作方法正确的是( )选项
物质(括号内为杂质)
操作方法
A
氯化钾(二氧化锰)
加水溶解、过滤、烘干
B
碳酸钙(氧化钙)
高温煅烧
C
二氧化碳(一氧化碳)
通过灼热的氧化铜粉末
D
氢气(水蒸气)
将混合气体通入稀硫酸
A、A B、B C、C D、D二、填空题
-
11. 请用化学用语填空:(1)、3个氢离子。(2)、生理盐水中的溶质。(3)、标出二氧化碳中碳元素的化合价。12. 2020年中国水周的主题是“坚持节水优先,建设幸福河湖”。(1)、向某自来水样品中加入一定量的肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该自来水属于(填“硬水”或“软水”)。(2)、生活中常用的方法降低水的硬度。(3)、用洗剂清洗餐具上的油污,利用了洗涤剂对油污的作用。(4)、珍惜水资源是每个公民应尽的责任和义务。下列做法有利于保护水资源的是(填字母序号)。
A实验室的废液经处理达标后排放
B洗净试管后,忘记关闭水龙头
C在实验室中安装节水的水龙头
13. 如图是氯元素在元素周期表中的信息以及四种粒子的结构示意图。请根据图回答下列问题: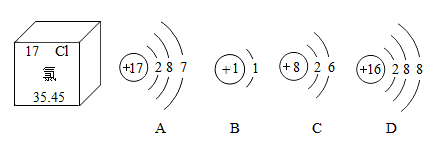 (1)、氯元素的相对原子质量是。(2)、A-D中具有相对稳定结构的粒子是(填字母序号)。(3)、为了缓解二氧化碳过多引起的温室效应加剧,我国科学研究人员成功研制出一种纳米纤维催化剂,将二氧化碳转化为液体燃料甲醇(CH3OH),其反应的微观示意图如下,请写出该反应的化学方程式。
(1)、氯元素的相对原子质量是。(2)、A-D中具有相对稳定结构的粒子是(填字母序号)。(3)、为了缓解二氧化碳过多引起的温室效应加剧,我国科学研究人员成功研制出一种纳米纤维催化剂,将二氧化碳转化为液体燃料甲醇(CH3OH),其反应的微观示意图如下,请写出该反应的化学方程式。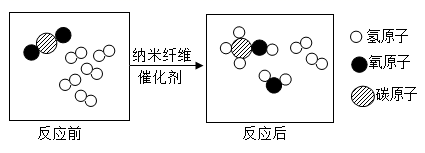 14. 如图是甲、乙、丙三种固体物质的溶解度曲线。请根据图回答下列问题:
14. 如图是甲、乙、丙三种固体物质的溶解度曲线。请根据图回答下列问题: (1)、在℃时,甲、丙两种物质的溶解度相等。(2)、若甲中混有少量的乙,提纯甲物质可采取的方法是。(3)、在t2℃时,配制180g甲物质的饱和溶液,需要甲物质的质量是g。(4)、t3℃时,将甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃,对所得溶液的叙述正确的是(填字母序号)。
(1)、在℃时,甲、丙两种物质的溶解度相等。(2)、若甲中混有少量的乙,提纯甲物质可采取的方法是。(3)、在t2℃时,配制180g甲物质的饱和溶液,需要甲物质的质量是g。(4)、t3℃时,将甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃,对所得溶液的叙述正确的是(填字母序号)。A溶质质量分数大小关系是:乙>甲>丙
B溶剂质量大小关系是:丙>乙>甲
C溶液质量大小关系是:丙>甲>乙
15. 妈妈为小鹏准备了一份午餐:米饭、红烧肉、糖醋鱼、咸鸭蛋、豆腐汤、酸奶。请回答下列问题:(1)、为保证各种营养素的均衡摄入,午餐中还应补充的营养素是。(2)、做红烧肉时,油锅起火,妈妈立即盖上锅盖。其灭火原理是。(3)、午饭后,小鹏感到胃不舒服,服用含氢氧化铝的药物中和过多的胃酸,症状有所缓解。写出该反应的化学方程式。(4)、废弃的酸奶袋等塑料垃圾会造成“白色污染”,请写出一条解决“白色污染”的措施。16. 金属材料在生活、生产中有广泛的应用。请回答下列问题:(1)、生活中用铁锅炒菜,主要利用了铁的性。(2)、工业上用赤铁矿(主要成分为氧化铁)炼铁,其反应原理是(用化学方程式表示)。(3)、2020年6月21日,时速600公里的高速磁悬浮试验样车成功试跑,制造样车外壳的主要材料是铝合金。铝合金与纯铝相比具有的优点是(写出一点即可)。(4)、金属资源有限,不能再生。写出防止铁生锈的一种方法。三、推断题
-
17. A-G是初中化学常见的七种物质,它们之间的关系如下图所示。图中“→”表示一种物质转化为另一种物质,“一”表示相连的两种物质能发生化学反应,部分反应物、生成物及反应条件已略去。其中A、B、C、D、E为不同类别的物质,B为铁锈的主要成分,G常用作食品干燥剂,D和E之间发生的反应是实验室制取二氧化碳的反应原理。请回答:
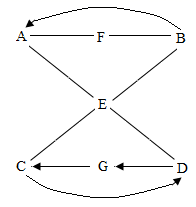 (1)、C的一种用途是。(2)、F所属的物质类别是(填“单质”、“氧化物”、“酸”、“碱”或“盐”)。(3)、G→C的基本反应类型是。(4)、A-E反应的实验现象是。(5)、B-E反应的化学方程式是。
(1)、C的一种用途是。(2)、F所属的物质类别是(填“单质”、“氧化物”、“酸”、“碱”或“盐”)。(3)、G→C的基本反应类型是。(4)、A-E反应的实验现象是。(5)、B-E反应的化学方程式是。四、实验题
-
18. 实验是进行科学探究的重要手段。根据下图回答问题:
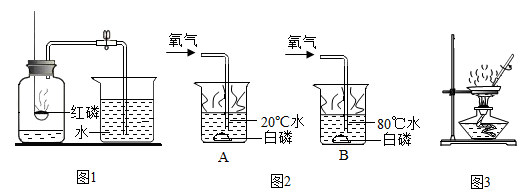 (1)、图1是测定空气中氧气含量的实验。由该实验得出关于空气中氧气含量的结论是。(2)、图2是探究燃烧条件的实验。A中白磷不燃烧,B中白磷燃烧,说明可燃物燃烧的条件之一是。(3)、图3是蒸发食盐水的实验。其中玻璃棒的作用是。19. 实验可以培养学生的化学核心素养。根据下图回答问题:
(1)、图1是测定空气中氧气含量的实验。由该实验得出关于空气中氧气含量的结论是。(2)、图2是探究燃烧条件的实验。A中白磷不燃烧,B中白磷燃烧,说明可燃物燃烧的条件之一是。(3)、图3是蒸发食盐水的实验。其中玻璃棒的作用是。19. 实验可以培养学生的化学核心素养。根据下图回答问题: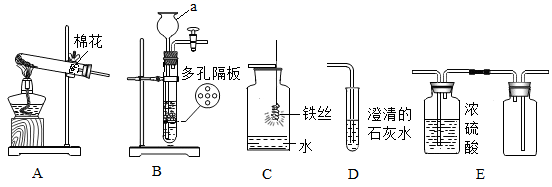 (1)、仪器a的名称是。(2)、若实验室制取氧气的发生装置选用A装置,反应的化学方程式为。用C装置进行氧气性质实验时,水的作用是。(3)、实验室制取二氧化碳应选择的发生装置是(填字母序号),将制得的二氧化碳通入到D装置中,发生反应的化学方程式为。(4)、若用E装置收集一瓶干燥的气体,则该气体可能是(填字母序号)。
(1)、仪器a的名称是。(2)、若实验室制取氧气的发生装置选用A装置,反应的化学方程式为。用C装置进行氧气性质实验时,水的作用是。(3)、实验室制取二氧化碳应选择的发生装置是(填字母序号),将制得的二氧化碳通入到D装置中,发生反应的化学方程式为。(4)、若用E装置收集一瓶干燥的气体,则该气体可能是(填字母序号)。A 、H2 B 、CO2 C、 O2
五、科学探究题
-
20. 有一包白色粉末,可能含有氢氧化钠、碳酸钠、氯化钙、碳酸钙中的一种几种。为了确定其成分,某兴趣小组进行了如下实验(微溶性物质按可溶处理)。
(查阅资料)氯化钡溶液呈中性。
(实验探究)
(1)、实验一:取一定量白色粉末放入烧杯中,加入足量水,搅拌,静置,观察到烧杯中有白色不溶物。由此小明得出白色粉末中一定含有碳酸钙。(讨论交流)有的同学对小明的结论提出了质疑,认为其结论不一定正确,理由是(用化学方程式表示)。
(2)、实验二:为进一步确定白色粉末成分,继续进行实验。实验步骤
实验现象
实验结论
步骤Ⅰ:取实验一中的上层清液少量于试管中,加入过量的氯化钡溶液,过滤
产生白色沉淀
白色粉末中一定含有
步骤Ⅱ:取步骤Ⅰ中的滤液少量于试管中,滴加酚酞溶液
白色粉末中一定含有氢氧化钠
(3)、(实验结论)综合以上探究,同学们通过讨论确定了白色粉末的组成,其可能的组成有种情况。(4)、(反思评价)a.步骤Ⅰ中加入过量的氯化钡溶液的目的是。
b.下列物质能替代步骤Ⅱ中酚酞溶液达到实验目的的是(填序号)。
①石蕊溶液
②氧化铜
③二氧化碳
④硫酸镁溶液
⑤稀盐酸
六、计算题
-
21. 取一定量的硫酸铵固体于烧杯中,加入100g氢氧化钠溶液,加热,恰好完全反应。反应后将溶液蒸干,得到7.1g固体。该反应的化学方程式为: 。请计算:(1)、生成氨气的质量。(2)、氢氧化钠溶液中溶质的质量分数。
-
-