吉林省2020年中考化学试卷
试卷更新日期:2020-08-17 类型:中考真卷
一、单选题
-
1. 制造五光十色的霓虹灯时,需要用到下列气体中的( )A、氮气 B、氧气 C、稀有气体 D、二氧化碳2. 在原子中,能决定元素种类的是( )A、电子层数 B、质子数 C、中子数 D、核外电子数3. 下列物质的用途中,主要利用其化学性质的是( )A、水银制温度计 B、石墨制铅笔芯 C、干冰作制冷剂 D、天然气作燃料4. 下列实验操作中,错误的是( )A、连接仪器
 B、铁丝燃烧
B、铁丝燃烧 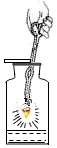 C、液体加热
C、液体加热 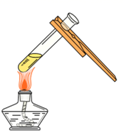 D、点燃酒精灯
D、点燃酒精灯 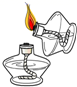 5. 生铁和钢都是铁的合金,它们都属于( )A、混合物 B、纯净物 C、单质 D、化合物6. 对下列现象解释正确的是( )A、汽油挥发——分子可分 B、花香四溢——分子不断运动 C、冰雪融化——分子很小 D、氧气液化——分子体积变小7. 下列关于“水”的说法中,错误的是( )A、生活污水应集中处理和排放 B、过滤操作能除去水中的所有杂质 C、可用肥皂水区分软水和硬水 D、活性炭可吸附水中有臭味的物质8. 下列与碳和碳的氧化物有关的说法中,正确的是( )A、煤炉上放一盆水可防止CO中毒 B、CO2能使紫色石蕊溶液变红,说明CO2显酸性 C、CO和CO2化学性质不同的原因是分子构成不同 D、用墨绘制的古画经久不变色,说明碳不与任何物质反应9. 下列实验数据分析合理的是( )A、向H2O2溶液中加入5gMnO2 , 充分反应后MnO2的质量仍为5g B、将5gNaCl溶解在100g水中,得到溶液中NaCl的质量分数为5% C、在“粗盐中难溶性杂质的去除”实验中,5g粗盐提纯后,可得到精盐5g D、使5gMg完全燃烧后,生成物的质量仍为5g10. 若利用碱的性质进行下列实验,不能达到相应目的的是( )A、分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液 B、分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体 C、分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液 D、分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
5. 生铁和钢都是铁的合金,它们都属于( )A、混合物 B、纯净物 C、单质 D、化合物6. 对下列现象解释正确的是( )A、汽油挥发——分子可分 B、花香四溢——分子不断运动 C、冰雪融化——分子很小 D、氧气液化——分子体积变小7. 下列关于“水”的说法中,错误的是( )A、生活污水应集中处理和排放 B、过滤操作能除去水中的所有杂质 C、可用肥皂水区分软水和硬水 D、活性炭可吸附水中有臭味的物质8. 下列与碳和碳的氧化物有关的说法中,正确的是( )A、煤炉上放一盆水可防止CO中毒 B、CO2能使紫色石蕊溶液变红,说明CO2显酸性 C、CO和CO2化学性质不同的原因是分子构成不同 D、用墨绘制的古画经久不变色,说明碳不与任何物质反应9. 下列实验数据分析合理的是( )A、向H2O2溶液中加入5gMnO2 , 充分反应后MnO2的质量仍为5g B、将5gNaCl溶解在100g水中,得到溶液中NaCl的质量分数为5% C、在“粗盐中难溶性杂质的去除”实验中,5g粗盐提纯后,可得到精盐5g D、使5gMg完全燃烧后,生成物的质量仍为5g10. 若利用碱的性质进行下列实验,不能达到相应目的的是( )A、分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液 B、分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体 C、分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液 D、分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体二、填空题
-
11. 根据如图,回答下列问题。
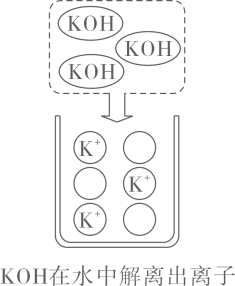 (1)、写出溶剂的化学式。(2)、写出图中阴离子的符号。(3)、KOH中氧元素的化合价为。12. 化学与人体健康有着密切联系。(1)、在“鸡蛋、西红柿、菜籽油”中,富含蛋白质的是。(2)、为预防骨质疏松、佝偻病,日常饮食中应摄入足量的元素为。(3)、“免洗消毒洗手液”的主要成分乙醇(C2H5OH)中共含有种元素。(4)、医用外科口罩的罩体材料多为聚丙烯,聚丙烯属于(填“合成材料”或“金属材料”)。13. 根据KNO3和NaCl的溶解度曲线,回答下列问题。
(1)、写出溶剂的化学式。(2)、写出图中阴离子的符号。(3)、KOH中氧元素的化合价为。12. 化学与人体健康有着密切联系。(1)、在“鸡蛋、西红柿、菜籽油”中,富含蛋白质的是。(2)、为预防骨质疏松、佝偻病,日常饮食中应摄入足量的元素为。(3)、“免洗消毒洗手液”的主要成分乙醇(C2H5OH)中共含有种元素。(4)、医用外科口罩的罩体材料多为聚丙烯,聚丙烯属于(填“合成材料”或“金属材料”)。13. 根据KNO3和NaCl的溶解度曲线,回答下列问题。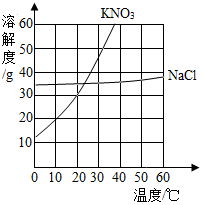 (1)、30℃时,KNO3和NaCl中溶解度较大的是。(2)、20℃时,使接近饱和的KNO3溶液变为该温度下的饱和溶液的方法之一是。(3)、为了使NaCl溶液中的溶质全部析出,应采用的方法是结晶。14. 根据工业制取氨气反应的微观示意图,回答下列问题。
(1)、30℃时,KNO3和NaCl中溶解度较大的是。(2)、20℃时,使接近饱和的KNO3溶液变为该温度下的饱和溶液的方法之一是。(3)、为了使NaCl溶液中的溶质全部析出,应采用的方法是结晶。14. 根据工业制取氨气反应的微观示意图,回答下列问题。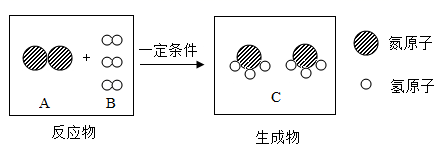 (1)、写出A物质的化学式。(2)、反应中B、C的分子个数比。(3)、该反应的基本反应类型是。15. 木炭是一种常见的燃料。(1)、在实验室中,用酒精灯点燃木炭,从燃烧条件分析,酒精灯的作用是。(2)、将机制木炭制成空心管状,可使其燃烧更加充分,原因是。16. 化学为5G助力。(1)、承载基站的铁塔表面涂漆,是为了隔绝和水,从而防止锈蚀。(2)、基站供电系统的导线多为铜线,使用铜是因为它具有延展性和。(3)、使用人造金刚石薄膜做基体材料,是未来芯片研究的发展方向,金刚石与石墨物理性质有明显差异的原因是。17. 学了酸的化学性质,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)、写出A物质的化学式。(2)、反应中B、C的分子个数比。(3)、该反应的基本反应类型是。15. 木炭是一种常见的燃料。(1)、在实验室中,用酒精灯点燃木炭,从燃烧条件分析,酒精灯的作用是。(2)、将机制木炭制成空心管状,可使其燃烧更加充分,原因是。16. 化学为5G助力。(1)、承载基站的铁塔表面涂漆,是为了隔绝和水,从而防止锈蚀。(2)、基站供电系统的导线多为铜线,使用铜是因为它具有延展性和。(3)、使用人造金刚石薄膜做基体材料,是未来芯片研究的发展方向,金刚石与石墨物理性质有明显差异的原因是。17. 学了酸的化学性质,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。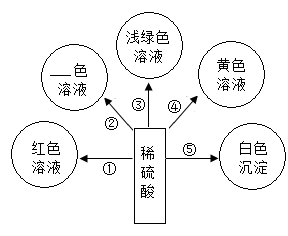 (1)、若用Cu(OH)2实现②,会得到色溶液。(2)、若想实现③,得到浅绿色溶液,可选用的单质是。(3)、若选用BaCl2溶液实现⑤,此反应的化学方程式为。
(1)、若用Cu(OH)2实现②,会得到色溶液。(2)、若想实现③,得到浅绿色溶液,可选用的单质是。(3)、若选用BaCl2溶液实现⑤,此反应的化学方程式为。三、实验题
-
18. 下图是在实验室里制取气体时的常用装置。
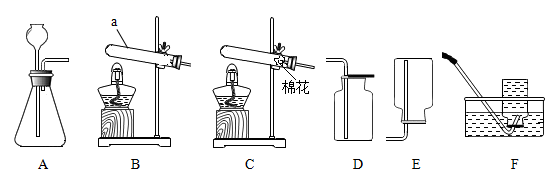 (1)、仪器a名称是。(2)、用加热KMnO4的方法制取O2 , 可以选用的发生装置是(填序号),反应的化学方程式为。(3)、用D装置收集CO2 , 验满的操作是。
(1)、仪器a名称是。(2)、用加热KMnO4的方法制取O2 , 可以选用的发生装置是(填序号),反应的化学方程式为。(3)、用D装置收集CO2 , 验满的操作是。四、科学探究题
-
19. 结合某校师生线上“互动探究”活动,回答有关问题。
(学习目标)了解生活中常见的几种盐的化学性质。
(实验用品)教师用品:NaCl溶液、Na2CO3溶液、酚酞溶液、CaCl2溶液、KNO3溶液等。
学生用品:洁厕灵(主要成分稀盐酸,不考虑其它成分)、Ca(OH)2溶液(用生石灰干燥剂制备)、纯碱(Na2CO3)溶液、小苏打(NaHCO3)溶液、注射器、废塑料瓶、吸管等。
(互动探究)
探究目的
探究过程
主要现象
解释或结论
探究一:盐溶液是否一定显中性
教师实验:
向分别盛有NaCl溶液、Na2CO3溶液的两支试管中滴加溶液
所加溶液遇NaCl溶液不变色,遇Na2CO3溶液变红色
盐溶液不一定显中性
探究二:Na2CO3溶液和NaHCO3溶液能否与某些
酸溶液反应
学生实验:
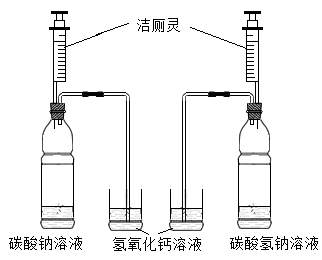
有产生,Ca(OH)2溶液变浑浊
Na2CO3溶液和NaHCO3溶液能与某些酸溶液反应
探究三:Na2CO3溶液能否与某些溶液反应
学生实验:
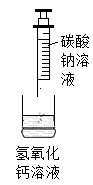
产生白色沉淀
写出化学方程式
探究四:Na2CO3溶液能否与某些盐溶液反应
教师实验:
⑴取少量KNO3溶液于试管中,向其中滴加Na2CO3溶液
⑵取少量CaCl2溶液于试管中,向其中滴加Na2CO3溶液
⑴无明显现象
⑵
Na2CO3溶液能与某些盐溶液反应
(拓展延伸)“垃圾是放错了位置的资源”,对下列物质的利用,正确的是。
A“探究一”中剩余溶液的混合液,可用于检验“探究二”中洁厕灵是否过量
B“探究二”中生成的这种气体,可以作为气体肥料
C“探究三”中生成的这种固体,可以作食品干燥剂
D“探究四”中剩余溶液的混合液,可以除去NaNO3溶液中混入的Ca(NO3)2
五、计算题
-
20. 北宋沈括编撰的《梦溪笔谈》中,记录了用CuSO4溶液熬制胆矾的铁釜,使用时间久了也可以化作铜。(1)、由上述材料分析,Fe比Cu的金属活动性(填“强”或“弱”)。(2)、如果向足量的CuSO4溶液中加入5.6gFe粉,充分反应后,理论上可以得到Cu的质量是多少?
-
-