高中化学人教版(新课标)选修4 第一章第二节 燃烧热 能源
试卷更新日期:2020-08-11 类型:同步测试
一、单选题
-
1. 下列物质中,属于可再生的能源是( )A、石油 B、氢气 C、天然气 D、煤2. 下列说法正确的是( )A、能源可分为一次能源和二次能源,电能、页岩气、煤、太阳能均为一次能源 B、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 C、向汽油中添加甲醇后,该混合燃料的热值发生改变 D、糖类、油脂和蛋白质都是天然有机高分子化合物3. 下列能源组合中,均属于新能源的一组是( )
①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能
A、①②③④ B、①⑤⑥⑦⑧ C、①③⑤⑥⑦⑧ D、③⑤⑥⑦⑧4. 下列燃烧反应的反应热是燃烧热的是:( )A、H2(g)+1/2 O2(g)=H2O(g) △H1 B、C(s)+1/2 O2(g)=CO(g) △H2 C、S(s)+O2(g)=SO2(g) △H3 D、H2S(g)+1/2O2=S(s)+H2O(l) △H45. 下列热化学方程式中的反应热表示燃烧热的是 ( )A、NH3(g) + O2(g) = NO(g) + H2O(g) ΔH=-a kJ·mol-1 B、C6H12O6(s) + 6O2(g) = 6CO2(g) + 6H2O(g) ΔH=-b kJ·mol-1 C、CO(g) + O2(g) = CO2(g) ΔH=-c kJ·mol-1 D、CH3CH2OH(l) + O2(g) = CH3CHO(l) + H2O(l) ΔH=-d kJ·mol-16. 下列对于太阳能、生物质能和氢能的利用的说法错误的是A、光伏电池可实现太阳能到电能的转化 B、将植物的秸秆、枝叶、杂草和人畜粪便加入沼气发酵池中,在富氧条件下,经过缓慢、复杂、充分的氧化反应最终生成沼气,从而有效利用生物质能 C、生活、生产中大量应用氢能源,要解决氢气的储存和运输等问题 D、垃圾焚烧处理厂把大量生活垃圾中的生物质能转化为热能、电能,减轻了垃圾给城市造成的压力,改善了城市的环境7. 下面均是正丁烷与氧气反应的热化学方程式(25℃、101kPa):
①C4H10(g)+ O2(g)═ 4CO2(g)+5H2O(l);△H=-2 878kJ/mol②C4H10(g)+ O2(g)═ 4CO2(g)+5H2O(g);△H=-2 658kJ/mol
③C4H10(g)+ O2(g)═ 4CO(g)+5H2O(l);△H=-1 746kJ/mol
④C4H10(g)+ O2(g)═ 4CO(g)+5H2O(g);△H=-1 526kJ/mol
由此判断,正丁烷的燃烧热为( )
A、2878kJ/mol B、2658kJ/mol C、1746kJ/mol D、1526kj/mol8. 下列说法错误的是( )A、化学反应过程中一定伴随着能量的变化,遵循能量守恒定律 B、氢气热值高,利用化石燃料燃烧放出的热量分解水产生氢气,是氢能开发的方向 C、101kPa下,S(s)+O2(g)=SO2(g)的反应热可以表示S(s)的标准燃烧热 D、稀的强酸和强碱反应只生成1molH2O(1)的反应热为中和热9. 下列关于热化学反应的描述中正确的是( )A、HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3) kJ/mol B、碳与二氧化碳的反应既是吸热反应,又是化合反应. C、热化学方程式中化学计量数可表示分子个数 D、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热二、综合题
-
10. 在新能源中,氢能将会成为21世纪最理想的能源,但现阶段氢气的主要用于合成氨工业;已知101kPa、25℃时,1mol下列物质完全燃烧生成稳定状态化合物时放出的热量数据如表:
物质
氢气
原煤
(主要成分是C)
汽油
(主要成分C8H18)
热量(kJ)
285.8
250.9
4910
(1)、H2燃烧的热化学方程式是 .(2)、工业上电解饱和盐水的副产物之一是H2 , 反应的离子方程式是 .11. 当前能源危机是一个全球性问题,开源节流是应对能源危机的重要举措。(1)、下列做法不利于能源“开源节流”的是________(填字母)。A、开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 B、研究采煤、采油新技术,提高产量以满足工业生产的快速发展 C、大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 D、减少资源消耗、增加资源的重复使用和资源的循环再生 (2)、金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,(填 “金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH=。(3)、N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为。(4)、综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:。12. 根据下列两个热化学方程式,回答下列问题:
(2)、金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,(填 “金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH=。(3)、N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为。(4)、综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:。12. 根据下列两个热化学方程式,回答下列问题:2H2(g)+O2(g)= 2H2O(1) ΔH=−571.6 kJ · mol−1
C3H8(g)+5O2(g)= 3CO2(g)+4H2O(l) ΔH=−2 220 kJ · mol−1
(1)、H2的燃烧热为 , C3H8的燃烧热为。(2)、1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为。(3)、现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3 847 kJ,则在混合气体中H2和C3H8的体积比是。13. 生物质资源是一种污染小的可再生能源。生物质的主要转化途径及主要产物如图所示。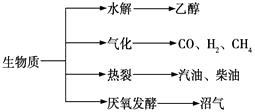 (1)、下列有关生物质能的说法正确的是。
(1)、下列有关生物质能的说法正确的是。a.生物质能本质上来源于太阳能
b.纤维素水解获得的产物中含有丰富的生物质能
c.生物质“热裂”获得的汽油、柴油等属于纯净物
d.将杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,可作家庭燃气
(2)、由生物质能可获得CO和H2。等物质的量的CO与H2反应时,其原子利用率可达100%,则该反应合成的物质可能是。a.汽油 b.甲醇(CH4O) c.甲醛(CH2O) d.乙酸(C2H4O2)