浙江省衢州市2019-2020学年高二下学期化学期末考试试卷
试卷更新日期:2020-08-07 类型:期末考试
一、选择题
-
1. 下列属于共价化合物的是( )A、Na2O2 B、H2SO4 C、NH4Cl D、Cl22. 下列仪器名称为“坩埚”的是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列物质属于电解质且能导电的是( )A、熔融氯化钾 B、金属铜 C、氢氧化钠溶液 D、酒精4. 黑火药的反应原理为:2KNO3+S+3C=K2S+N2↑+3CO2↑,该反应中还原剂是( )A、KNO3和S B、C C、K2S D、N25. 下列物质的名称不正确的是( )A、Na2CO3:小苏打 B、CaSO4·2H2O:生石膏 C、CH3CH2CH(CH3)CH2CH2CH3:3一甲基己烷 D、HCHO:甲醛6. 下列表示不正确的是( )A、O2-离子结构示意图:
3. 下列物质属于电解质且能导电的是( )A、熔融氯化钾 B、金属铜 C、氢氧化钠溶液 D、酒精4. 黑火药的反应原理为:2KNO3+S+3C=K2S+N2↑+3CO2↑,该反应中还原剂是( )A、KNO3和S B、C C、K2S D、N25. 下列物质的名称不正确的是( )A、Na2CO3:小苏打 B、CaSO4·2H2O:生石膏 C、CH3CH2CH(CH3)CH2CH2CH3:3一甲基己烷 D、HCHO:甲醛6. 下列表示不正确的是( )A、O2-离子结构示意图: B、CH4的球棍模型:
B、CH4的球棍模型:  C、CCl4的电子式:
C、CCl4的电子式:  D、乙烯的结构简式:CH2=CH2
7. 下列说法不正确的是( )A、乙酸和油酸(C17H33COOH) 互为同系物 B、35Cl和37Cl互为同位素 C、CH3CH2OH和CH3OCH3互为同分异构体 D、O2和O3互为同素异形体8. 下列叙述不正确的是( )A、二氧化硫可用于漂白纸浆 B、可利用二氧化碳制造全降解塑料 C、碳酸氢钠可用于中和胃酸过多 D、食品消毒、防腐常使用福尔马林9. 下列说法不正确的是( )A、可用电解氯化镁溶液制取金属镁 B、可用钠制得钛、钽、铌等金属 C、可用铝热反应制备金属Mn D、可用NH3还原CuO制备金属Cu10. 下列说法不正确的是( )A、厨余垃圾中蕴藏着丰富的生物质能 B、煤的气化、液化、干馏都是物理变化 C、利用蓝绿藻等低等植物和微生物在阳光作用下可使水分解产生氢气 D、熔喷布以聚丙烯为主要原料,制造聚丙烯的原料主要来自于石油的裂解11. 下列有关实验说法,不正确的是( )A、可用HNO3、AgNO3溶液鉴别NaCl溶液和NaNO2溶液 B、焰色反应时,先用稀硫酸清洗铂丝井在酒精灯火焰上灼烧,再进行实验 C、纸层析法时,亲脂性强的成分在流动相中分配的多一些,随流动相移动速度就快些 D、用镊子夹取金属钠固体,切割取用后剩余的钠放回原试剂瓶中12. 下列关于氮及其化合物说法,不正确的是( )A、氮气性质稳定,可用于工业制镁的冷却剂 B、N2H4可用作航天飞机的燃料 C、碳酸氢铵常用作氮肥,不可与碱性肥料混用 D、硝酸可用于制造染料、炸药等13. 不能正确表示下列变化的离子方程式是( )A、氧化镁与盐酸反应:MgO+2H+=Mg2++H2O B、氯气和水反应:Cl2+H2O=2H++Cl-+ClO- C、将过量CO2通入NaAlO2溶液中:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- D、氯化铵水解:NH4++H2O NH3·H2O+H+14. 下列说法不正确的是( )A、75%酒精、紫外光等可使蛋白质变性 B、用酸性KMnO4溶液可鉴别苯和甲苯 C、乙酸乙酯中混有的乙酸,可加入足量的NaOH溶液,经分液除去 D、将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,上层析出高级脂肪盐15. 某有机物的结构如图所示,下列关于该有机物的描述不正确的是( )
D、乙烯的结构简式:CH2=CH2
7. 下列说法不正确的是( )A、乙酸和油酸(C17H33COOH) 互为同系物 B、35Cl和37Cl互为同位素 C、CH3CH2OH和CH3OCH3互为同分异构体 D、O2和O3互为同素异形体8. 下列叙述不正确的是( )A、二氧化硫可用于漂白纸浆 B、可利用二氧化碳制造全降解塑料 C、碳酸氢钠可用于中和胃酸过多 D、食品消毒、防腐常使用福尔马林9. 下列说法不正确的是( )A、可用电解氯化镁溶液制取金属镁 B、可用钠制得钛、钽、铌等金属 C、可用铝热反应制备金属Mn D、可用NH3还原CuO制备金属Cu10. 下列说法不正确的是( )A、厨余垃圾中蕴藏着丰富的生物质能 B、煤的气化、液化、干馏都是物理变化 C、利用蓝绿藻等低等植物和微生物在阳光作用下可使水分解产生氢气 D、熔喷布以聚丙烯为主要原料,制造聚丙烯的原料主要来自于石油的裂解11. 下列有关实验说法,不正确的是( )A、可用HNO3、AgNO3溶液鉴别NaCl溶液和NaNO2溶液 B、焰色反应时,先用稀硫酸清洗铂丝井在酒精灯火焰上灼烧,再进行实验 C、纸层析法时,亲脂性强的成分在流动相中分配的多一些,随流动相移动速度就快些 D、用镊子夹取金属钠固体,切割取用后剩余的钠放回原试剂瓶中12. 下列关于氮及其化合物说法,不正确的是( )A、氮气性质稳定,可用于工业制镁的冷却剂 B、N2H4可用作航天飞机的燃料 C、碳酸氢铵常用作氮肥,不可与碱性肥料混用 D、硝酸可用于制造染料、炸药等13. 不能正确表示下列变化的离子方程式是( )A、氧化镁与盐酸反应:MgO+2H+=Mg2++H2O B、氯气和水反应:Cl2+H2O=2H++Cl-+ClO- C、将过量CO2通入NaAlO2溶液中:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- D、氯化铵水解:NH4++H2O NH3·H2O+H+14. 下列说法不正确的是( )A、75%酒精、紫外光等可使蛋白质变性 B、用酸性KMnO4溶液可鉴别苯和甲苯 C、乙酸乙酯中混有的乙酸,可加入足量的NaOH溶液,经分液除去 D、将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,上层析出高级脂肪盐15. 某有机物的结构如图所示,下列关于该有机物的描述不正确的是( ) A、含有4种官能团 B、能发生取代、加成、消去、酯化等反应 C、一定条件下1mol该物质最多可与1molH2发生加成反应 D、该有机物属于芳香族化合物16. 下列说法正确的是( )A、氧的非金属性比碳强,所以H2O的熔沸点比CH4高 B、ⅦA族的F和Cl都能形成+7价的稳定化合物 C、同主族元素,原子序数越大,元素的金属性越强 D、同周期元素,随着原子序数增大,原子半径越大17. 下列说法正确的是( )A、pH为6.8的溶液一定呈酸性 B、中和pH和体积均相等的醋酸和盐酸溶液,所需NaOH的物质的量相同 C、0.1mol·L-1的醋酸溶液加水稀释,溶液中所有离子的浓度都减小 D、0.1mol·L-1的氨水溶液中:c(NH4+) +c(NH3·H2O) =0.1mol·L-118. 欧洲足球锦标赛事中的拍摄车,装着“绿色心脏”一质子交换膜燃料电池,其工作原理如图所示。下列叙述中正确的是( )
A、含有4种官能团 B、能发生取代、加成、消去、酯化等反应 C、一定条件下1mol该物质最多可与1molH2发生加成反应 D、该有机物属于芳香族化合物16. 下列说法正确的是( )A、氧的非金属性比碳强,所以H2O的熔沸点比CH4高 B、ⅦA族的F和Cl都能形成+7价的稳定化合物 C、同主族元素,原子序数越大,元素的金属性越强 D、同周期元素,随着原子序数增大,原子半径越大17. 下列说法正确的是( )A、pH为6.8的溶液一定呈酸性 B、中和pH和体积均相等的醋酸和盐酸溶液,所需NaOH的物质的量相同 C、0.1mol·L-1的醋酸溶液加水稀释,溶液中所有离子的浓度都减小 D、0.1mol·L-1的氨水溶液中:c(NH4+) +c(NH3·H2O) =0.1mol·L-118. 欧洲足球锦标赛事中的拍摄车,装着“绿色心脏”一质子交换膜燃料电池,其工作原理如图所示。下列叙述中正确的是( ) A、装置中的能量变化为电能转化为化学能 B、通入氢气的电极发生氧化反应 C、通入空气的电极反应式:O2+4e-+2H2O=4OH- D、装置中电子从通入空气的电极经过导线流向通入氢气的电极19. H2S催化分解过程中通入CO2、CH4会发生如下反应,下列说法不正确的是( )A、CH4(g)+CO2(g) 2H2(g)+2CO(g),压缩容器体积,平衡转化率将增大 B、H2S(g) +CO2(g) H2O(g)+COS(g),通入CO2 , 将促进反应的进行 C、已知2H2S(g)+CH4(g) 4H2(g)+CS2(g) △H>0,则该反应在高温下易自发 D、2H2S(g) 2H2(g)+S(g) △H>020. 设NA为阿伏加德罗常数的数值。下列说法正确的是( )A、2molSO2和1mol O2混合在催化剂作用下充分反应生成SO3的分子数为2NA B、2Fe2++2H++3H2O2=2Fe3++O2↑+4H2O,则每生成1mol O2 , 该反应转移电子数为4NA C、25℃时,pH=3的醋酸溶液1L,溶液中含H+的数目小于0.001NA D、标准状况下,22.4L苯中C-H数目为6NA21. 600℃时,在2L的恒容密闭容器中充入一定量的CO和H2O,发生反应:
A、装置中的能量变化为电能转化为化学能 B、通入氢气的电极发生氧化反应 C、通入空气的电极反应式:O2+4e-+2H2O=4OH- D、装置中电子从通入空气的电极经过导线流向通入氢气的电极19. H2S催化分解过程中通入CO2、CH4会发生如下反应,下列说法不正确的是( )A、CH4(g)+CO2(g) 2H2(g)+2CO(g),压缩容器体积,平衡转化率将增大 B、H2S(g) +CO2(g) H2O(g)+COS(g),通入CO2 , 将促进反应的进行 C、已知2H2S(g)+CH4(g) 4H2(g)+CS2(g) △H>0,则该反应在高温下易自发 D、2H2S(g) 2H2(g)+S(g) △H>020. 设NA为阿伏加德罗常数的数值。下列说法正确的是( )A、2molSO2和1mol O2混合在催化剂作用下充分反应生成SO3的分子数为2NA B、2Fe2++2H++3H2O2=2Fe3++O2↑+4H2O,则每生成1mol O2 , 该反应转移电子数为4NA C、25℃时,pH=3的醋酸溶液1L,溶液中含H+的数目小于0.001NA D、标准状况下,22.4L苯中C-H数目为6NA21. 600℃时,在2L的恒容密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g),反应过程中的部分数据如下表所示:
n/mol
t/min
n(CO)
n(H2O)
0
1.20
0.60
10
0.80
20
0.20
下列说法正确的是( )
A、0~10min用CO表示的平均反应速率为0.04mol·L-1·min-1 B、该反应在10min后才达到平衡 C、CO的平衡转化率为66.7% D、温度升高至800℃时,反应平衡常数为0.64,则正反应为放热反应22. 乙烯与水加成制备乙醇的能量变化过程如下图所示。下列说法不正确的是( ) A、H2SO4是该合成过程的催化剂 B、合成过程的速率由反应②决定 C、保持温度不变缩小容器的体积,乙烯的转化率减小 D、C2H4(g)+H2SO4(1) =C2H5OSO3H(1) △H=(E1-E2) kJ·mol-123. 25℃时,将0.1mol·L-1的HCl溶液逐滴滴入10.00mL 0.1mol·L-1的NH3·H2O溶液中,其AG值变化的曲线如图所示。已知AG=lg ,下列分析不正确的是( )
A、H2SO4是该合成过程的催化剂 B、合成过程的速率由反应②决定 C、保持温度不变缩小容器的体积,乙烯的转化率减小 D、C2H4(g)+H2SO4(1) =C2H5OSO3H(1) △H=(E1-E2) kJ·mol-123. 25℃时,将0.1mol·L-1的HCl溶液逐滴滴入10.00mL 0.1mol·L-1的NH3·H2O溶液中,其AG值变化的曲线如图所示。已知AG=lg ,下列分析不正确的是( )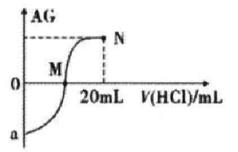 A、滴定前HCl溶液的AG=12 B、M点时溶液中c(Cl-)>c(NH4+) C、从M点到N点水的电离程度先增大后减小 D、N点溶液中:c(Cl-)=2c(NH3·H2O)+2c(NH4+)24. 白色固体Na2S2O4常用于织物的漂白,也能将污水中的某些重金属离子还原为单质除去。隔绝空气加热Na2S2O4固体完全分解得到固体产物Na2SO3、Na2S2O3 , 和SO2。下列关于Na2S2O4的说法不正确的是( )A、可以使品红溶液褪色 B、其溶液可以作吸氧剂 C、在空气中加热Na2S2O4固体可得到固体产物Na2SO4 D、Na2S2O4不能与强酸反应生成盐25. 白色固体混合物A, 含有KNO3、CaCO3、Na2CO3、Na2SiO3、CuSO4中的几种,常温常压下进行如下实验。下列推断不正确的是( )
A、滴定前HCl溶液的AG=12 B、M点时溶液中c(Cl-)>c(NH4+) C、从M点到N点水的电离程度先增大后减小 D、N点溶液中:c(Cl-)=2c(NH3·H2O)+2c(NH4+)24. 白色固体Na2S2O4常用于织物的漂白,也能将污水中的某些重金属离子还原为单质除去。隔绝空气加热Na2S2O4固体完全分解得到固体产物Na2SO3、Na2S2O3 , 和SO2。下列关于Na2S2O4的说法不正确的是( )A、可以使品红溶液褪色 B、其溶液可以作吸氧剂 C、在空气中加热Na2S2O4固体可得到固体产物Na2SO4 D、Na2S2O4不能与强酸反应生成盐25. 白色固体混合物A, 含有KNO3、CaCO3、Na2CO3、Na2SiO3、CuSO4中的几种,常温常压下进行如下实验。下列推断不正确的是( ) A、混合物A中一定有Na2SiO3、CuSO4 B、白色固体F的主要成分是H2SiO3 C、无色溶液B的pH<7 D、溶液B进行焰色反应,透过蓝色钴玻璃观察火焰呈紫色,说明A中有KNO3
A、混合物A中一定有Na2SiO3、CuSO4 B、白色固体F的主要成分是H2SiO3 C、无色溶液B的pH<7 D、溶液B进行焰色反应,透过蓝色钴玻璃观察火焰呈紫色,说明A中有KNO3二、非选择题(本题有6小题,共50分)
-
26.(1)、比较元素非金属性的相对强弱:ClS(填“>”、“<”或“=”):用一个化学方程式说明Cl2和S氧化性的相对强弱。(2)、离子化合物MgO2可用于治疗消化道疾病,各原子均满足8电子稳定结构。写出MgO2的电子式。(3)、CO2和SiO2均是IVA族元素氧化物,CO2常温为气态,SiO2为高熔点固体。请分析原因。27. 将wg镁和铝的混合物投入25mL4mol·L-1盐酸中,固体全部溶解后,得到标准状况下896mL气体(不考虑金属和盐酸反应时HCl的挥发)。向所得溶液中加入20mLNaOH溶液时,生成沉淀的质量达到最大。(1)、NaOH溶液的物质的量浓度为mol·L-1。(2)、沉淀的质量达到最大时为g(用含w的表达式表示)。28.(1)、I.化合物A由两种元素组成,两元素质量比为3:16,按如下流程进行试验:

产物B、C的物质的量之比为1:1,D、E均为气体,D能使湿润的红色石蕊试纸变蓝,E中含有18个电子,回答下列问题:
写出B的化学式。
(2)、C加到FeCl3溶液反应的离子方程式。(3)、A与足量氨水反应的化学方程式。(4)、Ⅱ.某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行试验(夹持仪器已略去),实验表明浓硝酸能将NO氧化成NO2 , 而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
实验时先检验装置的气密性,加入药品,打开弹簧夹后通入CO2一段时间,关闭弹簧夹,打开分液漏斗旋塞滴加浓硝酸。
①装置②中发生反应的化学方程式为。
②该小组得出的结论依据的实验现象是。
29. 研究含氮化合物具有重要意义。(1)、固体碳酸铵在恒温恒容的密闭容器中达到分解平衡:(NH4)2CO3(s) 2NH3(g)+CO2(g)+H2O(g)
①下列可以作为反应达到平衡的判据是(填选项字母)。
A.2v正(CO2)=V逆(NH3)
B.密闭容器中混合气体的平均摩尔质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中二氧化碳的体积分数不变
②该反应在室温就能自发地分解产生氨气,下列说法正确的是 (填选项字母)。
A.该反应△S>0
B.平衡后,其它条件不变,增加少量(NH4)2CO3固体的量,NH3浓度增大
C.放热反应在常温下一定容易进行
D.化学平衡常数K值很大,则该反应的速率一定很快
(2)、在不同温度下,反应N2(g)+O2(g) 2NO(g)的平衡常数K如下表:温度/℃
1538
1760
2404
平衡常数K
0.86×10-4
2.6×10-4
64×10-4
①该反应的△H0(填“>”“=”或“<”)
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图甲所示,请在图甲中补充画出1760℃时N2的转化率随时间变化曲线 。

③某种用TiO2作催化剂处理汽车尾气NO的方法为:
2H2O(g)+4NO(g)+O2(g) 4HNO3(g),在O2浓度几乎不变的条件下,模拟NO的降解,反应一段时间后检测到混合气体中N2浓度明显上升而硝酸气体浓度有所降低,请用化学方程式结合化学反应原理知识解释出现该现象可能的原因。
30. 某兴趣小组用废旧镀锌铁皮按下列流程制备七水合硫酸锌(ZnSO4·7H2O) 和磁性Fe3O4胶体粒子。 (1)、步骤①中可用于判断镀锌层完全反应的实验现象是。处理废旧锌铁皮也可以用NaOH溶解锌层,该反应的化学方程式为。(2)、步骤②,某同学采用不同降温方式进行冷却结晶,测得ZnSO4·7H2O晶体颗粒大小分布如图所示。根据该实验结果,为了得到颗粒大小相对均一的较大晶粒,宜选择 方式进行冷却结晶。
(1)、步骤①中可用于判断镀锌层完全反应的实验现象是。处理废旧锌铁皮也可以用NaOH溶解锌层,该反应的化学方程式为。(2)、步骤②,某同学采用不同降温方式进行冷却结晶,测得ZnSO4·7H2O晶体颗粒大小分布如图所示。根据该实验结果,为了得到颗粒大小相对均一的较大晶粒,宜选择 方式进行冷却结晶。 A、快速降温 B、缓慢降温 C、变速降温(3)、下列说法正确的是( )A、步骤①可用普通过滤法分离固体和液体,所用到玻璃仪器有分液漏斗、烧杯。 B、步骤④中H2O2的用量需要控制,用量不足或过量时,都会使产品不纯 C、步骤⑤中可用减压过滤得到Fe3O4胶体粒子 D、Fe3O4胶体粒子制备过程中可持续通入N2 , 防止Fe2+被氧化。(4)、用高锰酸钾法(一种氧化还原滴定法)可测定产物中Fe3O4的含量,称取mg产品溶解在稀硫酸中配成250mL溶液,取出25mL用浓度为0.01000mol·L-1的KMnO4标准溶液滴定,滴定终点时消耗KMnO4标准溶液VmL,
A、快速降温 B、缓慢降温 C、变速降温(3)、下列说法正确的是( )A、步骤①可用普通过滤法分离固体和液体,所用到玻璃仪器有分液漏斗、烧杯。 B、步骤④中H2O2的用量需要控制,用量不足或过量时,都会使产品不纯 C、步骤⑤中可用减压过滤得到Fe3O4胶体粒子 D、Fe3O4胶体粒子制备过程中可持续通入N2 , 防止Fe2+被氧化。(4)、用高锰酸钾法(一种氧化还原滴定法)可测定产物中Fe3O4的含量,称取mg产品溶解在稀硫酸中配成250mL溶液,取出25mL用浓度为0.01000mol·L-1的KMnO4标准溶液滴定,滴定终点时消耗KMnO4标准溶液VmL,已知:MnO4-+5Fe2++8H+=Mn2++5Fe+4H2O
①产品中Fe3O4的质量分数为(用含m、V的式子表示)
②滴定操作中,如果滴定前装有KMnO4标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将。
③测定过程中使用到移液管,选出其正确操作并按序列出字母:蒸馏水洗涤→待转移溶液润洗→( ) →()→()→()→洗净,放回管架。
a.放液完毕,停留数秒,取出移液管
b.移液管尖与锥形瓶内壁接触,松开食指放液
c.洗耳球吸溶液至移液管标线以上,食指堵住管口
d.放液至凹液面最低处与移液管标线相切,按紧管口
31. 2020年2月,国家卫生健康委办公厅、国家中医药管理局办公室联合发出《关于印发新型冠状病毒肺炎诊疗方案(试行第六版)的通知》,此次诊疗方案抗病毒治疗增加了阿比多尔这个药物。其中间体I的合成路线如下:
请回答:
(1)、下列说法正确的是 。A、③⑦的反应类型分别为还原反应、加成反应 B、化合物E中含氧官能团名称为酯基 C、化合物B具有酸性 D、中间体Ⅰ的分子式是C20H20NO4SBr(2)、写出化合物A的结构简式。(3)、写出B→C的化学方程式。(4)、写出化合物D同时符合下列条件的同分异构体的结构简式。①含有-NO2
②含有苯环
③核磁共振氢谱(1H-NMR)检测表明:分子中共有3种氢原子
(5)、已知:①当苯环有RCOO-、烃基时,新导入的基团进入原有基团的邻位或对位:原有基团为-COOH时, 新导入的基团进入原有基团的间位。②苯酚、苯胺(C6H5NH2) 易氧化。设计以 到
到  的合成路线(用流程图表示,无机试任选)。
的合成路线(用流程图表示,无机试任选)。