浙江省衢州市2019-2020学年高一下学期化学期末考试试卷
试卷更新日期:2020-08-07 类型:期末考试
一、选择题
-
1. 氯气的分子式是( )A、O2 B、Cl2 C、N2 D、H2O2. 用于新冠肺炎疫情环境消毒用的“84消毒液”的主要成分是次氯酸钠(NaClO),按物质的组成和性质进行分类,次氯酸钠属于( )A、氧化物 B、酸 C、碱 D、盐3. 下列仪器名称为分液漏斗的是( )A、
 B、
B、 C、
C、 D、
D、 4. 下列物质中,不能与金属钠反应的是( )A、氧气 B、水 C、盐酸 D、煤油5. 下列分散系能产生“丁达尔效应”的是( )A、氯化钠溶液 B、硫酸铜溶液 C、氢氧化铁胶体 D、蔗糖溶液6. 反应Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O中,氧化剂是( )A、Cu B、浓H2SO4 C、CuSO4 D、SO27. 下列属于弱电解质的是( )A、酒精 B、醋酸 C、铝 D、硫酸钡8. 下列表示不正确的是( )A、CH4的比例模型
4. 下列物质中,不能与金属钠反应的是( )A、氧气 B、水 C、盐酸 D、煤油5. 下列分散系能产生“丁达尔效应”的是( )A、氯化钠溶液 B、硫酸铜溶液 C、氢氧化铁胶体 D、蔗糖溶液6. 反应Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O中,氧化剂是( )A、Cu B、浓H2SO4 C、CuSO4 D、SO27. 下列属于弱电解质的是( )A、酒精 B、醋酸 C、铝 D、硫酸钡8. 下列表示不正确的是( )A、CH4的比例模型 B、CO2的电子式
B、CO2的电子式  C、乙醇的官能团-OH
D、Cl-的结构示意图
C、乙醇的官能团-OH
D、Cl-的结构示意图  9. 下列说法不正确的是( )A、2H和3H互为同位素 B、O2和O3互为同素异形体 C、CH3CH2OH和CH3OCH3互为同分异构体 D、C2H2和C6H6互为同系物10. 下列说法正确的是( )A、工业上常用电解NaCl溶液制备金属钠 B、在医疗上碳酸钠是治疗胃酸过多的一种药剂 C、过量的铁在氯气中燃烧可生成氯化亚铁 D、金属镁燃烧时发出耀眼的白光,因此常用来制造信号弹和焰火11. 有A,B,C,D四种短周期元素,其在周期表中位置如图所示,A2+与C原子的电子数相差2。下列推断不正确的是( )
9. 下列说法不正确的是( )A、2H和3H互为同位素 B、O2和O3互为同素异形体 C、CH3CH2OH和CH3OCH3互为同分异构体 D、C2H2和C6H6互为同系物10. 下列说法正确的是( )A、工业上常用电解NaCl溶液制备金属钠 B、在医疗上碳酸钠是治疗胃酸过多的一种药剂 C、过量的铁在氯气中燃烧可生成氯化亚铁 D、金属镁燃烧时发出耀眼的白光,因此常用来制造信号弹和焰火11. 有A,B,C,D四种短周期元素,其在周期表中位置如图所示,A2+与C原子的电子数相差2。下列推断不正确的是( )……
C
A
B
……
D
A、A和D组成的化合物是弱电解质且水溶液呈酸性 B、与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应中可作催化剂 C、离子半径:C>A>B D、D的最高价氧化物对应水化物为强酸12. 下列方程式不正确的是( )A、次氯酸的电离方程式:HClO H++ClO- B、盐酸与小苏打溶液反应的离子方程式:H++HCO3-=CO2↑+H2O C、工业制备粗硅的化学方程式:SiO2+C Si+CO2↑ D、苯和浓硝酸反应的化学方程式: +HO-NO2
+HO-NO2  -NO2+H2O
13. 下列实验操作或方法中,合理的是( )A、用铂丝蘸取某溶液置于酒精灯火焰上灼烧,直接观察火焰颜色,检验K+的存在 B、用玻璃棒蘸取Na2CO3溶液,滴在湿润的pH试纸上,测定该溶液的pH C、浓硫酸不慎沾到皮肤上,立即用大量的NaOH溶液冲洗 D、试管可用酒精灯直接加热,也可用水浴加热14. 下列说法正确的是( )A、汽油、煤油、柴油均可来自于石油的分馏 B、煤的液化与气化都是物理变化 C、乙烯和苯均能使酸性高锰酸钾溶液褪色 D、乙炔和苯均能使溴水褪色且原理相同15. 有机物与我们的生产生活密切相关,下列说法不正确的是( )A、葡萄糖可以发生氧化反应、银镜反应和水解反应 B、工业上利用油脂在碱性条件下的水解反应制取肥皂 C、食用植物油的主要成分是高级不饱和脂肪酸甘油酯 D、在一定条件下,蛋白质水解的最终产物是氨基酸16. 为了研究碳酸钙与稀盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况(0~t1、t1~t2、t2~t3各时间段相同),绘制出如图所示的曲线。下列说法不正确的是( )
-NO2+H2O
13. 下列实验操作或方法中,合理的是( )A、用铂丝蘸取某溶液置于酒精灯火焰上灼烧,直接观察火焰颜色,检验K+的存在 B、用玻璃棒蘸取Na2CO3溶液,滴在湿润的pH试纸上,测定该溶液的pH C、浓硫酸不慎沾到皮肤上,立即用大量的NaOH溶液冲洗 D、试管可用酒精灯直接加热,也可用水浴加热14. 下列说法正确的是( )A、汽油、煤油、柴油均可来自于石油的分馏 B、煤的液化与气化都是物理变化 C、乙烯和苯均能使酸性高锰酸钾溶液褪色 D、乙炔和苯均能使溴水褪色且原理相同15. 有机物与我们的生产生活密切相关,下列说法不正确的是( )A、葡萄糖可以发生氧化反应、银镜反应和水解反应 B、工业上利用油脂在碱性条件下的水解反应制取肥皂 C、食用植物油的主要成分是高级不饱和脂肪酸甘油酯 D、在一定条件下,蛋白质水解的最终产物是氨基酸16. 为了研究碳酸钙与稀盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况(0~t1、t1~t2、t2~t3各时间段相同),绘制出如图所示的曲线。下列说法不正确的是( ) A、反应速率最大的是0~t1段,生成气体最多的是t3~t4段 B、t1~t2段曲线变化的可能是盐酸与大理石反应放热导致的 C、t2~t3时间段里影响反应速率的主要外界因素是浓度 D、为了减缓反应速率可向盐酸中加入NaCl溶液17. 如图为某种甲醇燃料电池示意图。下列判断正确的是( )
A、反应速率最大的是0~t1段,生成气体最多的是t3~t4段 B、t1~t2段曲线变化的可能是盐酸与大理石反应放热导致的 C、t2~t3时间段里影响反应速率的主要外界因素是浓度 D、为了减缓反应速率可向盐酸中加入NaCl溶液17. 如图为某种甲醇燃料电池示意图。下列判断正确的是( ) A、电极A反应式:CH3OH-6e-+H2O=CO2+6H- B、B电极为负极 C、B电极附近溶液pH增大 D、电池工作时,溶液中电子由电极B流向电极A18. 下列说法不正确的是( )A、室温下测得0.1mol·L-1的一元酸HA溶液pH=3.0,则HA一定为弱电解质 B、室温下将0.1mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11.0 C、室温下NaClO溶液中有:c(H+)+c(Na+)=c(OH-) +c(ClO-) D、室温下0.1mol·L-1的HA溶液与0.1mol·L-1的NaOH溶液等体积混合,所得溶液pH一定等于7.019. 下列说法正确的是( )A、碘晶体受热变成蒸汽,吸收的热量用于克服碘原子间的作用力 B、金刚石、富勒烯、干冰都是由共价键形成的原子晶体 C、HCl溶于水后,化学键被破坏,形成水合离子 D、CH4、PCl3分子中各原子均达到8电子稳定结构20. 已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据能量变化示意图,下列说法不正确的是( )
A、电极A反应式:CH3OH-6e-+H2O=CO2+6H- B、B电极为负极 C、B电极附近溶液pH增大 D、电池工作时,溶液中电子由电极B流向电极A18. 下列说法不正确的是( )A、室温下测得0.1mol·L-1的一元酸HA溶液pH=3.0,则HA一定为弱电解质 B、室温下将0.1mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11.0 C、室温下NaClO溶液中有:c(H+)+c(Na+)=c(OH-) +c(ClO-) D、室温下0.1mol·L-1的HA溶液与0.1mol·L-1的NaOH溶液等体积混合,所得溶液pH一定等于7.019. 下列说法正确的是( )A、碘晶体受热变成蒸汽,吸收的热量用于克服碘原子间的作用力 B、金刚石、富勒烯、干冰都是由共价键形成的原子晶体 C、HCl溶于水后,化学键被破坏,形成水合离子 D、CH4、PCl3分子中各原子均达到8电子稳定结构20. 已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据能量变化示意图,下列说法不正确的是( ) A、①、②的数值分别为1370、1852 B、拆开H2O(g) 中的1molH-O键吸收463kJ的能量 C、2H2(g)+O2(g) =2H2O(g) △H=-482kJmol-1 D、已知H2O(I)=H2O(g) △H>0,说明1molH2O(l) 的能量比1molH2O(g) 高21. 用NA表示阿伏加德罗常数的值。下列说法正确的是( )A、0.1mol重水(D2O) 分子中含有的中子数为NA B、10g质量分数为46%的C2H5OH水溶液中含有的氧原子数目为0.1NA C、标准状况下,2.24L己烷中含有的共价键数目为1.9NA D、过氧化氢分解制得标准状况下2.24LO2 , 转移电子数目为0.4NA22. 已知X(g)+3Y(g) 2W(g)+M(s) △H=-a kJ·mol-1(a>0),一定温度下,在容积为1L密闭容器中,加入1molX(g) 与1molY(g),2s后Y的物质的量浓度为0.4mol·L-1 , 下列说法正确的是( )A、X体积分数保持不变,说明反应已经达到平衡状态 B、若减小Y的浓度,则正反应速率减小,逆反应速率增大 C、0~2s,W的平均反应速率为0.2mol·L-1·s-1 D、反应达到平衡状态时,W与M的物质的量浓度比为2:123. 下列有关实验装置(夹持和尾气处理装置已省略)进行的相应实验,不能达到实验目的的是( )
A、①、②的数值分别为1370、1852 B、拆开H2O(g) 中的1molH-O键吸收463kJ的能量 C、2H2(g)+O2(g) =2H2O(g) △H=-482kJmol-1 D、已知H2O(I)=H2O(g) △H>0,说明1molH2O(l) 的能量比1molH2O(g) 高21. 用NA表示阿伏加德罗常数的值。下列说法正确的是( )A、0.1mol重水(D2O) 分子中含有的中子数为NA B、10g质量分数为46%的C2H5OH水溶液中含有的氧原子数目为0.1NA C、标准状况下,2.24L己烷中含有的共价键数目为1.9NA D、过氧化氢分解制得标准状况下2.24LO2 , 转移电子数目为0.4NA22. 已知X(g)+3Y(g) 2W(g)+M(s) △H=-a kJ·mol-1(a>0),一定温度下,在容积为1L密闭容器中,加入1molX(g) 与1molY(g),2s后Y的物质的量浓度为0.4mol·L-1 , 下列说法正确的是( )A、X体积分数保持不变,说明反应已经达到平衡状态 B、若减小Y的浓度,则正反应速率减小,逆反应速率增大 C、0~2s,W的平均反应速率为0.2mol·L-1·s-1 D、反应达到平衡状态时,W与M的物质的量浓度比为2:123. 下列有关实验装置(夹持和尾气处理装置已省略)进行的相应实验,不能达到实验目的的是( )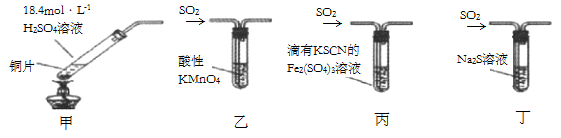 A、若将甲中上层清液倒入水中,观察到溶液呈蓝色,说明有CuSO4生成 B、图乙装置中溶液的颜色变浅,说明SO2具有漂白性 C、图丙装置中溶液的颜色变浅,说明SO2具有还原性 D、图丁装置中产生淡黄色沉淀,说明SO2或H2SO4具有氧化性24. 有3.2gCuO、Fe2O3混合物跟足量CO充分反应后固体减少了0.72g,反应后全部气体用50mL 0.7mol·LBa(OH)2溶液吸收。下列有关叙述中正确的是( )A、反应中生成的CO2体积为1.008L B、吸收CO2后的溶液中一定不含Ba(HCO3)2 C、原混合物中CuO与Fe2O3质量比为3:1 D、若将质量相同的混合物加过量硫酸溶解后,再加入100mLNaOH溶液时沉淀达最大量,由此可求得c(NaOH)=0.75mol·L-125. 某固体粉末X中可能含有K2SO4、(NH4)2CO3、K2SO3、Cu2O、FeO、Fe2O3中几种,为确定其组成,某同学进行如下实验:
A、若将甲中上层清液倒入水中,观察到溶液呈蓝色,说明有CuSO4生成 B、图乙装置中溶液的颜色变浅,说明SO2具有漂白性 C、图丙装置中溶液的颜色变浅,说明SO2具有还原性 D、图丁装置中产生淡黄色沉淀,说明SO2或H2SO4具有氧化性24. 有3.2gCuO、Fe2O3混合物跟足量CO充分反应后固体减少了0.72g,反应后全部气体用50mL 0.7mol·LBa(OH)2溶液吸收。下列有关叙述中正确的是( )A、反应中生成的CO2体积为1.008L B、吸收CO2后的溶液中一定不含Ba(HCO3)2 C、原混合物中CuO与Fe2O3质量比为3:1 D、若将质量相同的混合物加过量硫酸溶解后,再加入100mLNaOH溶液时沉淀达最大量,由此可求得c(NaOH)=0.75mol·L-125. 某固体粉末X中可能含有K2SO4、(NH4)2CO3、K2SO3、Cu2O、FeO、Fe2O3中几种,为确定其组成,某同学进行如下实验:
已知:Cu2O+2H+=Cu2++Cu+H2O
根据实验过程及现象,下列说法正确的是( )
A、无色气体A可用湿润的蓝色石蕊试纸检验 B、固体X中一定含有(NH4)2CO3、K2SO4、FeO C、无色气体E一定含有CO2 , 一定不含SO2 D、固体X中可能含有Cu2O、Fe2O3二、非选择题(共5小题,共50分。)
-
26. 按要求作答。(1)、①写出MgO的名称;
②写出乙炔的结构式。
(2)、写出NaHCO3受热分解的化学方程式。(3)、写出Cl2与NaOH溶液反应的离子方程式 。(4)、海带中提取碘的过程中,将I-氧化生成I2时,若加入过量的氯水,则Cl2将I2氧化生成HIO3 , 同时还有一种强酸生成,写出该反应的化学方程式。27. 以淀粉为原料,经过一系列反应可以制得酯F(C5H8O4)。B结构中有甲基,1molB可以与2molNa和1molNaOH反应。
请回答:
(1)、E中官能团名称是。(2)、C→D的反应类型是。(3)、D→E的化学反应方程式是。(4)、F的结构简式是。(5)、下列说法不正确的是 。A、由A生成C时可以产生一种无色无味气体 B、可以用新制Cu(OH)2悬浊液鉴别C,D,E(必要时可以加热) C、相同物质的量的B,D耗氧量相同 D、1molF与足量钠反应,消耗钠2mol(6)、检验淀粉在酸性条件下水解产物A(C6H12O6)的操作是。28. 无机盐X(仅含两种元素)可通过单质甲与Ca(OH)2浊夜共热的方法来制备,某同学为探究X的组成和性质,设计了如下实验(流程图中部分产物已略去)。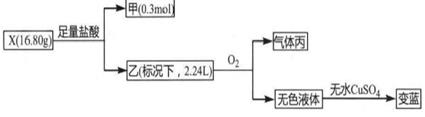
已知:气体乙在标况下的密度为1.52g·L-1 , 气体丙无色、有刺激性气味,能使品红溶液褪色。
(1)、X的化学式为 , 乙的电子式为。(2)、X与足量盐酸反应的化学方程式为 。(3)、在澄清石灰水中通入过量气体丙反应的离子方程式为。29. 实验室制乙酸乙酯的主要装置如图中A所示,主要步骤:①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2mL产物时停止加热。撤下b试管并用力振荡,然后静置待其中液体分层;
⑤分离出纯净的乙酸乙酯。

请回答下列问题:
(1)、步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:。(2)、A装置中使用球形管除起到冷凝作用外,另一重要作用;步骤⑤中分离乙酸乙酯必须使用的一种仪器是。(3)、为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图A所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min,实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:实验编号
试管a中试剂
试管b中试剂
测得有机层的厚度/cm
A
3mL乙醇、2mL乙酸、ImL18mol·L-1浓硫酸
饱和Na2CO3溶液
5.0
B
3mL乙醇、2mL乙酸
0.1
C
3mL乙醇、2mL乙酸、6mL.3mol·LH2SO4
1.2
D
3mL乙醇、2mL乙酸、盐酸
1.2
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入6mL浓度为 mol·L-1盐酸。
②分析对比实验(填实验编号)的数据,可推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
③为充分利用反应物,该同学又设计了图中甲、乙两个装置(利用乙装置时,待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。
你认为更合理的是。理由是:。
30. 在120℃、1.01×105Pa时,将1L丙烷与若干升O2混合点燃充分燃烧后,恢复至原温度、压强,测得气体体积为aL,通过碱石灰后气体体积变为bL。(1)、若a-b=7,则bL气体中一定含有。(2)、若a-b=5,则混合前O2体积为 , 点燃前混合气体的平均摩尔质量为。