黑龙江省大庆市2020年中考化学试卷
试卷更新日期:2020-08-06 类型:中考真卷
一、单选题
-
1. 化学就在我们身边,人类的衣、食、住、行都离不开化学,下列叙述错误的是( )A、制衣服用的棉花、羊毛、蚕丝等属于合成纤维 B、为了人类的生存和发展,人类必须爱惜并保护水资源 C、粉刷墙壁用的乳胶漆的主要原料﹣﹣乳液是乳浊液 D、氢氧燃料电池可用作汽车的驱动电源2. 下列变化属于物理变化的是( )A、钢铁生锈 B、红磷转化为白磷 C、活性炭净水 D、葡萄酿酒3. 下列图示实验操作正确的是( )A、
 稀释浓硫酸
B、
稀释浓硫酸
B、 夹持蒸发皿
C、
夹持蒸发皿
C、 量筒体积读数
D、
量筒体积读数
D、 O2验满
4. 运用分类法学习和研究化学物质,能够收到事半功倍的效果,下列分类正确的是( )
O2验满
4. 运用分类法学习和研究化学物质,能够收到事半功倍的效果,下列分类正确的是( )类别/选项
混合物
单质
氧化物
碱
盐
A
黄铜
C60
Na2O2
Cu2(OH)2CO3
明矾
B
过磷酸钙
Hg
干冰
KOH
纯碱
C
空气
煤
Fe3O4
Ca(OH)2
碳铵
D
福尔马林
Ne
SiO2
NH3•H2O
HBr
A、A B、B C、C D、D5. 下列化学方程式与事实相符且正确的是( )A、甲烷在空气中完全燃烧: B、用含氢氧化铝的药物治疗胃酸过多:2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O C、三氧化硫与氢氧化钠溶液的反应:SO3+2NaOH═Na2SO4+H2O D、赤铁矿溶于盐酸:Fe2O3+2HCl═FeCl3+H2O6. 下列表述错误的是( )A、带电的原子是离子 B、在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变 C、实验室中常将固体药品配成溶液进行化学反应,以提高反应速率 D、纤维素作为六大基本营养素可以被人体消化吸收7. 除去下列物质中的少量杂质,所选试剂和操作方法都正确的是( )选项
物质
杂质
除杂试剂或操作方法
A
Cu(NO3)2溶液
AgNO3
加过量铁粉,过滤
B
氨气
水蒸气
通过足量的氢氧化钠固体干燥
C
KCl固体
KClO3
加少量二氧化锰,加热
D
NH4HCO3固体
NaCl
加热
A、A B、B C、C D、D8. 如图所示的图象能正确反映对应变化关系的是( )A、 向一定浓度的NaOH溶液中加水稀释
B、
向一定浓度的NaOH溶液中加水稀释
B、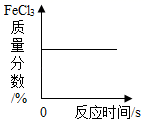 FeCl3催化H2O2溶液的分解
C、
FeCl3催化H2O2溶液的分解
C、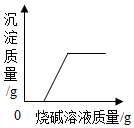 向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
D、
向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
D、 等质量的铁、锌分别与等质量分数的足量稀硫酸反应
9. A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
等质量的铁、锌分别与等质量分数的足量稀硫酸反应
9. A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )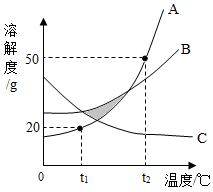 A、阴影区域中,A,C均处于不饱和状态 B、除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯B C、将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>B D、t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%10. 碘元素被称为“智力元素”,是人体必需的微量元素之一,人体缺碘会引起甲状腺肿大,幼儿缺碘会造成思维迟钝,影响生长发育。因此,人们常通过摄入海产品或食用加碘盐来补充碘元素,以保证人体健康。利用海带提取碘单质(I2)的工艺流程如图所示,下列说法错误的是( )
A、阴影区域中,A,C均处于不饱和状态 B、除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯B C、将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>B D、t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%10. 碘元素被称为“智力元素”,是人体必需的微量元素之一,人体缺碘会引起甲状腺肿大,幼儿缺碘会造成思维迟钝,影响生长发育。因此,人们常通过摄入海产品或食用加碘盐来补充碘元素,以保证人体健康。利用海带提取碘单质(I2)的工艺流程如图所示,下列说法错误的是( ) A、操作①中,所需要的玻璃仪器有3种 B、由于淀粉有遇碘(I2)变蓝的特性,因此可以利用淀粉检验加入H2O2溶液后所得的“溶液一”中是否有单质碘生成 C、在上述过程中碘元素的化合价没有发生变化 D、在蒸馏操作中,蒸馏烧瓶内加入沸石的目的是为了防止液体的暴沸
A、操作①中,所需要的玻璃仪器有3种 B、由于淀粉有遇碘(I2)变蓝的特性,因此可以利用淀粉检验加入H2O2溶液后所得的“溶液一”中是否有单质碘生成 C、在上述过程中碘元素的化合价没有发生变化 D、在蒸馏操作中,蒸馏烧瓶内加入沸石的目的是为了防止液体的暴沸二、填空题
-
11.(1)、在电解水的实验中,产生的H2和O2的体积比约为。(2)、硫在空气里燃烧发出色火焰。(3)、画出铝离子的结构示意图。(4)、由于氮气的化学性质不活泼,因此常用作。(5)、日常生活中肥皂水遇(填“硬水”或“软水”)泡沫少、易起浮渣。12. 新型冠状病毒肺炎威胁着人们的身体健康,预防病毒除了戴口罩、勤洗手,还要做好消毒工作。请按要求填空:(1)、口罩成为每个人的生活必需品,医用口罩生产中采用环氧乙烷灭菌消毒。环氧乙烷的化学式为C2H4O,环氧乙烷由种元素组成,一个环氧乙烷分子中的电子总数为个,氧原子在化学反应中易(填“得到”或“失去”)电子,形成相对稳定结构。(2)、生活中我们使用医用酒精进行消毒。医用酒精中乙醇的分数为75%(填“质量”或“体积”)。(3)、如图是酒精完全燃烧的微观示意图。

①已知:“
 ”的相对原子质量是“”的
”的相对原子质量是“”的  n倍,该反应中“
n倍,该反应中“  ”和“
”和“  ”的质量比是(用含n的式子表示)。
”的质量比是(用含n的式子表示)。②酒精易挥发且易燃,使用医用酒精消毒时要注意。
三、实验题
-
13. 根据如图装置,回答问题:
 (1)、写出图中标号仪器的名称:①。(2)、用装置A分解一种暗紫色的固体制取氧气,试管内的固体应为(填化学式)。(3)、实验室利用C装置制备CO2气体的化学方程式。(4)、从实验安全角度考虑,(填“能”或“不能”)利用D装置制备和收集满H2。(5)、装置E通氧气前白磷不燃烧,通氧气后白磷燃烧,由此得出燃烧的条件之一是。14. 在实验室中常用二氧化锰和浓盐酸共热制取氯气,反应的化学方程式为:
(1)、写出图中标号仪器的名称:①。(2)、用装置A分解一种暗紫色的固体制取氧气,试管内的固体应为(填化学式)。(3)、实验室利用C装置制备CO2气体的化学方程式。(4)、从实验安全角度考虑,(填“能”或“不能”)利用D装置制备和收集满H2。(5)、装置E通氧气前白磷不燃烧,通氧气后白磷燃烧,由此得出燃烧的条件之一是。14. 在实验室中常用二氧化锰和浓盐酸共热制取氯气,反应的化学方程式为:请回答下列问题:
(1)、Ⅰ.Cl2的制备
根据实验室制备Cl2的反应原理,图一中应选用的发生装置是(填字母)。
 (2)、为获得纯净的氯气,可利用装置D除去Cl2中混有的;装置E中浓硫酸的作用是。若将浓硫酸滴到白纸上,现象是。(3)、图二的装置用于收集Cl2 , 则气体应从图三中的(填“a”或“b”)进入。
(2)、为获得纯净的氯气,可利用装置D除去Cl2中混有的;装置E中浓硫酸的作用是。若将浓硫酸滴到白纸上,现象是。(3)、图二的装置用于收集Cl2 , 则气体应从图三中的(填“a”或“b”)进入。 (4)、多余的Cl2通入NaOH溶液中进行尾气吸收,请配平相应的化学方程式:NaOH+Cl2═NaCl+NaClO+H2O(5)、Ⅱ.Cl2的性质及用途
(4)、多余的Cl2通入NaOH溶液中进行尾气吸收,请配平相应的化学方程式:NaOH+Cl2═NaCl+NaClO+H2O(5)、Ⅱ.Cl2的性质及用途根据金属活动性顺序,可用活动性强的金属把活动性弱的金属从它的盐溶液中置换出来;同理非金属单质间也存在相似的规律。已知,非金属单质活动性强弱关系如下:Cl2>I2>S.试写出将Cl2通入Na2S溶液中的化学方程式。
(6)、Cl2可用于生产“84”消毒液(有效成分为NaClO)和盐酸。①NaClO中氯元素的化合价是。
②喷洒“84”消毒液后,室内充满刺激性气味,主要体现分子的性质是。
A、分子可再分
B、分子在不停地运动
C、分子间有间隔
③工业上常用氢气和氯气反应制盐酸,在实验室我们测定稀盐酸pH,最简便的方法是使用 , 测定的操作是。
四、流程题
-
15. 以黄铁矿(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:
 (1)、将黄铁矿粉碎,目的是。(2)、沸腾炉中发生反应的化学方程式是。(3)、若硫酸厂产生的废气未经处理就排放到空气中,可能形成酸兩,我们把pH<的降雨称为酸雨。(4)、炉渣Fe2O3可回收冶炼成铁,生活中防止铁生锈的常见方法(答出一条即可)。
(1)、将黄铁矿粉碎,目的是。(2)、沸腾炉中发生反应的化学方程式是。(3)、若硫酸厂产生的废气未经处理就排放到空气中,可能形成酸兩,我们把pH<的降雨称为酸雨。(4)、炉渣Fe2O3可回收冶炼成铁,生活中防止铁生锈的常见方法(答出一条即可)。五、推断题
-
16. A~J是初中化学常见的物质,它们的相互转化关系如图所示。其中B是生活中最常见的液体,D物质俗称苏打,E是天然大理石的主要成分,G为最轻气体单质。

请回答下列问题:
(1)、A的化学式为 , A与B反应热量(填“放出”或“吸收”)。(2)、反应①的化学方程式该反应属于(填基本反应类型)。(3)、若I为紫红色固体单质,通过对反应②的分析。体现出G物质具有性。六、科学探究题
-
17. 某白色固体可能由BaCl2、NaOH、Na2CO3、Na2SO4、Fe3O4中的一种或几种物质组成。同学们为了确定该白色固体的成分,进行了如下实验探究:
(资料卡片)BaCl2溶液显中性。
(初步结论)
(1)、甲同学根据固体的描述确定样品中肯定没有(填化学式),原因是。(2)、(初步探究)同学们设计的实验过程及现象如图所示。

(交流讨论)
同学们认为:无色溶液M中一定含有(填化学式),无色溶液M加入酚酞试液后变红色,说明溶液M显碱性,需对溶液M继续探究。
(3)、(提出问题)使溶液M显碱性的物质是什么?
(猜想与假设)
猜想一:是氢氧化钠;猜想二:是碳酸钠;猜想三:……。
请将猜想三补充完整:。
(4)、(探究与结论)乙同学取无色溶液M于试管中,加入过量的氯化钡溶液,振荡,静置,观察到 , 证明无色溶液M中含有碳酸钠,此过程发生反应的化学方程式为。
(5)、丙同学为进一步证明无色溶液M中的成分,取乙同学实验所得上层清液少许于试管中,加入 , 观察到 , 证明猜想三成立。综合分析,乙同学加入过量氯化钡溶液的作用:①证明无色溶液M中含有碳酸钠,②。(6)、(实验结论)原白色固体中一定有的物质是(填化学式)。
七、计算题
-
18. 将20.0g NaOH、Ca(OH)2、NaCl组成的固体混合物溶于水配成溶液,向混合液中缓慢通入CO2气体(气体的溶解忽略不计),生成沉淀的质量与通入CO2气体的质量关系如图所示,请根据题意回答问题:
已知:Na2CO3+CO2+H2O═2NaHCO3
NaHCO3+NaOH═Na2CO3+H2O
(1)、经分析,A点溶液中所含溶质为(填化学式)。(2)、在B点时,溶液里碳元素均存在于NaHCO3中,若B点后继续通入足量的CO2气体,请将图象补充完整。(3)、该混合物中NaCl的质量分数为多少?(写出计算过程,计算结果精确至0.1%)
-
-
-