浙教版科学八下第2章微粒的模型与符号第1—3节综合训练
试卷更新日期:2016-05-18 类型:同步测试
一、选择题(每题2分,共30分)
-
1. 下列选项属于模型的是( )A、H2O B、表示方向的指向标 C、电流Ⅰ D、沙盘中的校园2. 下列物质中含有氧分子的是( )A、二氧化锰 B、氧化镁 C、氧化铜 D、液氧3. 下列关于钠原子和钠离子的说法中,正确的是( )A、它们的核外电子数相同 B、它们的性质完全相同 C、钠原子的质量比钠离子大的多 D、它们的质子数和中子数都相同4.
提起压在容器中水面上方的活塞,容器中的水发生汽化,如下图所示:下图中最能表示水汽化后在相同空间内粒子分布的是( )
 A、
A、 B、
B、 C、
C、 D、
D、 5. 正在生产中的国产大型客机C919部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性。铝锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )A、元素符号不同 B、原子质量不同 C、质子数不同 D、电子数不同6. 化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,则1735Cl和1737Cl( )A、属于同种元素 B、原子核内质子数不同 C、原子中核外电子数不同 D、原子中含有相同数目的中子7. 关于原子、分子、离子的说法中,错误的是( )A、原子不能直接构成物质 B、分子可以保持物质的化学性质 C、原子的质量主要集中在原子核上 D、金属原子失去电子会形成阳离子8. 下列实验能证明分子在化学反应中可分的是( )A、水通过直流电生成氢气和氧气 B、冷却热的饱和硫酸铜溶液时有晶体析出 C、烧碱能吸收空气中的水分而潮解 D、一个氧分子是由两个氧原子构成的9. 固态碘、碘溶液和碘蒸气中都存在碘分子,馒头遇到固态碘、碘溶液和碘蒸气都能变蓝色这一实验现象说明( )A、分子始终在做无规则运动 B、分子之间存在空隙 C、分子之间存在引力和斥力 D、分子是保持物质化学性质的一种微粒10. 有①氮气,②碘,③金刚石,④水,⑤水银,⑥高锰酸钾,⑦氧气,⑧磷8种物质。其中由原子直接构成的是( )A、②③⑧ B、③⑤⑧ C、②⑤⑦ D、①④⑥11.
5. 正在生产中的国产大型客机C919部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性。铝锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )A、元素符号不同 B、原子质量不同 C、质子数不同 D、电子数不同6. 化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,则1735Cl和1737Cl( )A、属于同种元素 B、原子核内质子数不同 C、原子中核外电子数不同 D、原子中含有相同数目的中子7. 关于原子、分子、离子的说法中,错误的是( )A、原子不能直接构成物质 B、分子可以保持物质的化学性质 C、原子的质量主要集中在原子核上 D、金属原子失去电子会形成阳离子8. 下列实验能证明分子在化学反应中可分的是( )A、水通过直流电生成氢气和氧气 B、冷却热的饱和硫酸铜溶液时有晶体析出 C、烧碱能吸收空气中的水分而潮解 D、一个氧分子是由两个氧原子构成的9. 固态碘、碘溶液和碘蒸气中都存在碘分子,馒头遇到固态碘、碘溶液和碘蒸气都能变蓝色这一实验现象说明( )A、分子始终在做无规则运动 B、分子之间存在空隙 C、分子之间存在引力和斥力 D、分子是保持物质化学性质的一种微粒10. 有①氮气,②碘,③金刚石,④水,⑤水银,⑥高锰酸钾,⑦氧气,⑧磷8种物质。其中由原子直接构成的是( )A、②③⑧ B、③⑤⑧ C、②⑤⑦ D、①④⑥11.如图所示是水分子在一定条件下分解的示意图,从中获得的信息不正确的是( )
 A、一个水分子由两个氢原子和一个氧原子构成 B、水分解后生成氢气和氧气的分子数比为2∶1 C、水分解过程中,分子的种类不变 D、水分解过程中,原子的数目不变12.
A、一个水分子由两个氢原子和一个氧原子构成 B、水分解后生成氢气和氧气的分子数比为2∶1 C、水分解过程中,分子的种类不变 D、水分解过程中,原子的数目不变12.原子结构模型的建立,经过了几代科学家的艰辛努力,直到现在仍在探索中。其中,行星模型的提出标志着原子结构的现代模型的问世,如图2-3-2所示是锂原子结构的行星模型,图中原子核内有3个质子、4个中子。不能根据原子结构的行星模型得出的结论是( )
 A、原子始终在做无规则的运动 B、原子核的体积只占整个原子体积的很小部分 C、构成原子核的粒子之间存在一种互相吸引的力 D、原子呈电中性13. 钛和钛合金被认为是21世纪的重要金属材料,它们具有熔点高、密度小、抗腐蚀性能好等优良性能,因此被广泛用于火箭、航天飞机、船舶和化工等。已知钛原子的质子数为22,中子数为26,则钛原子的核外电子数为( )A、48 B、26 C、4 D、2214. C-12和C-14是碳元素的两种不同的原子,二者的不同点有( )
A、原子始终在做无规则的运动 B、原子核的体积只占整个原子体积的很小部分 C、构成原子核的粒子之间存在一种互相吸引的力 D、原子呈电中性13. 钛和钛合金被认为是21世纪的重要金属材料,它们具有熔点高、密度小、抗腐蚀性能好等优良性能,因此被广泛用于火箭、航天飞机、船舶和化工等。已知钛原子的质子数为22,中子数为26,则钛原子的核外电子数为( )A、48 B、26 C、4 D、2214. C-12和C-14是碳元素的两种不同的原子,二者的不同点有( )①原子中的电子数;②原子核内的中子数;③原子核内的质子数;④原子的质量。
A、①② B、③④ C、①③ D、②④15. 法国科学家发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似.有关该粒子的说法不正确的是( )A、不显电性 B、失去一个中子后显+1价 C、相当于一个氦原子的质量 D、周期表中没有该“元素”的位置二、填空题(每空1分,共30分)
-
16. 20世纪初科学家发现,原子的核式结构与太阳系十分相似。它的中心是原子核,原子核是由 和 组成的。17. 物质是由分子、原子、离子等微小粒子构成的,如:二氧化碳是由 构成,氯化钠是由 构成。分子是保持物质化学性质的最小粒子,水的化学性质是由 保持;在过氧化氢制取氧气的反应中的最小粒子是 。18. 铁是由 构成;水由 构成;二氧化碳分子由 构成;氧分子由 构成;氩气由 构成。19.
如图所示是液态水与气态水的状态模型。
 (1)、改变水的 , 可以使水在固态、液态、气态三种状态间相互转变;(2)、在这三种状态的变化中,水分子之间的发生了变化,构成水这种物质的分子(填“会”或“不会”)变成其他分子。20. 在分子、原子,质子,中子,电子,原子核这些粒子中:
(1)、改变水的 , 可以使水在固态、液态、气态三种状态间相互转变;(2)、在这三种状态的变化中,水分子之间的发生了变化,构成水这种物质的分子(填“会”或“不会”)变成其他分子。20. 在分子、原子,质子,中子,电子,原子核这些粒子中:
(1)不显电性的粒子有 ;
(2)带正电的粒子有 ;
(3)质量最小的粒子是 .21. 科学研究证实,物质是由微粒构成的,例如铁是由铁原子构成的。请你填写构成下列物质的具体微粒的名称。
(1)铅笔芯中的石墨是由构成的。
(2)用于人工降雨的干冰是由构成的。
(3)平时用于配制生理盐水的氯化钠固体是由构成的。
22. 下表微粒中,(以下均填字母编号)是阳离子的是;互为同位素的是;与是同种元素。组别
质子
中子
电子
A
14
14
14
B
26
30
24
C
26
30
26
D
14
16
14
三、实验探究题(每空2分,共16分)
-
23.
碘是一种由碘分子构成的非金属,某同学利用碘进行了如图所示的实验:①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝色;②再取少量的碘溶解在水中,用馒头去蘸取碘液,发现馒头也会变蓝色。则:
 (1)、取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头(填“会”或“不会”)变蓝色。(2)、把碘溶解在酒精中,可以得到消毒用的碘酒,用馒头去蘸取少量的碘酒,馒头(填“会”或“不会”)变蓝色。(3)、请用分子的观点来解释实验中的现象。。(4)、现在从市场上买来的食盐大多是加碘盐,用馒头蘸取少量的碘盐水,馒头却不变色,这说明,我们食用的碘盐中(填“存在”或“不存在”)碘分子。24.
(1)、取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头(填“会”或“不会”)变蓝色。(2)、把碘溶解在酒精中,可以得到消毒用的碘酒,用馒头去蘸取少量的碘酒,馒头(填“会”或“不会”)变蓝色。(3)、请用分子的观点来解释实验中的现象。。(4)、现在从市场上买来的食盐大多是加碘盐,用馒头蘸取少量的碘盐水,馒头却不变色,这说明,我们食用的碘盐中(填“存在”或“不存在”)碘分子。24.探究原子结构的奥秘。
【情景提供】 19世纪以前,人们一直以为原子是不可分的,直到1887年,汤姆生发现了带负电的电子后,才引起人们对原子结构模型的探索。
【提出问题】 电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?
【进行实验】 1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。
实验做法如图所示:
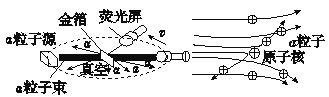
①放射源——放射性物质放出α粒子(带正电荷),质量是电子质量的7000倍;
②金箔——作为靶子,厚度1 μm,重叠了3000层左右的原子;
③荧光屏——α粒子打在上面发出闪光;
④显微镜——通过显微镜观察闪光,且通过360度转动可观察不同角度α粒子的到达情况。
【收集证据】 绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。
【猜想与假设】 α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)、若原子质量、正电荷在原子内均匀分布,则极少数α粒子就(填“会”或“不会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是。(2)、1 μm厚度的金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变,说明____;A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、科学家对原子结构的探究经历了三个过程,通过α粒子散射实验,你认为原子结构为下图中的________。A、 道尔顿模型特点:不可再分的实心球体
B、
道尔顿模型特点:不可再分的实心球体
B、 汤姆生模型特点:正负电荷均匀分布
C、
汤姆生模型特点:正负电荷均匀分布
C、 卢瑟福模型特点:核位于原子中心,重量集中在核上
卢瑟福模型特点:核位于原子中心,重量集中在核上
四、解答题(第25题每空1分,其他每空2分,共24分)
-
25.
如图所示是从空气中分离氧气的示意图:请你写出从图中所获得的有关物质组成、结构、性质、变化等信息各一条:

组成:;结构:;
性质:;变化:。
26.看图回答:
 (1)、过氧化氢分子中有种原子,甲醛分子中有个原子;(2)、比较氢分子(或氧分子)与水分子,可得出什么结论?。(3)、比较过氧化氢和水分子或乙炔分子与甲烷分子,可得出什么结论?。27.
(1)、过氧化氢分子中有种原子,甲醛分子中有个原子;(2)、比较氢分子(或氧分子)与水分子,可得出什么结论?。(3)、比较过氧化氢和水分子或乙炔分子与甲烷分子,可得出什么结论?。27.人类对原子结构的认识,经历了汤姆生、卢瑟福和玻尔等提出的模型的过程。
 (1)、卢瑟福核式结构模型是在α粒子轰击金箔实验的基础上提出的。上图中能正确反映他的实验结果的示意图是(选填序号)。(2)、从原子结构模型建立的过程中,我们发现________(选填序号)。A、科学模型的建立是一个不断完善、不断修正的过程 B、模型在科学研究中起着很重要的作用 C、玻尔的原子模型建立,使人们对原子结构的认识达到了完美的境界 D、人类借助模型的建立,对原子的认识逐渐接近本质28. 下表为几种常见元素原子的结构信息,请认真阅读分析后并回答:符号、质子数、中子数、核外电子数、相对原子质量;
(1)、卢瑟福核式结构模型是在α粒子轰击金箔实验的基础上提出的。上图中能正确反映他的实验结果的示意图是(选填序号)。(2)、从原子结构模型建立的过程中,我们发现________(选填序号)。A、科学模型的建立是一个不断完善、不断修正的过程 B、模型在科学研究中起着很重要的作用 C、玻尔的原子模型建立,使人们对原子结构的认识达到了完美的境界 D、人类借助模型的建立,对原子的认识逐渐接近本质28. 下表为几种常见元素原子的结构信息,请认真阅读分析后并回答:符号、质子数、中子数、核外电子数、相对原子质量;符号
质子数
中子数
核外电子数
相对原子质量
C
6
6
6
12
H
1
0
1
1
O
8
8
8
16
Na
11
12
11
23
Fe
26
30
26
56
(1)、构成原子的微粒有种,原子中一定含有的微粒是 ,(2)、你还能获得有关原子结构的其他信息吗?(写出两条即可)。①。
②。