福建省2020年中考化学试卷
试卷更新日期:2020-08-03 类型:中考真卷
一、单选题
-
1. 远古时期,半坡人从事的下列生活、生产活动中,一定有化学变化的是( )A、夯筑土屋 B、结绳记事 C、磨制石器 D、烧制彩陶2. 下列物质均可用于配制灭活新型冠状病毒的消毒剂,其中属于无机化合物的是( )A、过氧化氢(H2O2) B、乙醇(C2H6O) C、三氯甲烷(CHCl3) D、过氧乙酸(C2H4O3)3. 在制取氢气( )的实验中,下列操作正确的是( )A、检查气密性
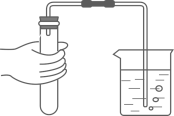 B、加入锌粒
B、加入锌粒 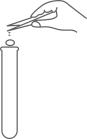 C、加入稀硫酸
C、加入稀硫酸  D、收集氢气
D、收集氢气  4. 下列食物中,蛋白质含量最高的是( )A、米饭 B、瘦肉 C、青菜 D、玉米油5. “加铁酱油”“高锌奶粉”“富硒茶叶”中,“铁、锌、硒”指的是( )A、单质 B、元素 C、金属 D、维生素6. 下列物质的性质与其用途不匹配的是( )A、石墨质软——用作电池的电极材料 B、不锈钢耐腐蚀——制造医疗器械 C、熟石灰显碱性——用来改良酸性土壤 D、干冰易升华——用于人工降雨7. 2020年6月23日,我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成北斗卫星导航系统的组网。该火箭第三级的推进剂为液氢和液氧组合,下列说法正确的是( )A、氢气液化过程中,氢分子之间的间隔保持不变 B、分离液态空气得到液氧的过程中,氧分子静止不动 C、液氧变成气态氧时,放出热量 D、氢气与氧气反应的本质是氢、氧原子的重新组合8. NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是( )
4. 下列食物中,蛋白质含量最高的是( )A、米饭 B、瘦肉 C、青菜 D、玉米油5. “加铁酱油”“高锌奶粉”“富硒茶叶”中,“铁、锌、硒”指的是( )A、单质 B、元素 C、金属 D、维生素6. 下列物质的性质与其用途不匹配的是( )A、石墨质软——用作电池的电极材料 B、不锈钢耐腐蚀——制造医疗器械 C、熟石灰显碱性——用来改良酸性土壤 D、干冰易升华——用于人工降雨7. 2020年6月23日,我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成北斗卫星导航系统的组网。该火箭第三级的推进剂为液氢和液氧组合,下列说法正确的是( )A、氢气液化过程中,氢分子之间的间隔保持不变 B、分离液态空气得到液氧的过程中,氧分子静止不动 C、液氧变成气态氧时,放出热量 D、氢气与氧气反应的本质是氢、氧原子的重新组合8. NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是( )温度/℃
0
20
40
60
NaCl的溶解度/g
35.7
36.0
36.6
37.3
KNO3的溶解度/g
13.3
31.6
63.9
110
A、20℃时,100gH2O最多能溶解36.0gNaCl B、40℃时,KNO3饱和溶液的溶质质量分数小于63.9% C、可用冷却海水的方法获取大量食盐 D、其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液9. 下列实验操作能达到实验目的的是( )实验目的
实验操作
A
测定某废水的酸碱度
取样,将湿润的pH试纸浸入样品中
B
除去水中的色素
将水通过装有活性炭的净化装置
C
除去粗盐中的难溶性杂质
溶解、蒸发、结晶
D
检验某固体是否为铵态氮肥
取样,加稀盐酸,闻气味
A、A B、B C、C D、D10. 将一定浓度的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得两者产生的CO2体积(V)与反应时间(t)的关系如下图所示。下列判断错误的是( ) A、0~300s内,两个容器内溶液的pH均逐渐增大 B、0-100s内,反应Ⅰ、Ⅱ生成CO2的速率均先慢后快 C、反应Ⅱ中,0~100s内产生的CO2体积比100-200s内的少5amL D、实验室可以用一定浓度的稀硫酸与CaCO3粉末反应制备CO2
A、0~300s内,两个容器内溶液的pH均逐渐增大 B、0-100s内,反应Ⅰ、Ⅱ生成CO2的速率均先慢后快 C、反应Ⅱ中,0~100s内产生的CO2体积比100-200s内的少5amL D、实验室可以用一定浓度的稀硫酸与CaCO3粉末反应制备CO2二、填空题
-
11. 模型认知是建立宏观与微观联系的思维方法。(1)、①如图为硅在元素周期表中的部分信息,硅的相对原子质量为。

②如图为氧原子结构示意图,x的数值为。在化学变化中,氧原子容易(填“得到”或“失去”)电子。
 (2)、某化学反应的微观示意图如下:
(2)、某化学反应的微观示意图如下:
①
 所表示的微粒中,碳、氢、氧原子的个数比为。
所表示的微粒中,碳、氢、氧原子的个数比为。②
 处的微粒是(填化学式)。(3)、道尔顿原子学说的部分观点如下:
处的微粒是(填化学式)。(3)、道尔顿原子学说的部分观点如下:①原子是不可分割的实心球体;
②物质都是由原子构成的;
③同种元素的所有原子的质量完全相同。
现代科学证实以上观点均不确切,请选择其中一个观点简要说明:
12. 燃烧与人类生产、生活有着密切的关系。(1)、下列成语的原意与燃烧不相关的是____(填标号)。A、卧薪尝胆 B、釜底抽薪 C、火上浇油 D、煽风点火(2)、古籍《天工开物》就有“煤饼烧石成灰”的记载。“烧石成灰”指高温条件下碳酸钙转化为生石灰。①“煤饼烧石成灰”的过程中,能量转化的主要方式是。
②“石”转化为“灰”的反应属于(填基本反应类型)。
③“灰”遇水成浆,该反应的化学方程式为。
(3)、室内起火时,如果急于打开门窗,火反而会烧得更旺。原因是。13. 科学使用化学物质,可以保障人体健康。(1)、某同学的部分体液的pH如图所示。
①图中碱性最强的体液是。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平(主要成分为Al(OH)3)治疗,其原理是(用化学方程式表示)。
(2)、某84消毒液产品的部分说明如下表。84消毒液
(产品特点)主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%。
(餐具消毒)用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。
(注意事项)①外用消毒剂,须稀释后使用。
②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。
依据表中信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1:进行稀释,即可用于餐具消毒。洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整: 2HCl+NaClO=+Cl2↑+H2O。
14. 合理利用化石燃料资源,是人类不断探索的课题。某城市家用燃料的使用经历了下图所示的过程,并将逐步向理想燃料发展。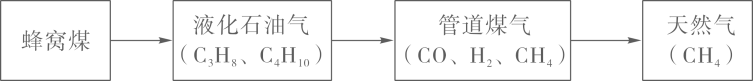
(注:括号中的物质是对应燃料的主要成分)
(1)、CH4、C3H8两种物质中,氢元素的质量分数较大的是(填化学式)。(2)、倡导“家用燃料低碳化”的意义是。(3)、一定条件下,仅用一个置换反应即可制得CO和H2 , 反应的化学方程式为。(4)、随着全球能源使用量的增长,化石燃料等不可再生能源将日趋枯竭。请提出一个缓解能源危机的设想:。15. “铜的循环”如下图所示。其中,箭号表示能一步实现的物质转化方向,X、Y、Z是初中化学常见的物质。 (1)、若反应①为 ,预测该反应可能观察到的实验现象:(写一个)。(2)、反应②中,X的化学式是(写一个)。(3)、Y是黑色固体,反应④的化学方程式为。(4)、利用反应⑤的转化原理,除去FeSO4溶液中的少量CuSO4。需要的药品和分离方法分别是、。(5)、已知:同一化学反应中,若有元素的化合价升高,则必有元素的化合价降低。铜曝露在空气中生成铜锈(主要成分为Cu2(OH)2CO3)的过程中,空气中参与反应的物质是。
(1)、若反应①为 ,预测该反应可能观察到的实验现象:(写一个)。(2)、反应②中,X的化学式是(写一个)。(3)、Y是黑色固体,反应④的化学方程式为。(4)、利用反应⑤的转化原理,除去FeSO4溶液中的少量CuSO4。需要的药品和分离方法分别是、。(5)、已知:同一化学反应中,若有元素的化合价升高,则必有元素的化合价降低。铜曝露在空气中生成铜锈(主要成分为Cu2(OH)2CO3)的过程中,空气中参与反应的物质是。三、实验题
-
16. 请将下列实验报告补充完整。
实验内容
现象
说明、解释或结论
⑴用高锰酸钾制取氧气。
连接仪器,检查装置气密性。用(填仪器名称)取少量高锰酸钾装入试管中,并在试管口放一团棉花,固定好装置,加热试管,用排水法收集O2。
当观察到时,开始收集气体。
收集O2之前,将集气瓶内空气完全排净的方法是。产生O2的化学方程式为。
⑵酸与碱发生中和反应。
i.取少量稀NaOH溶液于试管中,滴入2滴酚酞溶液,再逐滴加入稀盐酸,边滴边振荡,至溶液的颜色恰好变为无色。
ii.往上述无色溶液中再滴入1滴稀NaOH溶液,观察现象。
步骤ⅱ中观察到。
步骤i中“边滴边振荡”的目的是。
四、科学探究题
-
17. 欲证明“CO2与NaOH发生了化学反应”,某化学兴趣小组进行以下探究实验(实验装置中夹持仪器已略去)。(1)、(实验1)配制溶液
用NaOH固体配制20g20%NaOH溶液,无需用到的玻璃仪器有___(填标号)。
A、胶头滴管 B、酒精灯 C、量筒 D、烧杯 E、玻璃棒(2)、(实验2)按如图所示装置进行实验。
实验前U型管两端液面相平,将NaOH溶液滴入试管中,恢复到室温后,U型管中的液面左高右低。据此,甲同学得出“CO2与NaOH发生了化学反应”的结论。
U型管中液面高度发生变化的原因是。
(3)、上述结论的证据不充足,理由是。(4)、(实验3)按如图所示装置进行实验。
查阅资料:i.CaCl2溶液呈中性;ii.
实验步骤如下:
①检查装置的气密性,往装置中加入药品;
②关闭K1、K2 , 将注射器中的NaOH溶液缓缓推入A中;
③A中物质充分作用后,打开K1 , B中无色溶液倒吸入A中,A中产生沉淀且溶液显红色
④关闭K1 , 打开K2 , 将注射器活塞向上拉,C中溶液倒吸入A中。
步骤③“产生沉淀”的现象仍不足以证明CO2与NaOH发生了化学反应,理由是。
(5)、步骤④中,若观察到(填现象),证明CO2与NaOH发生了化学反应。CO2与NaOH反应的化学方程式为。五、计算题
-
18. 推广车用乙醇汽油,可以减少汽车尾气污染。利用秸秆为原料可生产乙醇(C2H6O),其中包含葡萄糖(C6H12O6)转化为乙醇的反应( )。每生产2.3t乙醇,理论上参加反应的葡萄糖的质量是多少?(写出计算过程)
-
-