高中化学人教版(2019)必修第一册 第二章第一节 钠及其化合物
试卷更新日期:2020-07-31 类型:同步测试
一、单选题
-
1. 有关焰色反应的说法正确的是( )A、焰色反应是金属单质表现的性质 B、焰色反应是因为发生了化学变化而产生的 C、焰色反应看到黄色火焰并不能确定该物质一定不含钾元素 D、洗涤焰色反应中用到的铂丝可用稀硫酸代替稀盐酸2. 下列关于Na2O和Na2O2的叙述正确的是( )A、Na2O与Na2O2均可与水反应产生氧气 B、Na2O与Na2O2分别与CO2反应的产物完全相同 C、Na2O与Na2O2均为碱性氧化物 D、在呼吸面具中,Na2O2常做供氧剂,而Na2O不能3. 下列叙述正确的是( )A、Na2O与Na2O2中阴、阳离子的个数比均为1:2 B、足量Cl2、O2分别和两份等质量的Na反应,前者得到电子多 C、胃酸过多可用服用碳酸钠 D、钠投入水中会熔成小球,并四处游动,说明钠与水反应放热并生成氧气4. 观察是研究物质性质的基本方法。一同学将一小块金属钠露置于空气中,观察到下列现象:银白色 变灰暗 变白色 表面潮湿 白色固体,下列说法错误的是( )A、①中钠发生了氧化反应 B、②变白色是因为生成了氢氧化钠 C、③发生物理变化 D、④生成了碳酸氢钠5. 下列解释实验现象的反应方程式正确的是( )A、切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2=Na2O2 B、金属钠比通金属铜活泼,金属钠放入CuSO4溶液:CuSO4+2Na=Cu+Na2SO4 C、Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+2CO2=2Na2CO3+O2 D、将Na块放入水中,产生气体:2Na+2H2O=2NaOH+H2↑6. 取一块金属钠放在燃烧匙里加热,观察到下列现象:①金属先熔化;②在空气中燃烧,表面变暗;③燃烧后得到白色固体;④燃烧后火焰为黄色;⑤燃烧后生成浅黄色固体物质。描述正确的是( )A、①② B、①②③ C、①④ D、①④⑤7. 焰色实验过程中,铂丝的清洗和灼烧与钾焰色实验的观察两项操作如图所示,下列叙述中错误的是( )
 A、每次实验中都要先将铂丝灼烧到火焰颜色,再蘸取被检验物质 B、钾的焰色实验要透过蓝色钴玻璃观察 C、焰色实验是某种金属元素灼烧时所具有的特殊颜色,是化学变化 D、没有铂丝可用无锈铁丝代替进行实验8. 关于 Na2CO3 和 NaHCO3 性质的说法错误的是( )A、热稳定性:NaHCO3<Na2CO3 B、与同浓度盐酸反应的剧烈程度:NaHCO3<Na 2CO3 C、相同温度时,在水中的溶解性:NaHCO3<Na2CO3 D、等物质的量的 Na2CO3、NaHCO3 分别与足量盐酸反应产生的 CO2 质量相同9. 下列叙述中正确的是( )A、向含有 CaCO3 沉淀的水中通入足量的 CO2 , 沉淀不会溶解. B、向 Na2CO3 溶液中逐滴加入含等物质的量HCl的稀盐酸,生成的 CO2 与原 Na2CO3 的物质的量之比为 1:1 C、等质量的 NaHCO3 和 Na2CO3 分别与足量盐酸反应,在同温同压下,生成的 CO2 体积不相同 D、分别向 NaHCO3 溶液和 Na2CO3 溶液中加入 Ca(OH)2 溶液,只有 Na2CO3 溶液产生沉淀10. 要除去碳酸氢钠溶液中混有的少量碳酸钠,最好采用( )A、加入过量的澄清石灰水 B、通入足量的CO2气体 C、将溶液加热蒸干并灼烧 D、加入适量的氢氧化钠溶液11. 某种混合气体可能有N2、HCl、CO,把混合气体依次通过足量的NaHCO3溶液和灼热的氧化铜粉末,气体体积都没有变化;再通过足量的过氧化钠固体,气体体积减小;最后经过铜网,经充分反应后气体体积又减少,但还有气体剩余。以下对混合气体组成的判断,正确的是( )A、一定没有N2 , HCl和CO中至少有一种 B、一定有N2、HCl和CO C、一定有N2 , HCl和CO中至少有一种 D、一定有N2和HCl,没有CO12. 下图模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
A、每次实验中都要先将铂丝灼烧到火焰颜色,再蘸取被检验物质 B、钾的焰色实验要透过蓝色钴玻璃观察 C、焰色实验是某种金属元素灼烧时所具有的特殊颜色,是化学变化 D、没有铂丝可用无锈铁丝代替进行实验8. 关于 Na2CO3 和 NaHCO3 性质的说法错误的是( )A、热稳定性:NaHCO3<Na2CO3 B、与同浓度盐酸反应的剧烈程度:NaHCO3<Na 2CO3 C、相同温度时,在水中的溶解性:NaHCO3<Na2CO3 D、等物质的量的 Na2CO3、NaHCO3 分别与足量盐酸反应产生的 CO2 质量相同9. 下列叙述中正确的是( )A、向含有 CaCO3 沉淀的水中通入足量的 CO2 , 沉淀不会溶解. B、向 Na2CO3 溶液中逐滴加入含等物质的量HCl的稀盐酸,生成的 CO2 与原 Na2CO3 的物质的量之比为 1:1 C、等质量的 NaHCO3 和 Na2CO3 分别与足量盐酸反应,在同温同压下,生成的 CO2 体积不相同 D、分别向 NaHCO3 溶液和 Na2CO3 溶液中加入 Ca(OH)2 溶液,只有 Na2CO3 溶液产生沉淀10. 要除去碳酸氢钠溶液中混有的少量碳酸钠,最好采用( )A、加入过量的澄清石灰水 B、通入足量的CO2气体 C、将溶液加热蒸干并灼烧 D、加入适量的氢氧化钠溶液11. 某种混合气体可能有N2、HCl、CO,把混合气体依次通过足量的NaHCO3溶液和灼热的氧化铜粉末,气体体积都没有变化;再通过足量的过氧化钠固体,气体体积减小;最后经过铜网,经充分反应后气体体积又减少,但还有气体剩余。以下对混合气体组成的判断,正确的是( )A、一定没有N2 , HCl和CO中至少有一种 B、一定有N2、HCl和CO C、一定有N2 , HCl和CO中至少有一种 D、一定有N2和HCl,没有CO12. 下图模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )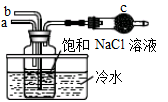 A、a先通入CO2 , 然后b通入NH3 , c中放碱石灰 B、b先通入NH3 , 然后a通入CO2 , c中放碱石灰 C、a先通入NH3 , 然后b通入CO2 , c中放蘸稀硫酸的脱脂棉 D、b先通入CO2 , 然后a通入NH3 , c中放蘸稀硫酸的脱脂棉13. 由CO和H2组成的混合气体2.4g在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为( )A、1.2g B、2.4 g C、3.6g D、无法计算
A、a先通入CO2 , 然后b通入NH3 , c中放碱石灰 B、b先通入NH3 , 然后a通入CO2 , c中放碱石灰 C、a先通入NH3 , 然后b通入CO2 , c中放蘸稀硫酸的脱脂棉 D、b先通入CO2 , 然后a通入NH3 , c中放蘸稀硫酸的脱脂棉13. 由CO和H2组成的混合气体2.4g在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为( )A、1.2g B、2.4 g C、3.6g D、无法计算二、填空题
-
14. 按要求填空:
⑴ 钠与水反应(离方程式)
⑵ 除去碳酸氢钠容液中少量碳酸钠<离子方程式)
⑶ 除去碳酸钠固体混有的碳酸氢钠(化学方程式)
⑷ 镁在二氧化碳中燃烧(化学方程式)
⑸ 二氧化碳中混有少量氯化氢(离子方程式)
15. 将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是①MgSO4溶液②NaCl溶液③Na2SO4溶液④饱和澄清石灰水⑤Ca(HCO3)2溶液⑥CuSO4溶液 ⑦饱和NaCl溶液.
16. 某银白色固体A在空气中点燃,火焰呈黄色,并生成淡黄色固体B;将A在空气中露置,最后变成白色固体C.将A、B投入水中都生成D;B与D分别与二氧化碳反应.则A是;B是;C是;D是 . B与H2O反应的化学方程式 , B与CO2反应的化学方程式为 A与H2O反应的化学方程式 .三、综合题
-
17. NaHSO4与NaHCO3是两种重要的酸式盐.(1)、NaHSO4固体溶于水显酸性,而NaHCO3固体溶于水显碱性,请用离子方程式表示NaHCO3固体溶于水显碱性的原因(2)、NaHSO4和NaHCO3两溶液混合反应的离子方程式为 .(3)、向NaHSO4溶液中逐滴加入Ba(OH)2溶液至呈中性,请写出发生的离子方程式;在以上溶液中,继续滴加Ba(OH)2溶液,此时发生的离子方程式为 .(4)、若将等体积、等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,反应的离子方程式为 .18. 如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3 , D为固定蚊香的硬纸片。试回答下列问题:
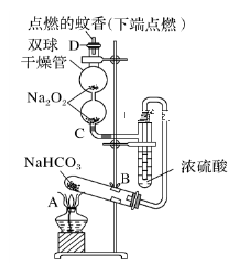 (1)、在A试管内发生反应的化学方程式是。(2)、B装置的作用是。(3)、在双球干燥管内发生反应的化学方程式为。(4)、双球干燥管内及D处观察到的实验现象是。(5)、若将干燥管内的Na2O2换成Na2O,则双球干燥管内及D处观察到的实验现象是:。19. 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。请填写下列空白:
(1)、在A试管内发生反应的化学方程式是。(2)、B装置的作用是。(3)、在双球干燥管内发生反应的化学方程式为。(4)、双球干燥管内及D处观察到的实验现象是。(5)、若将干燥管内的Na2O2换成Na2O,则双球干燥管内及D处观察到的实验现象是:。19. 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。请填写下列空白: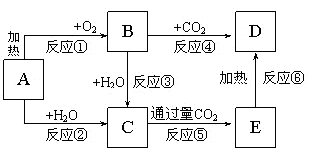 (1)、写出下列物质的化学式:
(1)、写出下列物质的化学式:A , B , C。
(2)、写出下列反应的离子方程式、化学方程式:A→C(离子方程式) ,
B→D(化学方程式)。