高中化学人教版(2019)必修第一册 第一章第二节 离子反应
试卷更新日期:2020-07-31 类型:同步测试
一、单选题
-
1. 下列物质属于电解质且能导电的是( )A、金属铜 B、液态HCl C、酒精 D、熔融KNO32. 下列反应过程中溶液的导电性有显著变化的是( )A、向NaOH溶液中滴加相同浓度的醋酸至完全中和 B、向Ba(OH)2溶液中滴加相同浓度的盐酸至完全中和 C、向Ba(OH)2溶液中滴加相同浓度的稀硫酸至沉淀完全 D、向BaCl2溶液中滴加相同浓度的硝酸银溶液至沉淀完全3. 对于下列实验,能正确描述其反应的离子方程式是( )A、用Na2SO3溶液吸收少量Cl2:3 +Cl2+H2O = 2 +2 + B、向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+ C、向H2O2溶液中滴加少量FeCl3:2Fe3++H2O2=O2↑+2H++2Fe2+ D、同浓度同体积NH4HSO4溶液与NaOH溶液混合: +OH-=NH3·H2O4. Fe3+、 、Al3+和X四种离子以物质的量之比2∶4∶1∶1大量共存于同一溶液中,X可能是( )A、Na+ B、OH- C、CO32- D、Cl-5. 某固体混合物X,含有Cu、Fe2O3、K2SO4、K2SiO3、K2SO3、KAlO2中的几种。进行如下实验:①X与盐酸作用,产生白色沉淀Y和蓝色强酸性溶液Z;②溶液Z中加入BaCl2溶液,产生白色沉淀M。下列说法正确的是( )A、白色沉淀Y能分别溶于HF溶液和氨水 B、往溶液Z中加入过量氨水,产生白色沉淀,说明X中一定含有KAlO2 C、X中一定含有Cu、Fe2O3、K2SiO3 , 可能含有K2SO4 D、沉淀M含有BaSO4、BaSO3中的至少一种6. 不能正确表示下列变化的离子方程式是( )A、用醋酸除去水垢: B、用氢氧化钠溶液除去镁粉中的杂质铝: C、室温下,测得小苏打溶液pH>7,证明碳酸是弱酸: D、将 溶液与0.40mol·L-1NaOH溶液等体积混合:7. 向下列溶液中加入足量Na2O2后,仍能共存的离子是( )A、K+、AlO2-、SO42-、Cl- B、Na+、Cl-、CO32-、SO32- C、Ca2+、Mg2+、HCO3-、NO3- D、NH4+、Ba2+、Cl-、NO3-8. 某学生利用如图装置对电解质溶液导电性进行实验探究。下列说法中正确的是( )
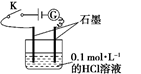 A、闭合开关K,电流计指针发生偏转,证明HCl溶液是电解质 B、闭合开关K,向烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流计指针不发生变化 C、闭合开关K,向溶液中加入CaCO3固体,电流计示数不变 D、选取相同浓度的硫酸替换0.1 mol·L-1的HCl溶液,电流计的示数相同9. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、强碱性溶液中:NH4+、Cl-、Ba2+、Na+ B、新制饱和氯水中:K+、Fe2+、SO32-、SO42- C、澄清透明的溶液中:MnO4-、NO3-、SO42-、K+ D、c(I-)=0.1mol L-1的溶液中:Na+、Fe3+、ClO-、SO42-10. 某无色透明的溶液中只含有Cu2+、Mg2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-中的三种离子,若向其中加入石蕊试剂,溶液显蓝色,则原溶液中能大量存在的离子组是( )A、Ba2+、OH-、NO3- B、Ag+、HCO3-、NO3- C、Mg2+、Ag+、SO42- D、Cu2+、SO42-、OH-11. 下列反应可用2OH-+CO2=CO32-+H2O表示的是( )A、向氨水中通入过量CO2 B、向石灰乳中通入过量CO2 C、向氢氧化钠溶液中通入少量CO2 D、向氢氧化钡溶液中通入少量CO2
A、闭合开关K,电流计指针发生偏转,证明HCl溶液是电解质 B、闭合开关K,向烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流计指针不发生变化 C、闭合开关K,向溶液中加入CaCO3固体,电流计示数不变 D、选取相同浓度的硫酸替换0.1 mol·L-1的HCl溶液,电流计的示数相同9. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、强碱性溶液中:NH4+、Cl-、Ba2+、Na+ B、新制饱和氯水中:K+、Fe2+、SO32-、SO42- C、澄清透明的溶液中:MnO4-、NO3-、SO42-、K+ D、c(I-)=0.1mol L-1的溶液中:Na+、Fe3+、ClO-、SO42-10. 某无色透明的溶液中只含有Cu2+、Mg2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-中的三种离子,若向其中加入石蕊试剂,溶液显蓝色,则原溶液中能大量存在的离子组是( )A、Ba2+、OH-、NO3- B、Ag+、HCO3-、NO3- C、Mg2+、Ag+、SO42- D、Cu2+、SO42-、OH-11. 下列反应可用2OH-+CO2=CO32-+H2O表示的是( )A、向氨水中通入过量CO2 B、向石灰乳中通入过量CO2 C、向氢氧化钠溶液中通入少量CO2 D、向氢氧化钡溶液中通入少量CO2二、填空题
-
12. 现有以下物质: ①NaCl晶体 ②SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥纯蔗糖 ⑦酒精 ⑧熔化的KNO3 ⑨液氨⑩氯酸钾溶液⑪水,请回答下列问题(用序号):(1)、以上物质中能导电的是。(2)、以上物质中属于电解质的是。(3)、以上物质中属于非电解质的是。13. 书写下列反应的离子方程式
①NaOH溶液和H2SO4溶液:;
②NaCl溶液和AgNO3溶液:;
③Ba(OH)2溶液和H2SO4溶液:;
④Fe与CuSO4溶液反应:;
⑤Na2CO3溶液与Ca(OH)2溶液反应:。
14. ①写出Na2SO4的电离方程式 .②氧化铝和氢氧化钠溶液反应的离子反应方程式 .
③OH﹣+H+═H2O改写为化学方程式 .
三、综合题
-
15.(1)、按要求写出方程式:
①HNO3(电离方程式) 。
②Fe2(SO4)3(电离方程式) 。
③硫酸钠和氯化钡溶液反应(离子方程式) 。
④二氧化碳通入足量氢氧化钠溶液(离子方程式)。
(2)、以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有 , 属于非电解质的有(填序号)。16.(1)、写出下列物质的电离方程式① NaOH
② CuCl2
③ Fe2(SO4)3
(2)、写出与下列离子方程式相对应的化学方程式① H+ + OH- = H2O
② 2 H+ + Ca CO3 = Ca2+ + H2O + CO2↑
③ Cu2+ + 2 OH- = Cu(OH)2↓