江苏省扬州市2019-2020学年高一下学期化学期末考试试卷
试卷更新日期:2020-07-30 类型:期末考试
一、单选题
-
1. 习总书记多次强调要“像对待生命一样对待生态环境”。下列做法不应该提倡的是( )A、分类放置生活废弃物 B、实现化石燃料清洁利用 C、使用可降解塑料 D、大量使用化肥、农药提高粮食产量2. 侯氏制碱法原理:NaCl+H2O+CO2+NH3=NaHCO3↓+NH4Cl,下列相关化学用语正确的是( )A、中子数为8的氮原子: B、氧原子的结构示意图:
 C、NaHCO3的电离方程式:NaHCO3=Na++H++
D、CO2的球棍模型:
C、NaHCO3的电离方程式:NaHCO3=Na++H++
D、CO2的球棍模型:  3. 下列物质中属于离子化合物的是( )A、HCl B、NH3 C、NaOH D、H24. 下列各组物质互为同分异构体的是( )A、白磷与红磷 B、甲烷与乙烷 C、正丁烷与异丁烷 D、1H与2H5. 下列各组离子在水溶液中能大量共存的是( )A、 、Cl-、OH- B、Ba2+、H+、 C、Mg2+、K+、OH- D、K+、Na+、6. 下列说法正确的是( )A、1molN2中含有的分子数为2×6.02×1023 B、电解饱和食盐水可得到金属钠 C、常温下,铝片能溶于浓硝酸 D、常温下,淀粉溶液遇I2变成蓝色7. 下列关于化学反应与能量的说法正确的是( )A、化学键断裂放出能量 B、甲烷燃烧时的能量变化如图所示
3. 下列物质中属于离子化合物的是( )A、HCl B、NH3 C、NaOH D、H24. 下列各组物质互为同分异构体的是( )A、白磷与红磷 B、甲烷与乙烷 C、正丁烷与异丁烷 D、1H与2H5. 下列各组离子在水溶液中能大量共存的是( )A、 、Cl-、OH- B、Ba2+、H+、 C、Mg2+、K+、OH- D、K+、Na+、6. 下列说法正确的是( )A、1molN2中含有的分子数为2×6.02×1023 B、电解饱和食盐水可得到金属钠 C、常温下,铝片能溶于浓硝酸 D、常温下,淀粉溶液遇I2变成蓝色7. 下列关于化学反应与能量的说法正确的是( )A、化学键断裂放出能量 B、甲烷燃烧时的能量变化如图所示 C、铝热反应是放热反应
D、吸热反应均需要加热才能发生
8. 下列有关苯、乙烯的说法正确的是( )A、都易溶于水 B、乙烯在一定条件下可发生加聚反应 C、都能使酸性高锰酸钾溶液褪色 D、苯分子中存在碳碳双键9. 对于可逆反应2SO2+O2⇌2SO3 , 下列有关说法正确的是( )A、使用催化剂能加快反应速率 B、降低温度能加快反应速率 C、增大反应物浓度能减慢反应速率 D、SO2、O2能100%转化为产物10. 下列有关物质性质与用途具有对应关系的是( )A、热的碳酸钠溶液碱性较强,可用于洗涤油污 B、液氨具有还原性,可用作制冷剂 C、石墨具有导电性,可用于制铅笔芯 D、浓硫酸具有强氧化性,可用于干燥H211. 锌铜原电池装置如图所示,下列说法正确的是( )
C、铝热反应是放热反应
D、吸热反应均需要加热才能发生
8. 下列有关苯、乙烯的说法正确的是( )A、都易溶于水 B、乙烯在一定条件下可发生加聚反应 C、都能使酸性高锰酸钾溶液褪色 D、苯分子中存在碳碳双键9. 对于可逆反应2SO2+O2⇌2SO3 , 下列有关说法正确的是( )A、使用催化剂能加快反应速率 B、降低温度能加快反应速率 C、增大反应物浓度能减慢反应速率 D、SO2、O2能100%转化为产物10. 下列有关物质性质与用途具有对应关系的是( )A、热的碳酸钠溶液碱性较强,可用于洗涤油污 B、液氨具有还原性,可用作制冷剂 C、石墨具有导电性,可用于制铅笔芯 D、浓硫酸具有强氧化性,可用于干燥H211. 锌铜原电池装置如图所示,下列说法正确的是( )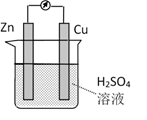 A、Cu是负极 B、反应一段时间后,溶液显蓝色 C、Zn棒发生反应:Zn-2e-=Zn2+ D、该装置实现电能向化学能的转化12. 下列关于元素周期表叙述错误的是( )A、短周期为第1、2、3周期 B、ⅠA族都是金属元素 C、元素周期表中有7个主族 D、可根据元素在周期表中位置预测其性质13. 下列有关浓硝酸说法正确的是( )A、保存在无色试剂瓶中 B、易挥发 C、常温时与铁反应放出氢气 D、受热不分解14. 乳酸具有很强的防腐蚀保鲜功效,其结构简式如图所示。下列有关乳酸说法错误的是( )
A、Cu是负极 B、反应一段时间后,溶液显蓝色 C、Zn棒发生反应:Zn-2e-=Zn2+ D、该装置实现电能向化学能的转化12. 下列关于元素周期表叙述错误的是( )A、短周期为第1、2、3周期 B、ⅠA族都是金属元素 C、元素周期表中有7个主族 D、可根据元素在周期表中位置预测其性质13. 下列有关浓硝酸说法正确的是( )A、保存在无色试剂瓶中 B、易挥发 C、常温时与铁反应放出氢气 D、受热不分解14. 乳酸具有很强的防腐蚀保鲜功效,其结构简式如图所示。下列有关乳酸说法错误的是( ) A、乳酸分子中含有两种含氧官能团 B、乳酸属于烃类有机物 C、乳酸能发生酯化反应 D、乳酸能和金属钠反应放出氢气15. 下列离子方程式书写正确的是( )A、向铁粉中加入足量稀盐酸:Fe+2H+=Fe3++H2↑ B、向FeCl3溶液中加入少量铜粉:Fe3++Cu=Fe2++Cu2+ C、Cu与稀硝酸反应:3Cu+8H++2 =3Cu2++2NO↑+4H2O D、向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-= +2H2O16. 在给定条件下,下列选项所示的物质间转化不能实现的是( )A、CH4 H2 H2O B、N2 NH3 NH
A、乳酸分子中含有两种含氧官能团 B、乳酸属于烃类有机物 C、乳酸能发生酯化反应 D、乳酸能和金属钠反应放出氢气15. 下列离子方程式书写正确的是( )A、向铁粉中加入足量稀盐酸:Fe+2H+=Fe3++H2↑ B、向FeCl3溶液中加入少量铜粉:Fe3++Cu=Fe2++Cu2+ C、Cu与稀硝酸反应:3Cu+8H++2 =3Cu2++2NO↑+4H2O D、向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-= +2H2O16. 在给定条件下,下列选项所示的物质间转化不能实现的是( )A、CH4 H2 H2O B、N2 NH3 NH4Cl C、Cu NO2 HNO3 D、CH2=CH2 CH3CH2OH CH3CHO17. 短周期主族元素X、Y、Z、W在周期表中的位置如图所示,其中Y原子的最外层电子数是内层电子数的3倍,下列说法一定正确的是( )X
Y
Z
W
A、X的简单气态氢化物的热稳定性比W的弱 B、元素Y、Z的简单离子具有相同的电子层结构 C、X与Y只能形成一种化合物 D、W的氧化物形成的晶体是分子晶体18. 下列装置或操作能达到实验目的的是( ) A、用甲所示的装置测量NH3的体积 B、用乙所示的装置灼烧Fe(OH)3固体 C、用丙所示的装置验证生石灰与水反应放热 D、用丁所示的装置制取少量乙酸乙酯
A、用甲所示的装置测量NH3的体积 B、用乙所示的装置灼烧Fe(OH)3固体 C、用丙所示的装置验证生石灰与水反应放热 D、用丁所示的装置制取少量乙酸乙酯二、多选题
-
19. 根据下列实验操作和现象所得出的结论正确的是( )
选项
实验操作和现象
结论
A
向盛有某盐溶液的试管中滴入氢氧化钠溶液后,加热,试管口处湿润的红色石蕊试纸变蓝
该盐中含
B
向溴水中通入某无色气体,溴水褪色
该气体可能是CH2=CH2
C
一定量的铜与硝酸充分反应后,有铜剩余,再加入少量稀硫酸,铜继续溶解,并有气泡放出
Cu与稀硫酸发生了反应
D
向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀
淀粉没有发生水解
A、A B、B C、C D、D20. 向容积为1.00L的密闭容器中通入一定量的N2O4和NO2的混合气体,发生反应:N2O4(g) 2NO2(g)ΔH>0,体系中各物质浓度随时间变化如图所示。下列有关说法正确的是( )
已知:NO2为红棕色气体,N2O4为无色气体
A、64s时,反应达到化学平衡状态 B、到达化学平衡前,混合气体的颜色逐渐变深 C、若该容器与外界无热传递,则反应达到平衡前容器内气体的温度逐渐升高 D、前100s内,用NO2浓度的变化表示的化学反应速率是0.008mol·L-1·s-1三、推断题
-
21. 短周期主族元素X、Y、Z、W原子序数依次增大,X的单质是空气中含量最高的气体,Y的焰色反应现象为黄色。Z为金属元素,由Z制得的容器常温下可盛装浓硫酸。W原子最外层比X原子最外层多2个电子。(1)、X在元素周期表中的位置为 , X单质的结构式为。(2)、W的简单气态氢化物电子式是 , 该气态氢化物溶于水时,破坏的化学键是。(3)、Y、Z、W的原子半径从大到小的顺序是(用元素符号表示)。Y的最高价氧化物的水化物和Z的最高价氧化物的水化物反应的离子方程式是。22. 丙酸乙酯常用于合成人造香料,其合成路线如图所示(部分反应条件略去):
 (1)、化合物B的分子式是 , 化合物C中含氧官能团的名称为。(2)、E→F的化学反应方程式是 , 反应类型是。(3)、A→B的反应是加成反应,则物质X的化学式为。(4)、E→F转化中有多种有机副产物,其中一种副产物Q的相对分子质量为74,氢的质量分数为13.51%,分子中碳氢原子个数比是2∶5,则Q的分子式为。
(1)、化合物B的分子式是 , 化合物C中含氧官能团的名称为。(2)、E→F的化学反应方程式是 , 反应类型是。(3)、A→B的反应是加成反应,则物质X的化学式为。(4)、E→F转化中有多种有机副产物,其中一种副产物Q的相对分子质量为74,氢的质量分数为13.51%,分子中碳氢原子个数比是2∶5,则Q的分子式为。四、工业流程
-
23. 硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O],其相对分子质量为392,在空气中不易被氧化,易溶于水,不溶于乙醇,100℃时易失去结晶水。现用FeSO4溶液与(NH4)2SO4反应,制取硫酸亚铁铵晶体,其流程如图所示:
 (1)、“混合反应”时温度需控制在70~80℃,可采取的措施是 , 该过程中乙醇的作用是。(2)、现对制得的硫酸亚铁铵晶体进行纯度测定:准确称取4.000g上述硫酸亚铁铵晶体置于锥形瓶中溶解,加适量稀硫酸酸化,用0.100mol·L-1标准KMnO4溶液进行反应,当 恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00mL。
(1)、“混合反应”时温度需控制在70~80℃,可采取的措施是 , 该过程中乙醇的作用是。(2)、现对制得的硫酸亚铁铵晶体进行纯度测定:准确称取4.000g上述硫酸亚铁铵晶体置于锥形瓶中溶解,加适量稀硫酸酸化,用0.100mol·L-1标准KMnO4溶液进行反应,当 恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00mL。已知: +5Fe2++8H+=Mn2++5Fe3++4H2O
①若用稀盐酸替代稀硫酸进行酸化,则实际消耗的标准KMnO4溶液的体积20.00mL。(填“大于”或“小于”或“等于”)
②试通过计算,求该硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]的纯度(写出计算过程)
五、综合题
-
24. 2SO2(g)+O2(g)
 2SO3(g)是工业生产硫酸的重要步骤,T℃时该反应过程中的能量变化如图所示:
2SO3(g)是工业生产硫酸的重要步骤,T℃时该反应过程中的能量变化如图所示:  (1)、2SO2(g)+O2(g)
(1)、2SO2(g)+O2(g) 2SO3(g)ΔH=kJ·mol-1( 含E1、E2的计算式表示) (2)、①下列措施不能使该反应速率加快的是。
2SO3(g)ΔH=kJ·mol-1( 含E1、E2的计算式表示) (2)、①下列措施不能使该反应速率加快的是。A.升高温度 B.降低压强 C.使用催化剂
②若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是。
A.SO3的浓度不再变化
B.SO2与SO3的物质的量相等
C.容器内气体的压强不再变化
D.单位时间内消耗1molO2 , 同时消耗2molSO2
(3)、运用电化学原理可生产硫酸,总反应为2SO2+O2+2H2O=2H2SO4 , 装置如图所示。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。
①该电池的负极是。(填“电极a”或“电极b”)
②H+通过质子交换膜时的移动方向是。
A.从左向右 B.从右向左
③通入O2的电极反应式是。
六、实验题
-
25. 某处工厂排出的烟道气中含氮氧化物(主要为NO、NO2)、粉尘和少量水蒸气。课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图所示:
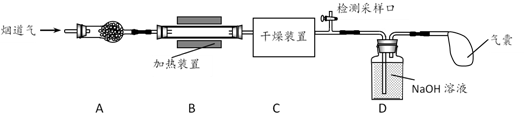 (1)、装置A中放置无碱玻璃棉,其目的是除去。为保证检测的准确性,装置C中盛放的化学试剂可以是(填字母)。
(1)、装置A中放置无碱玻璃棉,其目的是除去。为保证检测的准确性,装置C中盛放的化学试剂可以是(填字母)。a.碱石灰 b.浓硫酸 c.五水合硫酸铜(CuSO4·5H2O)
(2)、装置D中主要发生:2NaOH+2NO2=NaNO2+NaNO3+H2O;2NaOH+NO+NO2=2NaNO2+H2O①若反应后尾气无残留,则参加反应的NO2、NO物质的量比值为(填字母)。
a.≥1 b.≤1 c.任意值
②可使用适量酸性H2O2溶液,将溶液中的NO2-全部氧化为NO3- , 发生反应的离子方程式是。
(3)、溶液中NO3-直接排放在水体中也会造成污染,现用活泼金属将溶液中NO3-转化为N2 , 实现氮元素的脱除,具体步骤如下:步骤一、取适量(2)中H2O2处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO3-)为0.100mol·L-1的溶液甲。
步骤二、现量取50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中对溶液乙进行氮脱除。
步骤三、重复实验2~3次,溶液中NO3-的残留情况与反应时间的关系如图所示。

①金属铝和金属铁在0~3h内,NO3-的脱除效率均很低,几乎没被脱除,其可能的原因是。
②0~3h内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因。
(4)、气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO生成NO3-和Cl- , 发生反应的离子方程式是。
-
-