浙教版科学 九年级上 第一章 第4节 常见的碱
试卷更新日期:2020-07-24 类型:同步测试
一、单选题
-
1. 氢氧化钠、氢氧化钙的溶液都具有相似化学性质,其原因是( )A、都能解离出金属离子 B、都能与酸反应生成盐和水 C、都能使无色酚酞试液变成红色 D、溶液中都含有OH﹣2. 已知氢氧化锂是一种可溶性碱,下列关于氢氧化锂溶液的描述错误的是( )A、氢氧化锂溶液可使酚酞溶液变红色 B、氢氧化锂溶液能与硫酸反应 C、氢氧化锂溶液能与SO2反应 D、氢氧化锂溶液能与碳酸钙反应3. 物质性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体②有腐蚀性③易吸收水分而潮解④易溶于水,溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )A、①② B、③⑤ C、①②③ D、②③④4. 用石灰浆抹墙壁后,墙壁变坚硬的原因是( )A、石灰浆失去水分 B、吸收空气中的水分生成碳酸 C、生成了生石灰 D、吸收空气中的二氧化碳成碳酸钙5. 物质X可发生“X+碱→盐+H2O”的反应,则X可能是( )A、Mg B、CO2 C、KOH D、CaO6. 有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④FeCl3 , 不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是( )A、④③②① B、④①②③ C、①③④② D、①④②③7. 下列物质不能与氢氧化钙溶液发生化学反应的是( )A、稀硫酸 B、氧化铁 C、紫色石蕊试液 D、碳酸钠溶液8. 物质性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体 ②有腐蚀性 ③易吸收水分而潮解 ④易溶于水,溶解放热 ⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )A、①② B、①②③ C、②③④ D、③⑤9. 国庆晚会上小金表演魔术:他拿出一把装满“水”的“宝壶”,分别向编号为ABCDEF六只烧杯(各装有少量不同试剂)中倒“水”,结果A杯呈无色透明,B杯看似红墨水,C杯看似蓝墨水,D杯看似牛奶,E杯看似红褐色涂料,F杯看似蓝色果冻。则宝壶中的“水”可能是 ( )A、H2O2 B、NaOH溶液 C、HCl溶液 D、AgNO3溶液10.
将一大烧杯倒扣在培养皿上,培养皿上所放物质如图所示。下列对有关实验现象的描述肯定不正确的是( )
A、Ⅰ处试液变蓝 B、Ⅱ处溶液变浑浊 C、Ⅲ处溶液颜色逐渐变浅 D、Ⅳ处试纸变红二、填空题
-
11. 氢氧化钠是重要的化工原料,在生活、生产中应用广泛。(1)、氢氧化钠具有强烈的性,实验时最好戴防护眼镜。(2)、氢氧化钠若没有密封保存易变质,要检验氢氧化钠溶液是否变质,下列试剂无法达到目的的是 。(填选项)A、稀HCl B、酚酞试液 C、CaCl2溶液 D、Ca(OH)2溶液12. 在学习碱的性质时,郭老师做了如下实验:先在试管内加适量的水,然后用酒精灯加热至沸腾,然后撤去酒精灯,发现水停止沸腾了,此时向试管中马上加入氢氧化钠固体。请回答:(1)、加入固体后可以观察的实验现象是;(2)、这个实验可以说明氢氧化钠固体具有性质。13. 如图装置可以制造非常有趣的“化学喷泉”,将胶头滴管中的NaOH溶液挤入烧瓶内,在导管的尖嘴处就会形成美丽的“喷泉”。
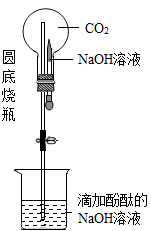 (1)、该现象的出现,原因是瓶内发生化学反应而使瓶内气压减小,请写出反应的化学方程式: 。(2)、若将烧瓶中的CO2换成下面的四种气体,仍可产生“喷泉”现象的瓶是 。A、SO2 B、H2 C、O2 D、HCl14. 化学活动小组的同学用右图所示装置进行实验(装置的气密性良好):先关闭止水夹,将足量氢氧化钠溶液滴入锥形瓶中,充分反应后,再打开止水夹.
(1)、该现象的出现,原因是瓶内发生化学反应而使瓶内气压减小,请写出反应的化学方程式: 。(2)、若将烧瓶中的CO2换成下面的四种气体,仍可产生“喷泉”现象的瓶是 。A、SO2 B、H2 C、O2 D、HCl14. 化学活动小组的同学用右图所示装置进行实验(装置的气密性良好):先关闭止水夹,将足量氢氧化钠溶液滴入锥形瓶中,充分反应后,再打开止水夹.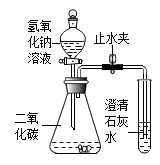 (1)、锥形瓶中能观察到的现象是 ;(2)、根据上述现象,能否得出“二氧化碳与氢氧化钠能反应”的结论?为什么?答:15. 小科通过图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,振荡集气瓶后打开止水夹。
(1)、锥形瓶中能观察到的现象是 ;(2)、根据上述现象,能否得出“二氧化碳与氢氧化钠能反应”的结论?为什么?答:15. 小科通过图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,振荡集气瓶后打开止水夹。 (1)、打开止水夹,观察到的现象是。(2)、实验中不能用澄清石灰水来替代CaCl2溶液,原因是。
(1)、打开止水夹,观察到的现象是。(2)、实验中不能用澄清石灰水来替代CaCl2溶液,原因是。三、实验探究题
-
16. 实验桌上有瓶敞口放置已久的NaOH溶液,小丽对其成分做如下探究:
【实验探究】小丽设计如下实验来验证自己的猜想,请根据表中内容填写实验时的现象
实验步骤
现象
结论
取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液。
___
NaOH溶液部分变质
(1)、按小丽的实验方案进行实验,则你观察到的实验现象.(2)、下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是(填序号).(3)、小丽第二次滴加的试剂除用指示剂外,还可以用替代。17. 科学兴趣小组的同学在探究碱溶液的化学性质时,进行了下图所示的实验。 (1)、实验A中,推入NaOH溶液后,可观察到的现象是。(2)、实验B中发生反应的化学方程式为。
(1)、实验A中,推入NaOH溶液后,可观察到的现象是。(2)、实验B中发生反应的化学方程式为。实验结束后,小组同学对B试管中上层清液的溶质成分产生疑问,作出猜想:
猜想一:只含有NaOH;猜想二:含有NaOH、Na2CO3;猜想三:含有NaOH、Ca(OH)2。同学们取少量B试管中的清液分别置于甲、乙两支试管中,进行探究:
实验操作
实验现象
结论
在试管甲中滴加碳酸钠溶液
不产生白色沉淀
猜想三错误
在试管乙中滴加足量稀盐酸
猜想二正确
(3)、A、B、C、D四个实验中能体现碱化学通性的是(填字母)。小组同学经过讨论认为A、B、C、D四个实验并没有探究出碱所有的化学通性。从这四个实验中选择一个,继续加入相关试剂,能得出碱的其他化学通性。实验的方案是(写出操作和现象)。四、解答题
-
18. 氢氧化钠溶液和二氧化碳反应没有明显现象,为验证CO2与NaOH能够发生反应,某同学按如图组装实验装置,并进行实验。
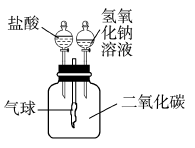 (1)、有时药品滴加顺序会影响实验现象。如果观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是_____(填序号)。A、先加入盐酸,再加入氢氧化钠溶液 B、先加入氢氧化钠溶液,再加入盐酸(2)、请解释气球“先膨胀”的原因: 。(3)、说明能否利用此实验装置验证CO2与NaOH溶液能否发生反应。
(1)、有时药品滴加顺序会影响实验现象。如果观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是_____(填序号)。A、先加入盐酸,再加入氢氧化钠溶液 B、先加入氢氧化钠溶液,再加入盐酸(2)、请解释气球“先膨胀”的原因: 。(3)、说明能否利用此实验装置验证CO2与NaOH溶液能否发生反应。