山东省潍坊市青州市2020年中考化学4月模拟试卷
试卷更新日期:2020-07-22 类型:中考模拟
一、单选题
-
1. 中国酒文化源远流长,下列白酒生产过程中主要属于化学变化的是( )A、谷物粉碎 B、淀粉发酵 C、白酒蒸馏 D、装瓶贴签2. 下列说法正确的是( )A、铵态氮肥不能与碱性物质混合施用 B、空气是由空气分子构成的 C、利用汽油的乳化作用可以除去衣服上的油污 D、棉花、羊毛、蚕丝、涤纶、尼伦和腈纶等都是合成纤维3. 下列有关安全知识的叙述中,正确的是( )A、图书馆着火能用泡沫灭火器扑灭 B、深夜家中煤气泄漏要先开灯寻找漏气源 C、进入干涸的深井,要先用手电筒做灯火实验 D、严禁在加油站、煤气站等处吸烟和拨打移动电话4. 下列实验操作错误的是( )A、加热液体
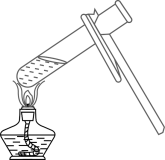 B、读取数据
B、读取数据 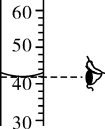 C、滴加试剂
C、滴加试剂 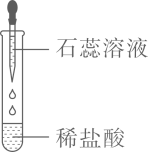 D、蒸发结晶
D、蒸发结晶  5. “天宫二号”太空舱利用NiFe2O4作催化剂将航天员呼出的二氧化碳转化为氧气。已知Fe元素的化合价为+3价,则Ni元素的化合价为( )A、+1 B、+2 C、+3 D、+46. 下列对分子、原子、离子的认识正确的是( )A、同种分子排列方式不同,化学性质不同 B、在干冰中,分子因相互作用而静止不动 C、同种原子按不同方式结合,可以构成不同的物质 D、原子得失电子形成离子后,原子核发生了变化7. 化学与健康生活息息相关。下列做法正确的是( )A、用硫酸铜溶液浸泡粽叶,使粽叶变得鲜绿 B、食品添加剂都对健康有害,应禁止使用 C、误食重金属盐,可以喝大量的鮮榨果汁解毒 D、适量食用加碘盐可以补充微量元素碘,预防甲状腺肿大8. 如表物质的用途与性质对应错误的是( )
5. “天宫二号”太空舱利用NiFe2O4作催化剂将航天员呼出的二氧化碳转化为氧气。已知Fe元素的化合价为+3价,则Ni元素的化合价为( )A、+1 B、+2 C、+3 D、+46. 下列对分子、原子、离子的认识正确的是( )A、同种分子排列方式不同,化学性质不同 B、在干冰中,分子因相互作用而静止不动 C、同种原子按不同方式结合,可以构成不同的物质 D、原子得失电子形成离子后,原子核发生了变化7. 化学与健康生活息息相关。下列做法正确的是( )A、用硫酸铜溶液浸泡粽叶,使粽叶变得鲜绿 B、食品添加剂都对健康有害,应禁止使用 C、误食重金属盐,可以喝大量的鮮榨果汁解毒 D、适量食用加碘盐可以补充微量元素碘,预防甲状腺肿大8. 如表物质的用途与性质对应错误的是( )物质
用途
性质
A
氧气
作火箭发射的助燃剂
氧气具有可燃性
B
熟石灰
改良酸性土壤
熟石灰能与酸发生中和反应
C
小苏打
治疗胃酸过多
小苏打能与盐酸反应
D
氮气
焊接金属时做保护气
氮气的化学性质不活泼
A、A B、B C、C D、D9. 下列对宏观事实的微观解释错误的是( )A、湿衣服晾在阳光充足的地方容易干——温度升高,分子运动加快 B、液态水受热变为水蒸气时体积增大——温度升高,分子体积变大 C、固体碘(I2)和碘蒸气(I2)都能使淀粉溶液变蓝色——同种分子性质相同 D、过氧化氢在催化剂作用下生成水和氧气——化学反应中分子发生改变10. 分类是化学学习、研究的重要方法。下列有关分类正确的是( )A、葡萄糖、油脂和蛋白质都能为人体提供能量 B、氯化钠、苛性钠、纯碱是盐 C、磁铁矿、二氧化锰、二氧化碳是氧化物 D、钙、铁、锌、硒是人体中的微量元素11. 潍坊丘陵地市盛产“富硒小米”,硒有防癌抗癌的功效。如图是硒在元素周期表中的信息,下列关于硒的说法错误的是( ) A、“富硒小米”中的硒是指硒元素 B、人体摄入硒元素的量并非越多越有利于健康 C、硒原子的核外电子数为34,中子数为45 D、硒的原子质量为78.9612. 抗击新冠肺炎疫情中,国内270名新型冠状病毒患者参加了瑞德西韦临床试验,瑞德西韦(分子式:C27H35N6O8P)新药或许会成为抗击新冠肺炎的“特效药”。下列说法正确的是( )A、瑞德西韦属于氧化物 B、瑞德西韦的相对分子质量是602 C、瑞德西韦完全氧化的产物只有二氧化碳和水 D、瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成13. 甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( )
A、“富硒小米”中的硒是指硒元素 B、人体摄入硒元素的量并非越多越有利于健康 C、硒原子的核外电子数为34,中子数为45 D、硒的原子质量为78.9612. 抗击新冠肺炎疫情中,国内270名新型冠状病毒患者参加了瑞德西韦临床试验,瑞德西韦(分子式:C27H35N6O8P)新药或许会成为抗击新冠肺炎的“特效药”。下列说法正确的是( )A、瑞德西韦属于氧化物 B、瑞德西韦的相对分子质量是602 C、瑞德西韦完全氧化的产物只有二氧化碳和水 D、瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成13. 甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( ) A、反应前后碳元素化合价没有发生变化 B、反应中甲和丙的质量之比为4:7 C、水煤气的成分是一氧化碳和氧气 D、反应中含氢元素的化合物有三种14. 模型构建可以变抽象为直观。下图为某原子结构模型的示意图,其中a、b、c是该原子的三种不同粒子,下列说法正确的是( )
A、反应前后碳元素化合价没有发生变化 B、反应中甲和丙的质量之比为4:7 C、水煤气的成分是一氧化碳和氧气 D、反应中含氢元素的化合物有三种14. 模型构建可以变抽象为直观。下图为某原子结构模型的示意图,其中a、b、c是该原子的三种不同粒子,下列说法正确的是( ) A、决定该原子种类的粒子是b B、原子的质量集中在a和c上 C、原子核中可能含有6个c和6个b D、原子中含有6个a和8个c15. 逻辑推理是学好化学的重要思维方法。以下推理正确的是( )A、有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 B、由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成 C、阳离子是带正电的粒子,带正电的粒子一定是阳离子 D、单质是由同种元素组成的,则只含同种元素的纯净物一定是单质16. 将草酸H2C2O4 , 沸点约150℃,分解温度约190℃.隔绝空气加热,得到的混合物经充分冷却后,残余气体M(CO、CO2中的一种或两种)。为探究M的成分,设计如图所示实验。下列说法错误的是( )
A、决定该原子种类的粒子是b B、原子的质量集中在a和c上 C、原子核中可能含有6个c和6个b D、原子中含有6个a和8个c15. 逻辑推理是学好化学的重要思维方法。以下推理正确的是( )A、有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 B、由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成 C、阳离子是带正电的粒子,带正电的粒子一定是阳离子 D、单质是由同种元素组成的,则只含同种元素的纯净物一定是单质16. 将草酸H2C2O4 , 沸点约150℃,分解温度约190℃.隔绝空气加热,得到的混合物经充分冷却后,残余气体M(CO、CO2中的一种或两种)。为探究M的成分,设计如图所示实验。下列说法错误的是( )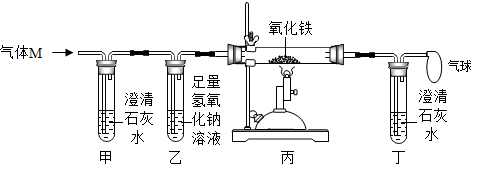 A、若甲试管内溶液变浑浊,则M中一定含有CO2 B、若丙中固体变黑、丁试管内溶液变浑浊,则M中一定含CO C、若装置甲、乙位置互换,则无法判断M中是否含有CO2 D、CO能把氧化铁中的铁元素置换出来17. 下列实验操作、现象或变化、结论对应关系正确的是( )
A、若甲试管内溶液变浑浊,则M中一定含有CO2 B、若丙中固体变黑、丁试管内溶液变浑浊,则M中一定含CO C、若装置甲、乙位置互换,则无法判断M中是否含有CO2 D、CO能把氧化铁中的铁元素置换出来17. 下列实验操作、现象或变化、结论对应关系正确的是( )选项
实验操作
现象或变化
结论
A
取少量井水,加入适量明矾,静置
产生沉淀
明矾可以降低水硬度
B
称量镁条在空气中燃烧前后质量
质量减少
不遵循质量守恒定律
C
向盛有NaOH溶液的试管中滴加几滴酚酞溶液
溶液变红色
NaOH溶液没有变质
D
向某溶液中先后滴加BaCl2溶液和稀硝酸
产生白色沉淀,继续滴加稀硝酸,沉淀不溶解
原溶液中存在Ag+或 SO42﹣
A、A B、B C、C D、D18. 甲、乙两种均不含结晶水的固体物质(设它们从溶液中析出时也都不含结晶水)的溶解度曲线如图所示。下列说法正确的是( ) A、t1℃时,将甲、乙各17g分别加入到50g水中,所得两溶液的质量相等 B、将甲、乙两种溶液由t3℃降温至t2℃,所得两溶液中溶质质量分数一定相等 C、将t3℃时甲的饱和溶液100g 降温至t1℃,析出甲的质量是59.4g D、若甲中混有少量的乙,可先配制较高温度下甲的饱和溶液,再采用降温结晶的方法提纯甲19. 现有氯化铜、烧碱、二氧化碳、氢氧化钙、碳酸钠五种物质的溶液,将其两两混合如图(I),其反应可以得到符合图(Ⅱ)关系的是( )
A、t1℃时,将甲、乙各17g分别加入到50g水中,所得两溶液的质量相等 B、将甲、乙两种溶液由t3℃降温至t2℃,所得两溶液中溶质质量分数一定相等 C、将t3℃时甲的饱和溶液100g 降温至t1℃,析出甲的质量是59.4g D、若甲中混有少量的乙,可先配制较高温度下甲的饱和溶液,再采用降温结晶的方法提纯甲19. 现有氯化铜、烧碱、二氧化碳、氢氧化钙、碳酸钠五种物质的溶液,将其两两混合如图(I),其反应可以得到符合图(Ⅱ)关系的是( ) A、A B、B C、C D、D20. 一定条件下,某反应前后各物质的质量如下表所示。下列判断错误的是( )
A、A B、B C、C D、D20. 一定条件下,某反应前后各物质的质量如下表所示。下列判断错误的是( )物质的构成微粒


M


反应前的质量/g
68
32
0
1
t时刻的质量/g
8
x
反应后的质量/g
0
0
y
37
A、x=0.75y B、物质M中一定不含氧元素 C、反应物的化学计量数之比为2:3 D、反应前后硫元素化合价发生改变二、填空题
-
21. 生活因化学而精彩。“砂锅鱼头”汤鲜汁浓,其烹饪方法为:将鱼头下油锅煎黄后,放入砂锅中加适量食盐、葱段、生姜、香菜、矿泉水等,在火上煨煮数小时即成。(1)、“砂锅鱼头”中几乎不含有的营养素是(填字母序号);用洗洁精清洗油腻的砂锅是利用洗洁精的作用。
A.无机盐
B.油脂
C.糖类
D.水
(2)、用液化气灶煨制砂锅鱼头时,砂锅外壁出现黑灰,此时可将灶具的进风口(填“调大”或“调小”)。液化气的主要成分之一是丙烷(C3H8),写出丙烷完全燃烧的化学方程式。(3)、使用液化气灶一定要注意安全,如果液化气一旦泄漏,遇到明火就可能发生爆炸。从微观角度解释发生爆炸的原因是。(4)、生活中的下列做法应该提倡的是_____。A、垃圾分类 B、减少使用一次性餐具 C、使用可降解的塑料袋 D、淘米水浇花22. 元素周期表是学习化学的重要工具。锶、镁元素在元素周期表中的部分信息及原子结构示意图如图,请回答下列问题。 (1)、写出锶的元素符号 , 它属于(填“金属”或“非金属”)元素,原子核外电子数为 , 图C所表示的粒子的化学符号是。(2)、元素锶和镁的化学性质相似,原因是 , 锶元素和氯元素形成化合物的化学式是。(3)、图E为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是_____。A、原子序数Z>Y B、核外电子数X=Y C、Y和Z处于同一周期 D、X、Y的化学性质相似(4)、元素的性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小。由此推测,锶的金属活动性比镁的金属活动性(选填“强”或“弱”)。23. 在宏观、微观、符号之间建立联系,是化学学科特有的思维方式。
(1)、写出锶的元素符号 , 它属于(填“金属”或“非金属”)元素,原子核外电子数为 , 图C所表示的粒子的化学符号是。(2)、元素锶和镁的化学性质相似,原因是 , 锶元素和氯元素形成化合物的化学式是。(3)、图E为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是_____。A、原子序数Z>Y B、核外电子数X=Y C、Y和Z处于同一周期 D、X、Y的化学性质相似(4)、元素的性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小。由此推测,锶的金属活动性比镁的金属活动性(选填“强”或“弱”)。23. 在宏观、微观、符号之间建立联系,是化学学科特有的思维方式。 (1)、在干冰、金刚石、氯化钠三种物质中,由离子构成的是。(2)、图1描述了稀盐酸与硝酸银溶液反应的微观实质,C处应填入的符号为。(3)、在稀盐酸中加入适量镁条的实验中:
(1)、在干冰、金刚石、氯化钠三种物质中,由离子构成的是。(2)、图1描述了稀盐酸与硝酸银溶液反应的微观实质,C处应填入的符号为。(3)、在稀盐酸中加入适量镁条的实验中:①宏观表征:可以观察到的主要现象为 , 固体逐渐溶解;
②微观表征:如图2表示反应前后溶液中的主要离子,写出
 所表示的微粒符号;
所表示的微粒符号;③符号表征:写出化学方程式。
(4)、以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图。如图3为铁的价类图,请分析该图后填写:①A点表示的物质类别是;
②B点表示化合物的化学式为;
③某化合物化学式为(NH4)2Fe(SO4)2 , 它代表的点是(填“A、B、C、D、E”)。
三、流程题
-
24. 某合金主要成分为Zn、Fe、Cu及这三种金属的少量氧化物。利用该合金制成的机械零件废弃物制取高纯 ZnO,其部分工艺流程如图所示。请回答:

已知:Zn(OH)2溶于强碱形成可溶性盐。
(1)、要验证Zn、Fe、Cu三种金属的活动性顺序,下列方法正确的是_____(填写序号),A、将Zn和Cu分别加入到FeSO4溶液中 B、将Fe分别加入到ZnSO4溶液和CuSO4溶液中 C、将Zn分别加入到FeSO4、CuSO4 D、将三种形状、大小相同的金属分别投入到相同溶质质量分数的稀硫酸中(2)、加酸溶解废弃物时,需要通风并远离火源,此过程中Zn还能起到除铜作用,除铜的化学方程式为 , 此反应属(填基本反应类型),滤渣I的组成中一定有。(3)、调节pH可用NaOH,但不能过量,其原因是。(4)、焙烧Zn(OH)2发生分解反应的化学方程式为。四、实验题
-
25. 回答下列问题

 (1)、标出字母 a、b 的仪器名称:a , b。写出用装置A制取O2的化学方程式。(2)、选用合适的装置制取二氧化碳气体,并能控制反应随时发生随时停止,可选用的发生装置是(填字母序号,下同),收集装置是。(3)、制得的CO2中含有少量的HCl气体和H2O,要除去杂质HCl,可在装置F中盛入小苏打溶液,则混合气体应由装置F(填数字序号)端通入,写出该反应的化学方程式。(4)、实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(已知:氨气密度比空气小,极易溶于水),则实验室制取氨气可选用的实验装置组合为_____(填序号)。A、A和D B、A和E C、B和E D、A和F
(1)、标出字母 a、b 的仪器名称:a , b。写出用装置A制取O2的化学方程式。(2)、选用合适的装置制取二氧化碳气体,并能控制反应随时发生随时停止,可选用的发生装置是(填字母序号,下同),收集装置是。(3)、制得的CO2中含有少量的HCl气体和H2O,要除去杂质HCl,可在装置F中盛入小苏打溶液,则混合气体应由装置F(填数字序号)端通入,写出该反应的化学方程式。(4)、实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(已知:氨气密度比空气小,极易溶于水),则实验室制取氨气可选用的实验装置组合为_____(填序号)。A、A和D B、A和E C、B和E D、A和F五、科学探究题
-
26. “84”消毒液在新冠肺炎预防措施中使用较为广泛,其还具有漂白、杀菌、消毒的功效。某化学兴趣小组对 一瓶敞口久置的“84”消毒液的成分产生兴趣,在老师的指导下,展开探究。
已知:“84”消毒液和洁厕灵作用会产生氯气。
(提出问题)该敞口久置的消毒液中溶质有哪些?
(查阅资料)“84”消毒液的主要成分是次氯酸钠(NaClO)和氯化钠;NaClO 为有效成分,有腐蚀性并 易与空气中的CO2反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效。HClO 不稳定,受热或光照条件下会发生分解。
(1)、(分析讨论)小组同学经过讨论,认为该消毒液中的溶质一定有 , 可能还有NaClO、Na2CO3、HClO中的一种或多种。(实验探究)
实验操作
实验现象
实验结论
Ⅰ.向装入红色布条的试管中加入适量该消毒液
布条长时间不褪色
消毒液中不含
Ⅱ.另取少量该消毒液于试管中,滴入氯化钡溶液
白色沉淀
消毒液中含 , 发生反应的化学方程式为 。
(交流反思)生活中,“84”消毒液贮藏时应注意;一般不用“84”消毒液对蔬菜、水果进行消毒,其原因可能是。
(2)、(拓展延伸)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为。
(3)、“84”消毒液(“能”或“不能”)与洁厕灵混合使用。六、计算题
-
27. 在含氯化钠杂质的碳酸钠13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量与pH的关系如图所示:
 (1)、100g稀盐酸中氯化氢的质量。(2)、完全反应后,计算生成二氧化碳的质量?(写出计算步骤)(3)、完全反应后,所得溶液中溶质的质量分数?(写出计算步骤)
(1)、100g稀盐酸中氯化氢的质量。(2)、完全反应后,计算生成二氧化碳的质量?(写出计算步骤)(3)、完全反应后,所得溶液中溶质的质量分数?(写出计算步骤)
-
-
-