浙教版科学 八年级上 第一章 第5节 物质的溶解
试卷更新日期:2020-07-18 类型:同步测试
一、单选题
-
1. 现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示。下列判断正确的是( )
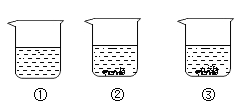 A、①中所得溶液一定是不饱和溶液 B、②③中所得溶液溶质的质量分数相等 C、若②中溶液升温到30℃,溶液的质量一定不变 D、若③中溶液恒温蒸发,溶质的质量分数一定变大2. 某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )A、变大 不变 B、变大 变小 C、不变 变大 D、不变 不变3. 小金在配硝酸钾溶液时得到下表数据,据此分析以下说法正确的是( )
A、①中所得溶液一定是不饱和溶液 B、②③中所得溶液溶质的质量分数相等 C、若②中溶液升温到30℃,溶液的质量一定不变 D、若③中溶液恒温蒸发,溶质的质量分数一定变大2. 某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )A、变大 不变 B、变大 变小 C、不变 变大 D、不变 不变3. 小金在配硝酸钾溶液时得到下表数据,据此分析以下说法正确的是( )序号
温度/℃
水的质量/克
加入硝酸钾的质量/克
所得溶液的质量/克
①
10
100
40
120.9
②
60
100
40
140
A、10℃时硝酸钾的溶解度为40克 B、②所得溶液一定是60℃时硝酸钾的饱和溶液 C、若通过加热将①中剩余硝酸钾全部溶解,则溶液的溶质质量分数与加热前保持一致 D、若将②所得溶液降温至10℃,则溶液的溶质质量分数会变小4. 甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是( ) A、甲的溶解度大于乙的溶解度 B、①②两溶液均变为不饱和溶液 C、①溶液质量增加,②溶液质量减少 D、①溶液中溶质的质量分数大于②溶液5. 50℃的饱和石灰水400克平均分成两份,将一份降温至20℃;另一份加入生石灰0.5克,温度仍保持50℃。在这两种情况下,下列说法正确的是( )A、 溶质质量相同 B、都会变浑浊 C、溶质质量分数相同 D、溶质的溶解度相同6. 甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析正确的是( )
A、甲的溶解度大于乙的溶解度 B、①②两溶液均变为不饱和溶液 C、①溶液质量增加,②溶液质量减少 D、①溶液中溶质的质量分数大于②溶液5. 50℃的饱和石灰水400克平均分成两份,将一份降温至20℃;另一份加入生石灰0.5克,温度仍保持50℃。在这两种情况下,下列说法正确的是( )A、 溶质质量相同 B、都会变浑浊 C、溶质质量分数相同 D、溶质的溶解度相同6. 甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析正确的是( )
 A、甲可能是不饱和溶液,丙和丁一定是饱和溶液 B、丙的溶液质量和乙的相同 C、在甲→丙的过程中,蔗糖的溶解度先增大后减小 D、乙的溶质质量分数比甲大7. 烧杯①中溶液是60℃时含有120g水的NH4Cl溶液,经过图示操作后得到18.0gNH4Cl固体,已知60℃和20℃时,NH4Cl的溶解度分别为55.2g和37.2g。则下列说法正确的是( )
A、甲可能是不饱和溶液,丙和丁一定是饱和溶液 B、丙的溶液质量和乙的相同 C、在甲→丙的过程中,蔗糖的溶解度先增大后减小 D、乙的溶质质量分数比甲大7. 烧杯①中溶液是60℃时含有120g水的NH4Cl溶液,经过图示操作后得到18.0gNH4Cl固体,已知60℃和20℃时,NH4Cl的溶解度分别为55.2g和37.2g。则下列说法正确的是( )
 A、①中溶液和②中溶液均为60℃时NH4Cl的不饱和溶液 B、①中溶液的溶质质量大于②中溶液的溶质质量 C、②中溶液和③中溶液的溶质质量分数相等 D、②中溶液和③中溶液分别为60℃和20℃时NH4Cl的饱和溶液8. 一杯40℃100g硫酸铜饱和溶液,加入16g无水硫酸铜粉末,若不考虑溶剂的蒸发与溶解过程中吸放热的影响,则该溶液与原溶液相比(硫酸铜溶解度随温度变化如表)( )
A、①中溶液和②中溶液均为60℃时NH4Cl的不饱和溶液 B、①中溶液的溶质质量大于②中溶液的溶质质量 C、②中溶液和③中溶液的溶质质量分数相等 D、②中溶液和③中溶液分别为60℃和20℃时NH4Cl的饱和溶液8. 一杯40℃100g硫酸铜饱和溶液,加入16g无水硫酸铜粉末,若不考虑溶剂的蒸发与溶解过程中吸放热的影响,则该溶液与原溶液相比(硫酸铜溶解度随温度变化如表)( )温度/℃
0
10
20
30
40
50
60
70
CuSO4溶解度/g
14.8
17.6
20.5
24.2
28.5
39.6
53.6
73.0
A、由饱和溶液变为不饱和溶液 B、将会析出2.5g蓝色晶体 C、溶质质量变小 D、溶质的质量分数仍为28.5%9. 现有一杯硝酸钾饱和溶液,欲改变其溶质质量分数,下列方法可行的是( )A、加入一定量硝酸钾 B、升温到60℃ C、加入一定量水 D、恒温蒸发部分水10. 30℃时将等质量的两份饱和石灰水一份冷却到20℃,另一份加入少量生石灰,温度仍保持在30℃。则两种情况下均不改变的是( )A、 溶剂的质量 B、溶质的质量 C、溶质的溶解度 D、溶液中溶质的质量分数二、填空题
-
11. 下表是A、B、C三种固体物质在不同温度下(t1<t2<t3)的溶解度,请回答:
温度(℃)
t1
t2
t3
物质A(克)
36.0
36.2
37.3
物质B(克)
31.6
36.2
110.0
物质C(克)
0.165
0.135
0.076
(1)、 ℃时,A、B两种物质的溶解度相同。(2)、t1℃时,分别取等量的B、C饱和溶液于试管甲、乙中(如图)。将试管放入盛有水的烧杯中,向烧杯中加入一定量硝酸铵(不考虑试管中水的变化),有固体析出的试管为(选填“甲”或“乙”)。 (3)、t2℃时,将10克A固体放入40克水中,充分搅拌后,所得溶液中溶质的质量分数为。12. 如图是小华配制100g溶质质量分数为5%的NaCl溶液的实验操作示意图:
(3)、t2℃时,将10克A固体放入40克水中,充分搅拌后,所得溶液中溶质的质量分数为。12. 如图是小华配制100g溶质质量分数为5%的NaCl溶液的实验操作示意图:
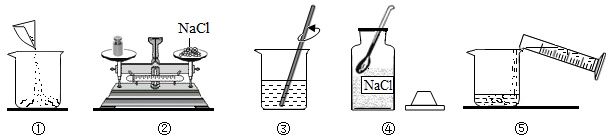 (1)、如图中的玻璃仪器分别是广口瓶、量筒、和玻璃棒,其中玻璃棒在此操作中的作用是。(2)、指出图②中的一处错误操作。(3)、通过计算确定需要水的质量是g,配制时应选择 (填10、50或100)mL的量筒量取所需要的水。量水时,量筒必须平放,视线要跟量筒中水的凹液面的处保持水平。(4)、用上述图示的序号表示配制溶液的操作顺序 。13. KNO3和KCl在不同温度时的溶解度如表所示。请回答下列问题:
(1)、如图中的玻璃仪器分别是广口瓶、量筒、和玻璃棒,其中玻璃棒在此操作中的作用是。(2)、指出图②中的一处错误操作。(3)、通过计算确定需要水的质量是g,配制时应选择 (填10、50或100)mL的量筒量取所需要的水。量水时,量筒必须平放,视线要跟量筒中水的凹液面的处保持水平。(4)、用上述图示的序号表示配制溶液的操作顺序 。13. KNO3和KCl在不同温度时的溶解度如表所示。请回答下列问题:温度/℃
0
10
20
30
40
50
60
70
溶解度/g
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
138
KCl
27.6
31.0
34.0
37.0
40.0
42.6
45.5
48.3
 (1)、依据上表数据,绘制KNO3和KCl的溶解度曲线,右图中能表示KNO3溶解度曲线的是。(填“m”或“n”)(2)、由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是。(3)、10℃时,131g饱和KCl溶液中含KCl的质量为。14. 下表是甲物质在不同温度时溶解度按下图步骤进行操作:
(1)、依据上表数据,绘制KNO3和KCl的溶解度曲线,右图中能表示KNO3溶解度曲线的是。(填“m”或“n”)(2)、由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是。(3)、10℃时,131g饱和KCl溶液中含KCl的质量为。14. 下表是甲物质在不同温度时溶解度按下图步骤进行操作:温度/℃
10
20
30
40
溶解度/g
10.0
18.0
36.0
56.0
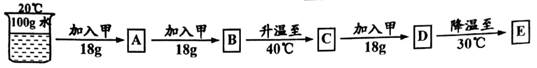 (1)、在A一E的溶液中,溶质质量分数最大的是(填字母)。(2)、要使E中未溶的甲物质全部溶解,至少需要加入30℃的水克。15. 烧杯中盛有150g水,加入某种固体A的进行如下图甲所示的实验操作,得到相应的溶液①~③,请回答下列问题:
(1)、在A一E的溶液中,溶质质量分数最大的是(填字母)。(2)、要使E中未溶的甲物质全部溶解,至少需要加入30℃的水克。15. 烧杯中盛有150g水,加入某种固体A的进行如下图甲所示的实验操作,得到相应的溶液①~③,请回答下列问题: (1)、固体A的溶解度曲线是图乙中的;(2)、①~③溶液中,溶质质量分数的大小关系是 。
(1)、固体A的溶解度曲线是图乙中的;(2)、①~③溶液中,溶质质量分数的大小关系是 。三、解答题
-
16. 小明所在的化学研究性小组在探究溶液的组成时提出了溶液组成的多种表示方法。如小明提出可用溶剂的质量分数表示溶液的组成,小亮提出可用溶质与溶剂的微粒个数比表示溶液的组成,小丽提出若溶液由两种液体组成,可用其中一种液体的体积分数表示,等等。请你加入该小组对有关溶液组成的探究,并回答下列问题:(1)、小明提出的溶剂的质量分数的概念是 。(2)、现有溶剂质量分数为98%的氯化钠溶液100g,欲使其溶剂质量分数变为96%,下列采取的措施中你认为可行的是( )A、将溶液蒸发掉50g水 B、向原溶液中再加入100g水 C、向原溶液中再加入2g氯化钠 D、向原溶液中再加入12g氯化钠17. 20℃时,向甲烧杯中加入100g水和25g固体固体A,向乙烧杯中加入100g水和25g固体B(A、B两种物质均不与水反应),充分搅拌后,甲烧杯中固体剩余,乙烧杯中固体全部溶解。请回答下列问题:(1)、20℃时,甲烧杯中溶液是(填“饱和”或“不饱和”溶液);一定能使甲烧杯中的固体A继续溶解的方法是。(2)、求乙烧杯中B溶液的溶质质量分数(请列式计算)18. 酒精是一种常用的杀菌消毒试剂,但酒精浓度越高并非消毒效果越好。95%酒精溶液能将细菌表面的蛋白质迅速凝固,但也阻止了酒精进一步向细菌内部渗透,细菌内部仍是活性的。75%的酒精溶液兼具蛋白质凝固作用及穿透效果,达到彻底的杀菌功能。(酒精的浓度通常用体积分数表示)
 (1)、用体积分数表示溶液的浓度比较粗略,但简单易行,在实际操作中经常使用。酒精和水以3:1的体积比粗略可以配成体积分数为75%的酒精溶液,请问体积分数为75%的酒精溶液相当于约多少质量分数的酒精溶液(酒精的密度为0.8克/厘米3)(2)、酒精溶液消毒过程中,一般严禁使用喷洒方式消毒,其原因是75%酒精溶液的闪点较低,容易引起火灾。所谓闪点指的是可燃性液体挥发出的蒸汽与空气混合达到一定浓度后遇火源达到闪火燃烧的最低温度,因闪火发生时的温度未达到着火点,闪火通常会瞬间熄灭。下表为不同浓度酒精溶液的闪点。
(1)、用体积分数表示溶液的浓度比较粗略,但简单易行,在实际操作中经常使用。酒精和水以3:1的体积比粗略可以配成体积分数为75%的酒精溶液,请问体积分数为75%的酒精溶液相当于约多少质量分数的酒精溶液(酒精的密度为0.8克/厘米3)(2)、酒精溶液消毒过程中,一般严禁使用喷洒方式消毒,其原因是75%酒精溶液的闪点较低,容易引起火灾。所谓闪点指的是可燃性液体挥发出的蒸汽与空气混合达到一定浓度后遇火源达到闪火燃烧的最低温度,因闪火发生时的温度未达到着火点,闪火通常会瞬间熄灭。下表为不同浓度酒精溶液的闪点。酒精浓度(%)
100
95
75
55
40
10
5
3
闪点(℃)
11
17
22
23
25
50
60
无
根据表格中的信息你能得出的结论是:。
(3)、由于液体燃料的闪点和着火点存在一定差值,有闪火不一定持续燃烧。若从防火安全角度考虑,液体燃料的闪点和着火点的差值(选填“大一些”或“小一些”)对防火更有利。19. 实验室保存﹣瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问: (1)、这一瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)(2)、取200克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?
(1)、这一瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)(2)、取200克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?四、实验探究题
-
20. 配制一定溶质质量分数的氯化钠溶液常按以下操作顺序进行。

请回答下列问题:
(1)、实验室配制一定溶质质量分数的溶液时,可能涉及以下操作:①称量②计算③溶解④量取⑤装瓶贴标签。用氯化钠固体和蒸馏水配制100g5%的氯化钠溶液时,其操作顺序是(填序号)。(2)、计算配制100g溶质质量分数为5%的氯化钠溶液所需氯化钠:g。(3)、用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 (填字母)。A、增加适量氯化钠固体 B、减少适量氯化钠固体 C、调节平衡螺母(4)、配制上述溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒和。