2020年浙江省高考化学试卷(7月选考)
试卷更新日期:2020-07-14 类型:高考真卷
一、单选题
-
1. 水溶液呈酸性的是( )A、 B、 C、 D、2. 固液分离操作中,需要用到的仪器是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列物质在熔融状态下不导电的是( )A、 B、 C、 D、4. 下列物质对应的组成错误的是( )A、干冰: B、熟石灰: C、胆矾: D、小苏打:5. 下列表示错误的是( )A、乙烯的结构式:
3. 下列物质在熔融状态下不导电的是( )A、 B、 C、 D、4. 下列物质对应的组成错误的是( )A、干冰: B、熟石灰: C、胆矾: D、小苏打:5. 下列表示错误的是( )A、乙烯的结构式: B、甲酸甲酯的结构简式:
C、 甲基丁烷的键线式:
B、甲酸甲酯的结构简式:
C、 甲基丁烷的键线式:  D、甲基的电子式:
D、甲基的电子式:  6. 下列说法错误的是( )A、天然气是不可再生能源 B、用水煤气可合成液态碳氢化合物和含氧有机物 C、煤的液化属于物理变化 D、火棉是含氮量高的硝化纤维7. 下列说法正确的是( )A、 和 是两种不同的元素 B、单晶硅和石英互为同素异形体 C、 和 互为同系物 D、H与 在元素周期表中处于同一主族8. 下列说法错误的是( )A、 会破坏铝表面的氧化膜 B、 的热稳定性比 强 C、 具有氧化性,其稀溶液可用于消毒 D、钢铁在潮湿空气中生锈主要是发生了电化学腐蚀9. 下列说法错误的是( )A、高压钠灯可用于道路照明 B、 可用来制造光导纤维 C、工业上可采用高温冶炼黄铜矿的方法获得粗铜 D、 不溶于水,可用作医疗上检查肠胃的钡餐10. 反应 中,氧化产物与还原产物的物质的量之比是( )A、1:2 B、1:1 C、2:1 D、4:111. 下列有关实验说法错误的是( )A、萃取 时,向盛有溴水的分液漏斗中加入 ,振荡、静置分层后,打开旋塞,先将水层放出 B、做焰色反应前,铂丝用稀盐酸清洗并灼烧至火焰呈无色 C、乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞 D、可用 溶液和稀 区分 、 和12. 下列说法正确的是( )A、 在空气中加热可得固体 B、 加入到过量 溶液中可得 C、 在沸腾炉中与 反应主要生成 D、 溶液中加入少量 粉末生成 和13. 能正确表示下列反应的离子方程式是( )A、 溶液与少量 溶液反应: B、电解 水溶液: C、乙酸乙酯与 溶液共热: D、 溶液中滴加稀氨水:14. 下列说法错误的是( )A、相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加 B、油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分 C、根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花 D、淀粉、纤维素、蛋白质都属于高分子化合物15. 有关
6. 下列说法错误的是( )A、天然气是不可再生能源 B、用水煤气可合成液态碳氢化合物和含氧有机物 C、煤的液化属于物理变化 D、火棉是含氮量高的硝化纤维7. 下列说法正确的是( )A、 和 是两种不同的元素 B、单晶硅和石英互为同素异形体 C、 和 互为同系物 D、H与 在元素周期表中处于同一主族8. 下列说法错误的是( )A、 会破坏铝表面的氧化膜 B、 的热稳定性比 强 C、 具有氧化性,其稀溶液可用于消毒 D、钢铁在潮湿空气中生锈主要是发生了电化学腐蚀9. 下列说法错误的是( )A、高压钠灯可用于道路照明 B、 可用来制造光导纤维 C、工业上可采用高温冶炼黄铜矿的方法获得粗铜 D、 不溶于水,可用作医疗上检查肠胃的钡餐10. 反应 中,氧化产物与还原产物的物质的量之比是( )A、1:2 B、1:1 C、2:1 D、4:111. 下列有关实验说法错误的是( )A、萃取 时,向盛有溴水的分液漏斗中加入 ,振荡、静置分层后,打开旋塞,先将水层放出 B、做焰色反应前,铂丝用稀盐酸清洗并灼烧至火焰呈无色 C、乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞 D、可用 溶液和稀 区分 、 和12. 下列说法正确的是( )A、 在空气中加热可得固体 B、 加入到过量 溶液中可得 C、 在沸腾炉中与 反应主要生成 D、 溶液中加入少量 粉末生成 和13. 能正确表示下列反应的离子方程式是( )A、 溶液与少量 溶液反应: B、电解 水溶液: C、乙酸乙酯与 溶液共热: D、 溶液中滴加稀氨水:14. 下列说法错误的是( )A、相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加 B、油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分 C、根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花 D、淀粉、纤维素、蛋白质都属于高分子化合物15. 有关 的说法正确的是( ) A、可以与氢气发生加成反应 B、不会使溴水褪色 C、只含二种官能团 D、 该物质与足量 溶液反应,最多可消耗16. X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为 价,Y元素与Z、M元素相邻,且与M元素同主族;化合物 的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法错误的是( )A、原子半径: B、最高价氧化物对应水化物的酸性: C、 易溶于水,其水溶液呈碱性 D、X、Z和Q三种元素形成的化合物一定是共价化合物17. 下列说法错误的是( )A、 的盐酸中 B、将 溶液从常温加热至 ,溶液的 变小但仍保持中性 C、常温下, 溶液呈碱性,说明 是弱电解质 D、常温下, 为3的醋酸溶液中加入醋酸钠固体,溶液 增大18. 溶液与 溶液发生反应: ,达到平衡。下列说法错误的是( )A、加入苯,振荡,平衡正向移动 B、经苯2次萃取分离后,在水溶液中加入 ,溶液呈血红色,表明该化学反应存在限度 C、加入 固体,平衡逆向移动 D、该反应的平衡常数19. 为阿伏加德罗常数的值。下列说法正确的是( )A、 , 完全反应转移的电子数为 B、用电解粗铜的方法精炼铜,当电路中通过的电子数为 时,阳极应有 转化为 C、常温下, 的 溶液中,水电离出的 数为 D、 浓度为 的 溶液中,阴离子数为20. 一定条件下: 。在测定 的相对分子质量时,下列条件中,测定结果误差最小的是( )A、温度 、压强 B、温度 、压强 C、温度 、压强 D、温度 、压强21. 电解高浓度 (羧酸钠)的 溶液,在阳极 放电可得到 (烷烃)。下列说法错误的是( )A、电解总反应方程式: B、 在阳极放电,发生氧化反应 C、阴极的电极反应: D、电解 、 和 混合溶液可得到乙烷、丙烷和丁烷22. 关于下列 的判断正确的是( )A、 B、 C、 D、23. 常温下,用 氨水滴定 浓度均为 的 和 的混合液,下列说法错误的是( )A、在氨水滴定前, 和 的混合液中 B、当滴入氨水 时, C、当滴入氨水 时, D、当溶液呈中性时,氨水滴入量大于 ,24. 是硅酸盐水泥的重要成分之一,其相关性质的说法错误的是( )A、可发生反应: B、具有吸水性,需要密封保存 C、能与 ,反应生成新盐 D、与足量盐酸作用,所得固体产物主要为25. 黄色固体X,可能含有漂白粉、 、 、 、 之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )A、X中含 ,可能含有 B、X中含有漂白粉和 C、X中含有 ,Y中含有 D、用 酸化溶液Z,若有黄绿色气体放出,说明X中含有
的说法正确的是( ) A、可以与氢气发生加成反应 B、不会使溴水褪色 C、只含二种官能团 D、 该物质与足量 溶液反应,最多可消耗16. X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为 价,Y元素与Z、M元素相邻,且与M元素同主族;化合物 的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法错误的是( )A、原子半径: B、最高价氧化物对应水化物的酸性: C、 易溶于水,其水溶液呈碱性 D、X、Z和Q三种元素形成的化合物一定是共价化合物17. 下列说法错误的是( )A、 的盐酸中 B、将 溶液从常温加热至 ,溶液的 变小但仍保持中性 C、常温下, 溶液呈碱性,说明 是弱电解质 D、常温下, 为3的醋酸溶液中加入醋酸钠固体,溶液 增大18. 溶液与 溶液发生反应: ,达到平衡。下列说法错误的是( )A、加入苯,振荡,平衡正向移动 B、经苯2次萃取分离后,在水溶液中加入 ,溶液呈血红色,表明该化学反应存在限度 C、加入 固体,平衡逆向移动 D、该反应的平衡常数19. 为阿伏加德罗常数的值。下列说法正确的是( )A、 , 完全反应转移的电子数为 B、用电解粗铜的方法精炼铜,当电路中通过的电子数为 时,阳极应有 转化为 C、常温下, 的 溶液中,水电离出的 数为 D、 浓度为 的 溶液中,阴离子数为20. 一定条件下: 。在测定 的相对分子质量时,下列条件中,测定结果误差最小的是( )A、温度 、压强 B、温度 、压强 C、温度 、压强 D、温度 、压强21. 电解高浓度 (羧酸钠)的 溶液,在阳极 放电可得到 (烷烃)。下列说法错误的是( )A、电解总反应方程式: B、 在阳极放电,发生氧化反应 C、阴极的电极反应: D、电解 、 和 混合溶液可得到乙烷、丙烷和丁烷22. 关于下列 的判断正确的是( )A、 B、 C、 D、23. 常温下,用 氨水滴定 浓度均为 的 和 的混合液,下列说法错误的是( )A、在氨水滴定前, 和 的混合液中 B、当滴入氨水 时, C、当滴入氨水 时, D、当溶液呈中性时,氨水滴入量大于 ,24. 是硅酸盐水泥的重要成分之一,其相关性质的说法错误的是( )A、可发生反应: B、具有吸水性,需要密封保存 C、能与 ,反应生成新盐 D、与足量盐酸作用,所得固体产物主要为25. 黄色固体X,可能含有漂白粉、 、 、 、 之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )A、X中含 ,可能含有 B、X中含有漂白粉和 C、X中含有 ,Y中含有 D、用 酸化溶液Z,若有黄绿色气体放出,说明X中含有二、非选择题
-
26.(1)、气态氢化物热稳定性 大于 的主要原因是。(2)、 是离子化合物,各原子均满足8电子稳定结构, 的电子式是。(3)、常温下,在水中的溶解度乙醇大于氯乙烷,原因是。27. 溶液与 锌粉在量热计中充分反应。测得反应前温度为 ,反应后最高温度为 。
已知:反应前后,溶液的比热容均近似为 、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)、反应放出的热量 J。(2)、反应 的 (列式计算)。28.(1)、Ⅰ.化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝的气体Y,Y为纯净物;取 ,用含 的盐酸完全溶解得溶液A,将溶液A分成 和 两等份,完成如下实验(白色沉淀C可溶于 溶液):
请回答:
组成X的四种元素是N、H和(填元素符号),X的化学式是。
(2)、溶液B通入过量 得到白色沉淀C的离子方程式是。(3)、写出一个化合反应(用化学方程式或离子方程式表示)。要求同时满足:①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“ ”相同。
(4)、Ⅱ.某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有白雾,烧杯中出现白色沉淀。请回答:
将浓硫酸和浓盐酸混合可产生 气体的原因是。
(5)、烧杯中出现白色沉淀的原因是。29. 研究 氧化 制 对资源综合利用有重要意义。相关的主要化学反应有:Ⅰ
Ⅱ
Ⅲ
Ⅳ
已知: 时,相关物质的相对能量(如图1)。

可根据相关物质的相对能量计算反应或变化的 ( 随温度变化可忽略)。例如: 。
请回答:
(1)、①根据相关物质的相对能量计算 。②下列描述正确的是
A 升高温度反应Ⅰ的平衡常数增大
B 加压有利于反应Ⅰ、Ⅱ的平衡正向移动
C 反应Ⅲ有助于乙烷脱氢,有利于乙烯生成
D 恒温恒压下通水蒸气,反应Ⅳ的平衡逆向移动
③有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下: ,且第二步速率较慢(反应活化能为 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从 的能量 ,开始(如图2)
。
 (2)、① 和 按物质的量1:1投料,在 和保持总压恒定的条件下,研究催化剂X对“ 氧化 制 ”的影响,所得实验数据如下表:
(2)、① 和 按物质的量1:1投料,在 和保持总压恒定的条件下,研究催化剂X对“ 氧化 制 ”的影响,所得实验数据如下表:催化剂
转化率
转化率
产率
催化剂X
19.0
37.6
3.3
结合具体反应分析,在催化剂X作用下, 氧化 的主要产物是 , 判断依据是。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高 的选择性(生成 的物质的量与消耗 的物质的量之比)。在 ,乙烷平衡转化率为 ,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到 。结合具体反应说明乙烷转化率增大的原因是。
30. 硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备 。
合成反应:
滴定反应:
已知: 易溶于水,难溶于乙醇, 开始失结晶水。
实验步骤:
Ⅰ. 制备:装置A制备的 经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液 约为7时,停止通入 气体,得产品混合溶液。
Ⅱ.产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到 产品。
Ⅲ.产品纯度测定:以淀粉作指示剂,用 产品配制的溶液滴定碘标准溶液至滴定终点,计算 含量。
请回答:
(1)、步骤Ⅰ:单向阀的作用是;装置C中的反应混合溶液 过高或过低将导致产率降低,原因是。(2)、步骤Ⅱ:下列说法正确的是。A 快速蒸发溶液中水分,可得较大晶体颗粒
B 蒸发浓缩至溶液表面出现品晶膜时,停止加热
C 冷却结晶后的固液混合物中加入乙醇可提高产率
D 可选用冷的 溶液作洗涤剂
(3)、步骤Ⅲ①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→()→()→()→()→()→开始滴定。
A 烘干 B 装入滴定液至零刻度以上 C 调整滴定液液面至零刻度或零刻度以下D 用洗耳球吹出润洗液 E 排除气泡 F 用滴定液润洗2至3次 G 记录起始读数
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是。
③滴定法测得产品中 含量为 ,则 产品中可能混有的物质是。
31. 某研究小组以邻硝基甲苯为起始原料,按下列路线合成利尿药美托拉宗。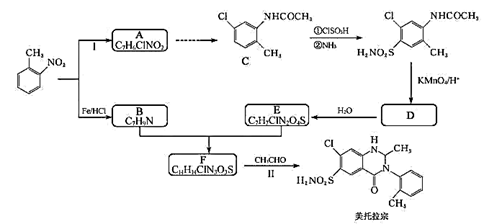
已知:
R-COOH+
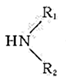
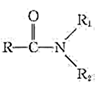
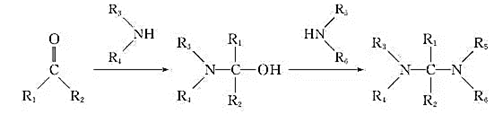
请回答:
(1)、下列说法正确的是。A 反应Ⅰ的试剂和条件是 和光照 B 化合物C能发生水解反应
C 反应Ⅱ涉及到加成反应、取代反应 D 美托拉宗的分子式是
(2)、写出化合物D的结构简式。(3)、写出 的化学方程式。(4)、设计以A和乙烯为原料合成C的路线(用流程图表示,无机试剂任选)。(5)、写出化合物A同时符合下列条件的同分异构体的结构简式。谱和 谱检测表明:①分子中共有4种氢原子,其中环上的有2种;②有碳氧双键,无氮氧键和 。