陕西省汉中市2020年高考理综-化学二模试卷
试卷更新日期:2020-07-09 类型:高考模拟
一、单选题
-
1. 化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是( )A、自来水厂常用明矾作消毒杀菌剂 B、高铁车用大部分材料是铝合金,铝合金材料具有强度大、质量轻、抗腐蚀能力强等优点 C、硅胶可作瓶装药品的干燥剂及催化剂载体,也是重要的半导体材料 D、使用肥皂洗手可预防病毒,肥皂的主要成分硬脂酸钠溶于水显酸性2. 设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )A、常温常压下,等物质的量浓度的Na2CO3与Na2S溶液中阳离子的数目相等 B、标准状况下,22.4LHF所含有的分子数目为NA C、常温常压下,NO2与N2O4的混合气体46g,原子总数为3NA D、0.1mol-NH2(氨基)中所含有的电子数为NA3. 某有机物的结构简式如图所示。下列关于该有机物的说法正确的是( )
 A、该有机物能发生酯化、加成、氧化、水解等反应 B、该有机物中所有碳原子不可能处于同一平面上 C、与该有机物具有相同官能团的同分异构体有3种 D、1mol该有机物最多与4molH2反应4. 短周期主族元素W、X、Y、Z的原子序数依次递增。X和Z形成的化合物的水溶液呈中性,W和X的最外层电子数之和等于Z的最外层电子数,同一主族的W和Y,Y的原子序数是W的2倍,下列说法错误的是( )A、原子半径:W<Z<Y<X B、Y的气态氢化物的稳定性弱于Z的气态氢化物 C、W与X形成的化合物不可能含有共价键 D、常温常压下,Y的单质是固态5. 某种钴酸锂电池的电解质为LiPF6 , 放电过程反应式为xLi+L1-xCoO2=LiCoO2。工作原理如图所示,下列说法正确的是( )
A、该有机物能发生酯化、加成、氧化、水解等反应 B、该有机物中所有碳原子不可能处于同一平面上 C、与该有机物具有相同官能团的同分异构体有3种 D、1mol该有机物最多与4molH2反应4. 短周期主族元素W、X、Y、Z的原子序数依次递增。X和Z形成的化合物的水溶液呈中性,W和X的最外层电子数之和等于Z的最外层电子数,同一主族的W和Y,Y的原子序数是W的2倍,下列说法错误的是( )A、原子半径:W<Z<Y<X B、Y的气态氢化物的稳定性弱于Z的气态氢化物 C、W与X形成的化合物不可能含有共价键 D、常温常压下,Y的单质是固态5. 某种钴酸锂电池的电解质为LiPF6 , 放电过程反应式为xLi+L1-xCoO2=LiCoO2。工作原理如图所示,下列说法正确的是( ) A、放电时,正极反应式为xLi++Li1-xCoO2+xe-=LiCoO2 B、放电时,电子由R极流出,经电解质流向Q极 C、充电时,R极净增14g时转移1 mol电子 D、充电时,Q极为阴极6. 下列实验操作与预期实验目的或所得实验结论一致的是( )
A、放电时,正极反应式为xLi++Li1-xCoO2+xe-=LiCoO2 B、放电时,电子由R极流出,经电解质流向Q极 C、充电时,R极净增14g时转移1 mol电子 D、充电时,Q极为阴极6. 下列实验操作与预期实验目的或所得实验结论一致的是( )选项
实验操作和现象
预期实验目的或结论
A
用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色
说明该食盐试样不含KIO3
B
SiO2能与氢氟酸及碱反应
SiO2是两性氧化物
C
向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀
KI3溶液中存在平衡: I2+I-
D
室温下向CuCl2和少量FeCl3的混合溶液中,加入铜屑,充分搅拌,过滤,得蓝绿色溶液
除去杂质FeCl3得纯净CuCl2溶液
A、A B、B C、C D、D7. 298K时,甲酸(HCOOH)和甲酸钠的混合溶液中HCOOH、HCOO−的浓度存在关系式c(HCOO−)+c(HCOOH)=0.100mol·L−1 , 而含碳元素的粒子的浓度与pH的关系如图所示:
下列说法正确的是( )
A、0.1mol·L−1HCOONa溶液中有c(HCOO−)+c(HCOOH)+c(OH−)=c(H+)+0.1 B、298K时,HCOOH的电离常数Ka=1.0×10−3.75 C、298K时,加蒸馏水稀释P点溶液,溶液中n(H+)·n(OH−)保持不变 D、0.1mol·L−1HCOONa溶液和0.1mol·L−1HCOOH溶液等体积混合后混合液的pH=3.75(混合后溶液体积变化忽略不计)二、综合题
-
8. 环境问题是广大群众关注的热点话题之一,化工厂排放的废水、废渣一般利用化学原理可以进行排放物达标检测与无害化处理。某皮革厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:

已知:①酸浸后的溶液中的金属离子主要是Cr3+ , 其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子
Fe3+
Mg2+
Al3+
Cr3+
沉淀完全时的pH
3.7
11.1
5.4
9
沉淀溶解时的pH
—
—
>8溶解
>9溶解
(1)、如需配制480 mL酸浸环节所需的硫酸,需要用量筒量取18.4 mol·L-1的浓硫酸mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需哪些仪器。(2)、经氧化环节滤液Ⅰ中的Cr3+转化为Cr2O72- , 写出此反应的离子方程式:。(3)、调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O72-转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请解释该颜色变化的原因。(4)、钠离子交换树脂的反应原理为Mn++nNaR⇌MRn+nNa+ , 则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有。(5)、请写出流程中用SO2进行还原时发生反应的离子方程式:。(6)、沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-的浓度,可用标准AgNO3溶液滴定待测液,已知:银盐性质
AgCl
AgI
AgCN
Ag2CrO4
AgSCN
颜色
白
黄
白
砖红
白
Ksp
1.8×10-10
8.3×10-17
1.2×10-16
3.5×10-11
1.0×10-12
①滴定时可选为滴定指示剂的是(填编号),
A.NaCl B.K2CrO4 C.KI D.NaCN
②如何确定该滴定过程的终点:。
9. 利用碳和水蒸气制备水煤气的核心反应为:C(s)+H2O(g)⇌H2(g)+CO(g)(1)、已知碳(石墨)、H2、CO的燃烧热分别为393.5kJ·mol-1、285.8kJ·mol-1、283kJ·mol-1 , 又知H2O(l)=H2O(g) ΔH=+44kJ·mol-1 , 则C(s)+H2O(g)⇌CO(g)+H2(g) ΔH=。(2)、在某温度下,在体积为1L的恒容密闭刚性容器中加入足量活性炭,并充入1mol H2O(g)发生上述反应,反应时间与容器内气体总压强的数据如表:时间/min
0
10
20
30
40
总压强/100kPa
1.0
1.2
1.3
1.4
1.4
①平衡时,容器中气体总物质的量为mol,H2O的转化率为。
②该温度下反应的平衡分压常数Kp=kPa(结果保留2位有效数字)。
(3)、保持25℃、体积恒定的1L容器中投入足量活性炭和相关气体,发生可逆反应C+H2O(g)⇌CO+H2并已建立平衡,在40 min时再充入一定量H2 , 50min时再次达到平衡,反应过程中各物质的浓度随时间变化如图所示:
①40min时,再充入的H2的物质的量为mol。
②40~50 min内H2的平均反应速率为mol·L-1·min-1。
(4)、新型的钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其原理如图所示:
①放电时,电极A为极,S发生反应(填“氧化”或“还原”)。
②充电时,总反应为Na2Sx=2Na+Sx(3<x<5),Na所在电极与直流电源极相连,阳极的电极反应式为。
10. 2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷汉和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:(1)、LiCoO2、LiFePO4常用作锂离子电池的正极材料。①基态Co原子核外电子排布式为;
②基态磷原子中,电子占据的最高能层符号为;该能层能量最高的电子云在空间有个伸展方向。
(2)、[Co(NO3)4]2-的配体中N原子的杂化方式为 , 该配离子中各元素的第一电离能由小到大的顺序为(填元素符号),1mol该配离子中含σ键数目为NA。(3)、LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为(用n代表P原子数)。
(4)、①Li2O被广泛用作玻璃的组分,其熔点Na2O(填高于或者低于),判断理由。②Li2O具有反萤石结构,晶胞如图所示,已知其晶胞参数为0.4665nm,NA为阿伏加德罗常数的值,则Li2O的密度为g·cm-3(列出计算式)。
 11. 我国第二代身份证采用的是具有绿色环保性能的PETG新材料,该材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:
11. 我国第二代身份证采用的是具有绿色环保性能的PETG新材料,该材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:
可采用的合成路线如图所示:

已知:①A的产量是衡量一个国家石油化工发展水平的重要标志之一。
②


③RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)、C的名称为 , 反应①的类型为。(2)、反应③所需条件为 , 试剂X为。(3)、写出I的结构简式:。(4)、写出反应⑤的化学方程式:(5)、与E互为同分异构体,且满足以下条件的有机物共有种,其中核磁共振氢谱有4组峰,峰面积比为1:2:2:1的一种同分异构体的结构简式为。①芳香化合物;②一定条件下能发生银镜反应;③能与NaHCO3溶液反应生成气体。
(6)、请以甲苯为原料,设计制备苯甲酸苯甲酯的合成路线。(无机试剂任选,合成路线示例见本题干)三、实验题
-
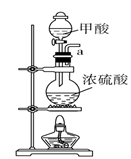
12. 甲酸(化学式HCOOH,分子式CH2O2 , 相对分子质量46),俗名蚁酸,是最简单的羧酸,无色而有刺激性气味的易挥发液体。熔点为8.6 ℃,沸点100.8℃,25℃电离常数Ka=1.8×10-4。某化学兴趣小组进行以下实验。(1)、Ⅰ.用甲酸和浓硫酸制取一氧化碳
A.
 B.
B. 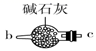 C.
C. 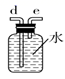 D.
D. 
请说出图B中盛装碱石灰的仪器名称。用A图所示装置进行实验。利用浓硫酸的脱水性,将甲酸与浓硫酸混合,甲酸发生分解反应生成CO,反应的化学方程式是;实验时,不需加热也能产生CO,其原因是。
(2)、如需收集CO气体,连接上图中的装置,其连接顺序为:a→(按气流方向,用小写字母表示)。(3)、Ⅱ.对一氧化碳的化学性质进行探究资料:ⅰ.常温下,CO与PdCl2溶液反应,有金属Pd和CO2生成,可用于检验CO;
ⅱ.一定条件下,CO能与NaOH固体发生反应:CO+NaOH HCOONa
利用下列装置进行实验,验证CO具有上述两个性质。

打开k2 , F装置中发生反应的化学方程式为;为了使气囊收集到纯净的CO,以便循环使用,G装置中盛放的试剂可能是 , H装置的作用是。
(4)、现需验证E装置中CO与NaOH固体发生了反应,某同学设计下列验证方案:取少许固体产物,配置成溶液,在常温下测该溶液的pH,若pH>7,证明CO与NaOH固体发生了反应。该方案是否可行,请简述你的观点和理由: , 。(5)、25℃甲酸钠(HCOONa)的水解平衡常数Kh的数量级为。若向100mL 0.1mol.L-1的HCOONa溶液中加入100mL0.2mol.L-1的HCl溶液,则混合后溶液中所有离子浓度由大到小排序为。