安徽省宣城市2020年高考理综-化学二模试卷
试卷更新日期:2020-07-09 类型:高考模拟
一、单选题
-
1. 化学与生产生活关系密切。下列有关说法错误的是( )A、港珠澳大桥使用的超高分子量聚乙烯纤维属于有机高分子化合物 B、质谱法是测定有机物相对分子质量及确定化学式的分析方法之一 C、“玉兔二号”月球车使用的帆板太阳能电池的材料是 D、宋·王希孟《千里江山图》卷中绿色颜料“铜绿”的主要成分是碱式碳酸铜2. 设 为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是: 。下列说法正确的是( )A、如果氯气管道漏气,则会看到有大量白雾生成 B、反应中每形成 键,转移电子数为 C、 的 溶液中, 的数目小于 D、该反应中,氧化剂与还原剂的物质的量之比为3. 乙酸异戊酯是蜜蜂信息素的成分之一,具有香蕉的香味。实验室中可利用乙酸和异戊醇
 制备乙酸异戊酯,装置图(夹持装置略)和所用药品有关数据如下。下列说法正确的是( )
制备乙酸异戊酯,装置图(夹持装置略)和所用药品有关数据如下。下列说法正确的是( ) 
药品
密度/( )
沸点/℃
水中溶解性
异戊醇
0.8123
131
微溶
乙酸
1.0492
118
易溶
乙酸异戊醇
0.8670
142
难溶
A、反应方程式为CH3COOH+
 B、实验时,冷凝水应从直形冷凝管的b口通入
C、异戊醇的同分异构体中属于醇类的有7种
D、反应后,取Ⅱ中物质经水洗、碱洗和蒸馏可提纯乙酸异戊酯
4. 微生物燃料电池(MFC)为可再生能源的开发和难降解废弃物的处理提供了一条新途径。某微生物燃料电池示意图如图所示(假设废弃物为乙酸盐)。下列说法错误的是( )
B、实验时,冷凝水应从直形冷凝管的b口通入
C、异戊醇的同分异构体中属于醇类的有7种
D、反应后,取Ⅱ中物质经水洗、碱洗和蒸馏可提纯乙酸异戊酯
4. 微生物燃料电池(MFC)为可再生能源的开发和难降解废弃物的处理提供了一条新途径。某微生物燃料电池示意图如图所示(假设废弃物为乙酸盐)。下列说法错误的是( ) A、甲室菌为好氧菌,乙室菌为厌氧菌 B、甲室的电极反应式为 C、该微生物燃料电池(MFC)电流的流向:由b经导线到a D、电池总反应式为5. 和 为原子序数依次增大的短周期元素, 同主族且能形成离子化合物, 的最外层电子数是 质子数之和的一半, 原子的核外电子数为偶数。四种元素组成的一种化合物 具有下列性质。下列说法正确的是( )
A、甲室菌为好氧菌,乙室菌为厌氧菌 B、甲室的电极反应式为 C、该微生物燃料电池(MFC)电流的流向:由b经导线到a D、电池总反应式为5. 和 为原子序数依次增大的短周期元素, 同主族且能形成离子化合物, 的最外层电子数是 质子数之和的一半, 原子的核外电子数为偶数。四种元素组成的一种化合物 具有下列性质。下列说法正确的是( )白色沉淀 M 溶液褪色并产生气泡
A、原子半径: B、 使溴水褪色体现氧化性 C、简单氢化物的稳定性: D、 与 均能形成具有漂白性的物质6. 下列有关实验现象和解释或结论都正确的是( )选项
实验操作
现象
解释或结论
A
取硫酸催化淀粉水解的反应液,滴入少量新制 悬浊液并加热
有砖红色沉淀生成
葡萄糖具有还原性
B
溶液与 溶液混合
有白色絮状沉淀生成
二者水解相互促进生成氢氧化铝沉淀
C
将充满 和 混合气体的密闭玻璃球浸泡在热水中
红棕色变深
反应 的
D
向 饱和溶液中滴入足量浓氨水,并加热至刚好沸腾
得到红褐色透明液体
得到 胶体
A、A B、B C、C D、D7. 常温下,向 浓度均为 和 的混合溶液中滴加 的 ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 的关系如图所示(忽略混合时体积变化),下列说法正确的是( ) A、常温下, 的 比同浓度 的 大 B、 过程中水的电离程度先减小后增大 C、 点溶液中, D、 点时,
A、常温下, 的 比同浓度 的 大 B、 过程中水的电离程度先减小后增大 C、 点溶液中, D、 点时,二、工业流程
-
8. 硫酸镍广泛应用于电镀、电池、催化剂等工业。某科研小组以粗硫酸镍(含 等)为原料,经如图一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。
 (1)、滤渣1的主要成分是(写化学式),写出“硫化除铜”过程生成含铜物质反应的离子方程式。(2)、“氧化除杂”时加入 和 的主要作用是。(3)、已知 时, ; 。则“氟化除杂”过后滤液3中 。(4)、“萃取”时使用萃取剂 在硫酸盐中对某些金属离子的萃取率与溶液 的关系如图。则实验时需控制的 适宜范围是_____(填字母序号)。
(1)、滤渣1的主要成分是(写化学式),写出“硫化除铜”过程生成含铜物质反应的离子方程式。(2)、“氧化除杂”时加入 和 的主要作用是。(3)、已知 时, ; 。则“氟化除杂”过后滤液3中 。(4)、“萃取”时使用萃取剂 在硫酸盐中对某些金属离子的萃取率与溶液 的关系如图。则实验时需控制的 适宜范围是_____(填字母序号)。 A、1~2 B、3~4 C、4~5 D、5~6(5)、将萃取后所得富含硫酸镍的溶液经操作A可得硫酸镍晶体,则操作A为、、过滤、洗涤等。(6)、称取 硫酸镍晶体( )样品溶解,定容至 。取 试液,用 的 标准溶液滴定至终点。重复实验,平均消耗 标准溶液体积为 。反应为 。计算样品纯度为。(不考虑杂质反应)
A、1~2 B、3~4 C、4~5 D、5~6(5)、将萃取后所得富含硫酸镍的溶液经操作A可得硫酸镍晶体,则操作A为、、过滤、洗涤等。(6)、称取 硫酸镍晶体( )样品溶解,定容至 。取 试液,用 的 标准溶液滴定至终点。重复实验,平均消耗 标准溶液体积为 。反应为 。计算样品纯度为。(不考虑杂质反应)三、实验题
-
9. 某小组探究 溶液和 溶液的反应原理。(1)、(实验一)将含淀粉的 溶液加入 酸性溶液(过量)中,混合后约5秒内无明显变化,随后有少量蓝色出现并迅速变蓝。
溶液变蓝,说明 具有性。
(2)、查阅文献:反应Ⅰ: 慢
反应Ⅱ: _=_+_ 较快
反应Ⅲ: 快
写出酸性条件下,反应Ⅱ的离子方程式。
(3)、向实验一所得蓝色溶液中加入少量 溶液,蓝色迅速褪去,后又变蓝色。据此得出 氧化性比 强,该结论(填“合理”或“不合理”),理由是。(4)、为了进一步研究 溶液和 溶液的反应原理,设计如下实验。(实验二)装置如图所示, 闭合后,电流表的指针偏转情况记录如表:
表盘


时间/min
偏转位置
右偏至“Y”处
指针回到“0”处,又返至“X”处;如此周期性往复多次……
指针归零
① 闭合后,检验b极附近溶液存在放电产物 的实验操作是。
② 时,直接向a极区滴加淀粉溶液,溶液未变蓝。取a极附近溶液于试管中,滴加淀粉溶液,溶液变蓝。判断 在a极放电的产物是。
(5)、下列关于上述实验解释合理的是__________(填字母序号)。A、实验一中:5秒内无明显变化,可能是因为反应Ⅰ的活化能太小,反应速率太慢 B、实验二中:指针回到“0”处,可能是因为反应Ⅱ比反应Ⅰ快,导致 难与 发生反应 C、实验二中:又返至“X”处,可能是因为发生了反应Ⅲ,重新形成了原电池四、综合题
-
10. 甲醇是一种可再生能源,具有广阔的开发和应用前景,可用 等作为催化剂,采用如下反应来合成甲醇:(1)、下表是有关化学键的键能数据,计算表中的a=。
化学键
键能
436
462.8
a
1075
351
(2)、将 的混合气体,匀速通过装有催化剂的反应器反应(如图甲),反应器温度变化与从反应器排出气体中 的体积分数φ关系如图乙,φ(CH3OH)变化的原因是。 (3)、某学习小组模拟工业合成甲醇的反应,在 的恒容密闭容器内充入 和 ,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如表:
(3)、某学习小组模拟工业合成甲醇的反应,在 的恒容密闭容器内充入 和 ,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如表:反应时间/min
0
5
10
15
20
25
压强/MPa
12.6
10.8
9.5
8.7
8.4
8.4
从反应开始到 时, 的平均反应速率为 , 该温度下的平衡常数 为。
(4)、另将 和 加入密闭容器中,在一定条件下发生上述反应。平衡时 的体积分数(%)与温度和压强的关系如图所示(虚线框表示没有测定该条件下的数据)。
由大到小的关系是 , 判断理由是。
11. 铁、铜及其化合物应用广泛。回答下列问题:(1)、基态铁原子核外最后一个电子填充在(填能级符号),含有个成单电子,具有磁性。(2)、铁氰化钾 是检验 的重要试剂。①铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为。
②铁氰化钾中,不存在(填字母标号)。
A.离子键 B.σ键 C.π键 D.氢键 E.金属键
(3)、血蓝蛋白是某些节肢动物体内能与氧气可逆结合的一种铜蛋白,其部分结构示意图如图。其中 的化合价为价, 的杂化类型是。 (4)、 合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成 合金的晶体结构图。在这种结构中,同一层的 距离为 。
(4)、 合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成 合金的晶体结构图。在这种结构中,同一层的 距离为 。
① 合金中 。
②同一层中, 原子之间的最短距离是 ,设 为阿伏加德罗常数的值,若要求算 晶体的密度,还需要知道的物理量是(钙、铜元素的相对原子质量为已知量)。
五、推断题
-
12. 美托洛尔可用于治疗高血压及心绞痛,某合成路线如图:
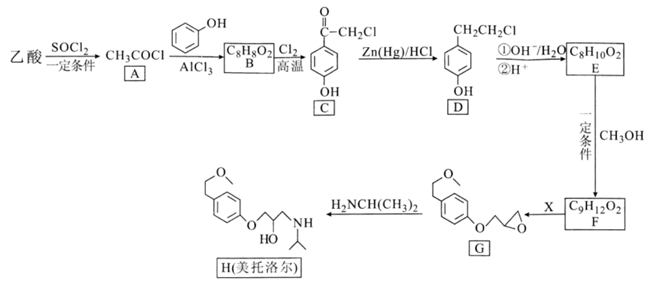
回答下列问题:
(1)、已知常温下, (氯化亚砜)是一种有强烈刺激气味发烟液体,遇水水解,加热分解。下列关于乙酸制备A的实验表述正确的是(填字母序号)。a.该实验常采用浓的醋酸溶液与过量 反应以提高产率
b.反应控制在较高温度下,并加入催化剂加快反应速率
c.反应产物中有污染性气体,需在通风厨中进行,且要吸收尾气
d.该反应有机副产物少、产品易分离,且产率较高。
(2)、C中含氧官能团的名称是。(3)、A→B的反应类型是 , D的分子式为。(4)、反应E→F的化学方程式为。(5)、试剂X的分子式为 ,则X的结构简式为 , X的同分异构体中含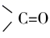 的有种。 (6)、4-苄基苯酚(
的有种。 (6)、4-苄基苯酚(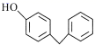 )是一种药物中间体,请设计以苯甲酸和苯酚为原料制备4-苄基苯酚的合成路线:(无机试剂任用)。
)是一种药物中间体,请设计以苯甲酸和苯酚为原料制备4-苄基苯酚的合成路线:(无机试剂任用)。
-
-