广东省广州市荔湾2020年中考化学模拟试卷
试卷更新日期:2020-07-07 类型:中考模拟
一、选择题
-
1. 广州市居民生活垃圾分为可回收物、餐厨垃圾、有害垃圾、其他垃圾四类。下列选项是放入“可回收”垃圾桶的物品,其成分属于有机合成材料的是( )A、金属罐
 B、塑料瓶
B、塑料瓶  C、玻璃瓶
C、玻璃瓶  D、快递纸箱
D、快递纸箱  2. 化学与人类健康密切相关。下列说法正确的是( )A、食用肉类和牛奶可补充维生素C B、发霉的大米煮熟后可以食用 C、禁止使用甲醛溶液浸泡海鲜产品 D、缺钙会引起甲状腺肿大3. 空气是一种宝贵的资源,下列有关空气的说法正确的是( )A、空气是由空气分子构成的 B、空气中各成分不再保持各自的化学性质 C、稀有气体化学性质不活泼,不与任何物质发生反应 D、氮气可用于填充食品包装起到防腐作用4. 下列过程中,发生了化学变化的是( )A、干冰升华 B、使用熟石灰改良酸性土壤 C、浓盐酸挥发 D、分离液态空气制取氧气5. 下列实验操作正确的是( )A、稀释浓硫酸
2. 化学与人类健康密切相关。下列说法正确的是( )A、食用肉类和牛奶可补充维生素C B、发霉的大米煮熟后可以食用 C、禁止使用甲醛溶液浸泡海鲜产品 D、缺钙会引起甲状腺肿大3. 空气是一种宝贵的资源,下列有关空气的说法正确的是( )A、空气是由空气分子构成的 B、空气中各成分不再保持各自的化学性质 C、稀有气体化学性质不活泼,不与任何物质发生反应 D、氮气可用于填充食品包装起到防腐作用4. 下列过程中,发生了化学变化的是( )A、干冰升华 B、使用熟石灰改良酸性土壤 C、浓盐酸挥发 D、分离液态空气制取氧气5. 下列实验操作正确的是( )A、稀释浓硫酸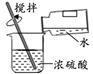 B、取用液体
B、取用液体 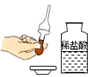 C、测溶液pH
C、测溶液pH 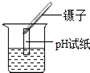 D、读出液体的体积
D、读出液体的体积 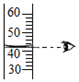 6. 下图为某反应的微观示意图,下列说法错误的是( )
6. 下图为某反应的微观示意图,下列说法错误的是( )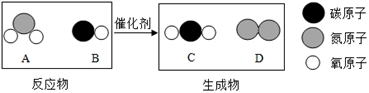 A、图示中共有4种分子 B、该反应属于置换反应 C、该反应符合质量守恒定律 D、图示中反应物都是化合物7. 常温下,下列物质水溶液的pH>7的是( )A、橘汁 B、白醋 C、氨水 D、食盐8. 如右图所示,试管中盛有无色溶液a,将气球中的固体b倒入溶液a中,观察气球胀大。a、b不可能是( )
A、图示中共有4种分子 B、该反应属于置换反应 C、该反应符合质量守恒定律 D、图示中反应物都是化合物7. 常温下,下列物质水溶液的pH>7的是( )A、橘汁 B、白醋 C、氨水 D、食盐8. 如右图所示,试管中盛有无色溶液a,将气球中的固体b倒入溶液a中,观察气球胀大。a、b不可能是( )
选项
a
b
A
H2O
NH4NO3
B
H2O
CaO
C
稀H2SO4
Zn
D
稀HCl
NaHCO3
A、A B、B C、C D、D9. 物质的性质决定物质的用途。下列说法错误的是( )A、锰钢韧性好,硬度大,可用于钢轨、自行车架子等 B、氢氧化钠具有吸水性,可用作某些气体的干燥剂 C、氧气具有助燃性,可用作燃料 D、稀盐酸能与金属氧化物反应,可用于金属表面除锈10. “归纳”是化学学习的重要方法,下列有关CO的知识归纳错误的是( )A、组成:一氧化碳是由碳元素和氧元素组成的。 B、性质:无色无味的气体,能溶于水,与水发生反应。 C、用途:CO可用作气体燃料、冶炼金属的还原剂。 D、危害:CO极易与血液中的血红蛋白结合引起中毒11. 化学与社会发展紧密相连,与生活息息相关。下列说法正确的是( )A、扑灭森林火灾时开辟隔离带,是为了清除和隔离可燃物 B、炒菜时油锅着火,应立即用水浇灭 C、石油是一种清洁能源,也是一种可再生能源 D、“钻木取火”的原理是通过摩擦生热提高木材的着火点12. 化肥和农药对提高农产品的产量有重要作用。下列关于说法正确的是( )A、NaNO3属于复合肥 B、残留农药可通过农作物转移到人体中 C、铵态氮肥可以与碱性物质混合使用 D、农药本身有毒,应该禁止施用农药13. 防疫关键时刻,少出门、不聚餐、多通风、勤洗手。某免洗消毒洗手液原理是洗手液中的乙醇、银离子等起到杀菌作用,甘油(C3H8O3)等起到护肤作用。下列关于甘油(C3H8O3)的说法正确的是( )A、甘油属于氧化物 B、甘油由14个原子构成 C、甘油中氧元素的质量分数为×100% D、甘油中碳元素、氢元素和氧元素的质量比为3:8:314. 下图为KNO3的溶解度曲线,a、b在溶解度曲线上。下列有关结论错误的是( )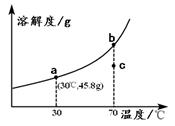 A、a点表示30℃时,硝酸钾的溶解度为45.8g B、a点对应的溶液的质量分数是 C、c点表示70℃时硝酸钾的不饱和溶液 D、欲使KNO3溶液的状态从b点转化为c点,可采取降低温度的措施15. 下列关于水的说法正确的是( )A、活性炭可以使硬水转化为软水 B、天然水经过沉淀、过滤、吸附、消毒等处理后得到水是纯净物 C、用汽油或加了洗涤剂的水都能除去衣服上的油污 D、pH<7的酸性降水称为酸雨,它的形成与大气中SO2有关16. 下列物质混合后能够反应,且有明显现象的是( )A、氯化镁与氢氧化钠溶液 B、氢氧化钡溶液与稀盐酸 C、铜与硝酸铝溶液 D、稀硫酸与氯化钠溶液17. 下图是元素X的一种粒子的结构示意图,下列说法错误的是( )
A、a点表示30℃时,硝酸钾的溶解度为45.8g B、a点对应的溶液的质量分数是 C、c点表示70℃时硝酸钾的不饱和溶液 D、欲使KNO3溶液的状态从b点转化为c点,可采取降低温度的措施15. 下列关于水的说法正确的是( )A、活性炭可以使硬水转化为软水 B、天然水经过沉淀、过滤、吸附、消毒等处理后得到水是纯净物 C、用汽油或加了洗涤剂的水都能除去衣服上的油污 D、pH<7的酸性降水称为酸雨,它的形成与大气中SO2有关16. 下列物质混合后能够反应,且有明显现象的是( )A、氯化镁与氢氧化钠溶液 B、氢氧化钡溶液与稀盐酸 C、铜与硝酸铝溶液 D、稀硫酸与氯化钠溶液17. 下图是元素X的一种粒子的结构示意图,下列说法错误的是( )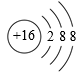 A、X的核外电子数为18 B、X属于非金属元素 C、该粒子可表示为X2+ D、该粒子最外层电子层已经达到相对稳定结构18. 现有X,Y,Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化,根据以上实验事实,可以判断三种金属的活动性顺序是( )A、Z>X>Y B、Z>Y>X C、Y>Z>X D、X>Y>Z19. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )A、CaCO3固体(CaO固体):高温煅烧 B、KCl溶液(CaCl2溶液):滴加过量碳酸钾溶液后过滤 C、CO2气体(CO气体):通过足量的氢氧化钠溶液 D、N2气体(O2气体):通过灼热的铜网20. 下列实验中,现象正确且可得到相应结论的是( )
A、X的核外电子数为18 B、X属于非金属元素 C、该粒子可表示为X2+ D、该粒子最外层电子层已经达到相对稳定结构18. 现有X,Y,Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化,根据以上实验事实,可以判断三种金属的活动性顺序是( )A、Z>X>Y B、Z>Y>X C、Y>Z>X D、X>Y>Z19. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )A、CaCO3固体(CaO固体):高温煅烧 B、KCl溶液(CaCl2溶液):滴加过量碳酸钾溶液后过滤 C、CO2气体(CO气体):通过足量的氢氧化钠溶液 D、N2气体(O2气体):通过灼热的铜网20. 下列实验中,现象正确且可得到相应结论的是( )实验操作
现象
结论
A
把燃着的木条插入某瓶无色气体中
木条熄灭
瓶中的气体是CO2
B
往久置于空气中的氢氧化钠溶液中滴加稀盐酸
有气泡产生
氢氧化钠溶液已变质
C
往某无色溶液中滴加氯化钡溶液
有白色沉淀生成
无色溶液中一定含有SO42-
D
点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯
烧杯内壁有无色液滴产生
该气体是CH4
A、A B、B C、C D、D二、非选择题
-
21. 硅元素在地壳中的含量仅次于氧元素,其化学性质与碳元素有相似的地方。硅主要用来制作高纯半导体(芯片、CPU等)、耐高温材料、光导纤维通信材料、有机硅化合物、合金等,广泛应用于航空航天、电子电气、建筑、运输、能源、化工、纺织、食品、轻工、医疗、农业等行业。
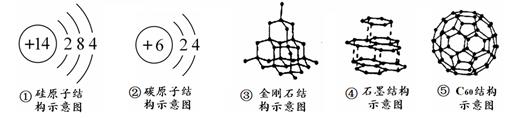
根据所学知识和上图所示的信息,回答问题:
(1)、化学上“Si”能表示硅元素,表示一个硅原子,还能表示;硅元素化学性质与碳元素相似的原因是;
硅元素和氯元素组成的化合物的化学式为。
(2)、石墨在一定条件下可以转化为金刚石,这个变化属于化学反应。这个反应的微观解释是。(3)、1993年,结构和性能与C60相似的Si60诞生了,Si60的硬度超过了金刚石的硬度。下列关于Si60的说法不正确的是 。A、它是由分子构成的物质 B、它的一个分子中含有60个原子 C、相对分子质量是1680 D、它是含硅的化合物22. 稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属铈是一种银灰色的金属,粉末在空气中易自燃,能与稀硫酸反应,生成硫酸铈,其水溶液为微红色。铈元素在周期表的相关信息如图所示。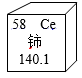 (1)、铈原子的核内中子数为;(2)、铈与稀硫酸反应,产物中铈元素化合价为+3,反应的化学方程式为 , 反应的现象为。(3)、硝酸铈铵,分子式为(NH4)2Ce (NO3)6 , 常用作氧化剂用于电路腐蚀及生产其它含铈化合物。(NH4)2Ce(NO3)6中Ce元素的化合价为。23. 有一包白色固体混合物样品,可能含有NaCl、Na2CO3、Ba(NO3)2、Na2SO4等物质中的一种或几种,为确定其组成,进行如下实验:
(1)、铈原子的核内中子数为;(2)、铈与稀硫酸反应,产物中铈元素化合价为+3,反应的化学方程式为 , 反应的现象为。(3)、硝酸铈铵,分子式为(NH4)2Ce (NO3)6 , 常用作氧化剂用于电路腐蚀及生产其它含铈化合物。(NH4)2Ce(NO3)6中Ce元素的化合价为。23. 有一包白色固体混合物样品,可能含有NaCl、Na2CO3、Ba(NO3)2、Na2SO4等物质中的一种或几种,为确定其组成,进行如下实验:步骤I:取少量混合物加足量的水充分搅拌,有白色不溶物生成,过滤;
步骤II:在滤出的白色不溶物中,加入足量的盐酸,白色不溶物全部溶解;
步骤III:在步骤II所得的溶液中,加入硝酸银溶液,生成白色沉淀,再加入稀硝酸经振荡沉淀不溶解。
根据上述实验现象,回答问题:
(1)、写出步骤I中反应的化学方程式 , 步骤II中发生的反应属于(填反应类型)。(2)、步骤III中反应前后溶液中的主要离子变化如右图所示,则 代表的离子是(填符号)。
代表的离子是(填符号)。 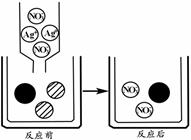 (3)、分析上述实验过程,关于样品的组成,可以得到的结论:肯定没有 , 可能含有。(4)、上述实验中,没有必要做的实验是步骤。(5)、为确定样品的组成,继续进行的实验操作是。24. 某同学在实验室进行实验研究化学反应速率的影响因素。(1)、研究催化剂对化学反应速率的影响,进行如下的实验:
(3)、分析上述实验过程,关于样品的组成,可以得到的结论:肯定没有 , 可能含有。(4)、上述实验中,没有必要做的实验是步骤。(5)、为确定样品的组成,继续进行的实验操作是。24. 某同学在实验室进行实验研究化学反应速率的影响因素。(1)、研究催化剂对化学反应速率的影响,进行如下的实验:步骤Ⅰ:向3支大小相同的试管abc中加入相同体积(2mL)5%H2O2溶液;
步骤Ⅱ:向试管a中加入少量MnO2粉末,向试管b中滴加1~2滴10%FeCl3溶液。
得出实验结论:MnO2和FeCl3均能加快H2O2的分解速率,均作催化剂,且前者的催化效率高得多。
回答问题:
①步骤I中分别向3支试管中加入相同体积的溶液的目的是。
②设计试管c的作用是。
③若继续用上述实验药品研究温度对H2O2分解速率的影响,为了便于观察,你选择的催化剂和选择它的原因是。
(2)、现提供下列实验用品,来研究影响化学反应速率的因素。实验仪器:试管、烧杯、量筒、天平、秒表;
实验药品:铝片、铝粉、5%盐酸、15%盐酸、冷/热水;
①利用所提供实验用品,研究的化学反应速率的影响因素是。
②请使用上面提供的实验用品,设计实验完成温度对化学反应速率的影响,说明实验步骤(文字表述、图示均可)。
25. 氯化铜晶体(CuCl2·2H2O,为结晶水合物,分子里的水,称为结晶水)常用作玻璃、陶瓷着色剂和饲料添加剂等。它在潮湿空气中易潮解,易溶于水,溶于乙醇,受热容易失去结晶水。一种以辉铜矿石为原料制备CuCl2·2H2O晶体的工艺流程如下:
查阅相关资料得知:
①辉铜矿主要含有硫化亚铜(Cu2S)、还有Fe2O3、SiO2及一些不溶性杂质。
②常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
金属离子
Fe3+
Cu2+
氢氧化物开始沉淀时的pH
1.9
4.7
氢氧化物完全沉淀时的pH
3.2
6.7
回答问题:
(1)、焙烧前需要将辉铜矿进行粉碎,粉碎的目的是;(2)、高温焙烧中有黑色固体生成,反应的化学方程式为。(3)、焙烧时产生的二氧化硫对环境有污染,可以使用溶液来吸收。(4)、滤液1中加入试剂X可以调节溶液pH ,控制pH的取值范围为(填不等式),从而除去Fe3+而不引入杂质。试剂X可选用下列物质中的 (填字母)A.CaO B.NaOH C.Cu D.Cu(OH)2
(5)、操作a包含蒸发浓缩、降温结晶、过滤、洗涤。洗涤CuCl2晶体时,用乙醇代替蒸馏水的目的是。(6)、用含Cu2S 80%的辉铜矿a吨,按上述流程最少可制得CuCl2·2H2O的质量为吨(列出算式即可。已知CuCl2·2H2O的相对分子质量为171)。三、本题包括4小题,共30分
-
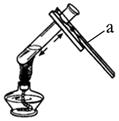
26. 下图是初中化学的两个实验装置。
A
 B
B 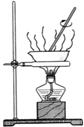 (1)、A为给试管中的液体加热,仪器a的名称是;仪器a的使用方法是。(2)、B是实验室粗盐提纯的蒸发操作,当时,停止加热;蒸发时,玻璃棒搅拌的作用是。27. 下面是实验室制取气体的相关装置图,回答下列问题。
(1)、A为给试管中的液体加热,仪器a的名称是;仪器a的使用方法是。(2)、B是实验室粗盐提纯的蒸发操作,当时,停止加热;蒸发时,玻璃棒搅拌的作用是。27. 下面是实验室制取气体的相关装置图,回答下列问题。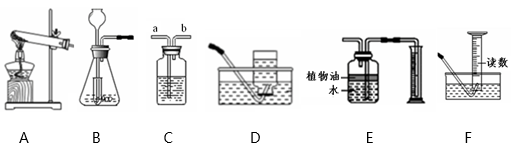 (1)、实验室选择AD的组合装置用高锰酸钾制取氧气,反应的化学方程式为 , 在反应物充足,外焰加热的情况下产生了气泡,一段时间后反应停止了,没有气体产生,此时,应 , 使反应继续进行。(2)、实验室用大理石和稀盐酸制取二氧化碳气体,用E装置来测量生成CO2的体积,在水面上放一层植物油的作用是。(3)、B装置中使用小试管的好处是 , C装置可以收集和储备氢气,若用水将装置中的氢气排出,水应从(填“a”或“b”) 端通入。(4)、用AF组合装置来测定参加反应的KClO3的质量分数。若读数时俯视液面,则录得的实验结果(选填 “偏大”、“偏小”或“无误差”)。28. 某化学小组需要用到质量分数为10%的氢氧化钠溶液来做实验,但实验室的氢氧化钠刚好用完。同学们提出用熟石灰与碳酸钠反应制取氢氧化钠,再配成溶液来做实验。
(1)、实验室选择AD的组合装置用高锰酸钾制取氧气,反应的化学方程式为 , 在反应物充足,外焰加热的情况下产生了气泡,一段时间后反应停止了,没有气体产生,此时,应 , 使反应继续进行。(2)、实验室用大理石和稀盐酸制取二氧化碳气体,用E装置来测量生成CO2的体积,在水面上放一层植物油的作用是。(3)、B装置中使用小试管的好处是 , C装置可以收集和储备氢气,若用水将装置中的氢气排出,水应从(填“a”或“b”) 端通入。(4)、用AF组合装置来测定参加反应的KClO3的质量分数。若读数时俯视液面,则录得的实验结果(选填 “偏大”、“偏小”或“无误差”)。28. 某化学小组需要用到质量分数为10%的氢氧化钠溶液来做实验,但实验室的氢氧化钠刚好用完。同学们提出用熟石灰与碳酸钠反应制取氢氧化钠,再配成溶液来做实验。下表是氢氧化钙和氢氧化钠的溶解度数据
温度/℃
0
20
40
60
80
100
溶解度
(g/100gH2O)
氢氧化钙
0.19
0.17
0.14
0.12
0.09
0.08
氢氧化钠
31
90
111
129
313
336
请回答问题:
(1)、制备氢氧化钠。写出制取氢氧化钠反应的化学方程式。反应后过滤,蒸发结晶得到固体氢氧化钠。小明提出这样制得的氢氧化钠可能含有少量杂质,其理由是。
(2)、提纯氢氧化钠。将上述制得的氢氧化钠(含少量氢氧化钙)在60℃时配成饱和溶液,降温、结晶、过滤,对滤渣和滤液成分的分析,正确的是________(双选)。A、滤渣中只有氢氧化钠 B、滤渣中主要是氢氧化钠,可能有少量氢氧化钙 C、滤液中一定有氢氧化钙,可能有氢氧化钠 D、滤液中一定有氢氧化钠和氢氧化钙 E、滤液中只有氢氧化钙(3)、配制氢氧化钠溶液。配制50克10%氢氧化钠溶液,需要氢氧化钠固体的质量为g,称取时必须将氢氧化钠固体放在里进行称量。(4)、进行实验。完全中和40g上述配得的氢氧化钠溶液,用去了稀硫酸的质量为20克,则稀硫酸的质量分数为(精确到0.1%)29. 食醋的主要成分为醋酸,醋酸又称为乙酸,化学式为CH3COOH,通常简写为HAc。(1)、在厨房烹饪鱼时,常常会加入少许食醋和酒(主要成分为乙醇,C2H5OH),一方面可以消除鱼的腥味,另一方面,加热会使乙醇和乙酸发生化学反应,生成一种有果香味的称为乙酸乙酯(CH3COOC2H5)的物质和另一种常见的物质,以增强菜肴的香味,其反应的化学方程式为。(2)、请根据你所学的知识,推测醋酸还具有的其他化学性质,说明预测的依据,并设计实验加以验证。查阅资料,醋酸及其一些盐的相关性质如下:
物质
HAc
NaAc
Ca(Ac)2
Ba(Ac)2
Cu(Ac)2
在水中
的溶解性
溶于水,有剌激性气味
溶于水成无色溶液
溶于水成无色溶液
溶于水成无色溶液
溶于水成蓝色溶液
限选试剂是:醋酸溶液、BaCl2溶液、CaCO3粉末、稀盐酸、酚酞溶液、紫色石蕊溶液、镁条、碳粉、氧化铜粉末。
预测
预测的依据
验证预测的实验操作与预期现象
①能够与碳酸盐反应
取少量醋酸溶液于试管中,加入CaCO3粉末,振荡,若观察到 , 则预测成立。
②能够与 (填物质类别)反应
取少量醋酸溶液于试管中, , 若观察到 , 则预测成立。
③能够与 (填物质类别)反应
取少量醋酸溶液于试管中, , 若观察到 , 则预测成立。