四川省南充市2020年中考化学模拟试卷
试卷更新日期:2020-07-01 类型:中考模拟
一、单选题
-
1. 近期,全球爆发了新型冠状病毒感染的肺炎疫情,在疫情防控中有许多措施都与化学息息相关。下列措施或现象不涉及化学变化的是( )A、为了达到理想的消毒效果,用水将酒精稀释成合理的浓度 B、制药厂将原料进行加工提炼,合成抗病毒药物达芦那韦 C、石油催化裂解制得丙烯,利用丙烯生产口罩中的熔喷布 D、新冠病毒在被感染的宿主细胞中不断增殖,加速疾病的发展2. 保护水资源包含“节水”和“防污”两个环节。我国将2020年世界水日的中国主题设立为“坚持节水优先,建设幸福河湖”,下列措施不利于“节水优先”原则的是( )A、农业上大力普及喷灌、微灌等节水灌溉技术 B、工业在可能的范围内将水循环使用 C、衣服集中洗涤,减少洗衣次数 D、将喷头洗浴改为浴缸泡浴3. 化学是一门以实验为基础的自然科学。下列实验操作正确的是( )A、
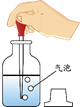 吸取液体药品
B、
吸取液体药品
B、 固体NaCl的称量
C、
固体NaCl的称量
C、 放置一瓶集满的二氧化碳
D、
放置一瓶集满的二氧化碳
D、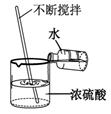 浓硫酸的稀释
4. 近期,我省西昌泸山自然保护区等多地突发森林火灾。掌握化学知识有利于避免火灾的发生,森林里发生的以下现象不易引发大火的是( )A、空气干燥地表温度较高 B、地面堆集着厚厚的枯枝落叶层 C、茂密的植被进行呼吸 D、雷击高耸枯枝5. 碳酸氢铵(NH4HCO3)是一种常见氮肥,极不稳定,常温下就会分解生成水、二氧化碳和一种有刺激性气味的气体,该气体可能是( )A、N2 B、SO2 C、CO D、NH36. 下列对九年级常见化学演示实验的现象描述错误的是( )A、红磷在空气中燃烧产生大量白雾 B、氢氧化钠固体暴露在空气中表面变潮湿并逐渐溶解 C、高温加热碳与氧化铜的混合物,固体由黑色变成红色 D、铜丝放入硝酸银溶液中,铜丝上慢慢附着银白色固体,溶液由无色逐渐变成蓝色7. 分类是认识自然界的常用方法。下列物质的分类错误的是( )A、Hg—非金属单质 B、H2O—氧化物 C、NaHCO3—盐 D、H2SO4—酸8. 如图是教材中水分子分解示意图,其中
浓硫酸的稀释
4. 近期,我省西昌泸山自然保护区等多地突发森林火灾。掌握化学知识有利于避免火灾的发生,森林里发生的以下现象不易引发大火的是( )A、空气干燥地表温度较高 B、地面堆集着厚厚的枯枝落叶层 C、茂密的植被进行呼吸 D、雷击高耸枯枝5. 碳酸氢铵(NH4HCO3)是一种常见氮肥,极不稳定,常温下就会分解生成水、二氧化碳和一种有刺激性气味的气体,该气体可能是( )A、N2 B、SO2 C、CO D、NH36. 下列对九年级常见化学演示实验的现象描述错误的是( )A、红磷在空气中燃烧产生大量白雾 B、氢氧化钠固体暴露在空气中表面变潮湿并逐渐溶解 C、高温加热碳与氧化铜的混合物,固体由黑色变成红色 D、铜丝放入硝酸银溶液中,铜丝上慢慢附着银白色固体,溶液由无色逐渐变成蓝色7. 分类是认识自然界的常用方法。下列物质的分类错误的是( )A、Hg—非金属单质 B、H2O—氧化物 C、NaHCO3—盐 D、H2SO4—酸8. 如图是教材中水分子分解示意图,其中 表示氧原子,
表示氧原子, 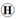 表示氢原子,根据示意图能得到的正确结论是( )
表示氢原子,根据示意图能得到的正确结论是( ) 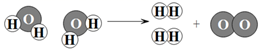 A、该反应属于化合反应 B、水分解过程中氢、氧原子的个数不会改变 C、水分子是该化学变化中的最小微粒 D、水分子由氢分子和氧原子构成9. 小梅同学设计的下列实验方案中,不能达到目的是( )A、用肥皂水区分硬水和软水 B、用加熟石灰研磨闻气味的方法来区分硫酸铵和硫酸钾 C、利用洗涤剂溶解油污 D、利用硝酸铵溶于水来降低溶液温度10. 科学的归纳推理可以由点到面得到普遍存在的规律。以下推理所得规律正确的是( )A、某碳原子的原子核里有6个质子和6个中子,则所有原子中质子数与中子数都相等 B、碳酸钙与盐酸反应生成二氧化碳,则可溶性碳酸盐与盐酸反应都可能生成二氧化碳 C、稀盐酸和氢氧化钠溶液中和时无明显现象,则所有酸碱中和反应都没有明显现象 D、镁、锌可以置换出硫酸铜溶液中的铜离子,则所有金属都可以置换出盐溶液中的铜离子11. 除去下列物质中的少量杂质,所选用的试剂和操作方法都适宜的是( )
A、该反应属于化合反应 B、水分解过程中氢、氧原子的个数不会改变 C、水分子是该化学变化中的最小微粒 D、水分子由氢分子和氧原子构成9. 小梅同学设计的下列实验方案中,不能达到目的是( )A、用肥皂水区分硬水和软水 B、用加熟石灰研磨闻气味的方法来区分硫酸铵和硫酸钾 C、利用洗涤剂溶解油污 D、利用硝酸铵溶于水来降低溶液温度10. 科学的归纳推理可以由点到面得到普遍存在的规律。以下推理所得规律正确的是( )A、某碳原子的原子核里有6个质子和6个中子,则所有原子中质子数与中子数都相等 B、碳酸钙与盐酸反应生成二氧化碳,则可溶性碳酸盐与盐酸反应都可能生成二氧化碳 C、稀盐酸和氢氧化钠溶液中和时无明显现象,则所有酸碱中和反应都没有明显现象 D、镁、锌可以置换出硫酸铜溶液中的铜离子,则所有金属都可以置换出盐溶液中的铜离子11. 除去下列物质中的少量杂质,所选用的试剂和操作方法都适宜的是( )选项
物质
杂质
试剂
操作方法
A
CO2
CO
——
点燃
B
Cu
Fe
过量的硫酸铜溶液
过滤、蒸发
C
KCl固体
KClO3
-----
充分加热、溶解、过滤、蒸发
D
NaCl溶液
Na2SO4
过量的氯化钡溶液
过滤
A、A B、B C、C D、D12. 下列示意图能正确反映对应关系的是( )A、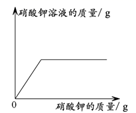 为20℃时,向不饱和的硝酸钾溶液中加入硝酸钾
B、
为20℃时,向不饱和的硝酸钾溶液中加入硝酸钾
B、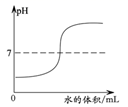 为在稀硫酸中不断加水,溶液pH的变化
C、
为在稀硫酸中不断加水,溶液pH的变化
C、 为密闭容器中等质量的硫和氧气完全燃烧
D、
为密闭容器中等质量的硫和氧气完全燃烧
D、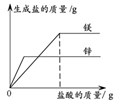 为等质量的镁、锌分别与足量的相同溶质质量分数的稀盐酸反应
为等质量的镁、锌分别与足量的相同溶质质量分数的稀盐酸反应
二、填空题
-
13. 南方黑芝麻糊具有浓郁的香味是营养丰富的传统美食, 其营养成分如表所示。根据芝麻糊的营养成分,回答:(1)、黑芝麻糊中的钠、钙、铁是指(填“原子”或“元素”),它们能否为人体提供能量(填“能”或“否”)。(2)、黑芝麻糊的塑料包装袋属于_____(填序号)。A、天然材料 B、金属材料 C、合成材料 D、复合材料(3)、营养成分中钙元素的原子结构示意图和元素周期表的信息如图所示。根据信息推测,钙元素位于元素周期表第周期,钙原子的质子数为 , 它在化学变化中易(填“得”或“失”)电子,形成的钙离子符号为。
 14. 随着中国经济的高速发展,老百姓过去“盼温饱”现在“盼环保”,尤其对干净的水、清新的空气期盼值越来越高。(1)、某自来水厂常采用沉降、吸附、过滤、消毒等净水措施。木炭、活性炭都能用于吸附,它们的吸附性属于性质(填“物理”或“化学”)。消毒使用的ClO2是一种安全、高效的消毒剂,标出ClO2中氯元素的化合价 , 实验室制取ClO2的化学方程式如下:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+X,其中X的化学式是。生活中饮用自来水之前我们常采用的方法来杀菌并降低水的硬度。(2)、绿色环保要求工业减少“三废”的排放。工业废气中SO2会造成硫酸型酸雨,酸雨是指pH小于的雨水,酸雨会导致土壤酸化不利于植物的生长。工业常使用氢氧化钠溶液来除去SO2 , 写出发生反应的化学方程式 , 农业常使用改良酸性土壤。15. 生活在盐湖附近的人们习惯“冬天捞碱,夏天晒盐”。(1)、这里的“碱”是指碳酸钠,俗名为 , 这里的“盐”的主要成分为氯化钠。(2)、如图为碳酸钠和氯化钠的溶解度曲线,根据曲线回答问题:两条溶解度曲线中代表氯化钠的是(填“A”或“B”)。碳酸钠、氯化钠在温度为时溶解度相等,都等于g。
14. 随着中国经济的高速发展,老百姓过去“盼温饱”现在“盼环保”,尤其对干净的水、清新的空气期盼值越来越高。(1)、某自来水厂常采用沉降、吸附、过滤、消毒等净水措施。木炭、活性炭都能用于吸附,它们的吸附性属于性质(填“物理”或“化学”)。消毒使用的ClO2是一种安全、高效的消毒剂,标出ClO2中氯元素的化合价 , 实验室制取ClO2的化学方程式如下:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+X,其中X的化学式是。生活中饮用自来水之前我们常采用的方法来杀菌并降低水的硬度。(2)、绿色环保要求工业减少“三废”的排放。工业废气中SO2会造成硫酸型酸雨,酸雨是指pH小于的雨水,酸雨会导致土壤酸化不利于植物的生长。工业常使用氢氧化钠溶液来除去SO2 , 写出发生反应的化学方程式 , 农业常使用改良酸性土壤。15. 生活在盐湖附近的人们习惯“冬天捞碱,夏天晒盐”。(1)、这里的“碱”是指碳酸钠,俗名为 , 这里的“盐”的主要成分为氯化钠。(2)、如图为碳酸钠和氯化钠的溶解度曲线,根据曲线回答问题:两条溶解度曲线中代表氯化钠的是(填“A”或“B”)。碳酸钠、氯化钠在温度为时溶解度相等,都等于g。 (3)、在t1℃,把20gA放入50g水中,用玻璃棒搅拌,完全溶解后所得溶液的溶质质量分数为(计算结果精确到0.1%),玻璃棒搅拌的目的是。(4)、将等质量的A、B饱和溶液从t1℃升温到t2℃,溶液中水(不考虑水的蒸发)的质量是AB(填“大于”、或“小于”或“相等”)。16. 人类的生产和生活都离不开金属材料。(1)、为补充铁元素预防贫血,国际上提倡向中国人学习用铁锅炒菜。使用铁锅时需注意防止它与空气中的发生反应而生锈,举例说明防止家中铁锅生锈的一种方法。铁制品锈蚀后,工业、实验室都可以使用稀盐酸除锈(Fe2O3),写出稀盐酸除铁锈的化学方程式。(2)、如图是实验室模仿工业冶炼生铁的原理炼铁的装置图,该实验中必须的安全或环保措施有(任举一种),写出一氧化碳与氧化铁反应的化学方程式。
(3)、在t1℃,把20gA放入50g水中,用玻璃棒搅拌,完全溶解后所得溶液的溶质质量分数为(计算结果精确到0.1%),玻璃棒搅拌的目的是。(4)、将等质量的A、B饱和溶液从t1℃升温到t2℃,溶液中水(不考虑水的蒸发)的质量是AB(填“大于”、或“小于”或“相等”)。16. 人类的生产和生活都离不开金属材料。(1)、为补充铁元素预防贫血,国际上提倡向中国人学习用铁锅炒菜。使用铁锅时需注意防止它与空气中的发生反应而生锈,举例说明防止家中铁锅生锈的一种方法。铁制品锈蚀后,工业、实验室都可以使用稀盐酸除锈(Fe2O3),写出稀盐酸除铁锈的化学方程式。(2)、如图是实验室模仿工业冶炼生铁的原理炼铁的装置图,该实验中必须的安全或环保措施有(任举一种),写出一氧化碳与氧化铁反应的化学方程式。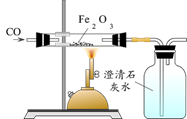 17. 自然资源部2020年3月26日公布:我国可燃冰试采创下两项世界纪录。可燃冰是由天然气与水在高压低温条件下形成的类冰状的结晶物质(主要成分化学式CH4·nH2O)。(1)、计算组成CH4的碳氢元素质量比。(2)、下列关于可燃冰的主要成分(CH4·nH2O)中各元素的质量分数,结论正确的是___。(填序号)A、碳元素的质量分数最大 B、氢元素的质量分数最大 C、氧元素的质量分数最大 D、各元素质量分数的大小关系无法确定
17. 自然资源部2020年3月26日公布:我国可燃冰试采创下两项世界纪录。可燃冰是由天然气与水在高压低温条件下形成的类冰状的结晶物质(主要成分化学式CH4·nH2O)。(1)、计算组成CH4的碳氢元素质量比。(2)、下列关于可燃冰的主要成分(CH4·nH2O)中各元素的质量分数,结论正确的是___。(填序号)A、碳元素的质量分数最大 B、氢元素的质量分数最大 C、氧元素的质量分数最大 D、各元素质量分数的大小关系无法确定三、科普阅读题
-
18. 阅读下面科普短文
近半年来,面对新型冠状病毒感染的肺炎疫情,除了戴口罩、勤洗手外,如何科学、正确、安全地消毒,成为了大家关注的话题。能有效杀灭新型冠状病毒常用方法有:56℃以上蒸煮30分钟,喷洒75%酒精、含氯消毒剂等。
对含氯消毒剂你了解多少呢?
含氯消毒剂是指溶于水能产生次氯酸(HClO)的消毒剂,次氯酸不稳定受热易分解。日常生活中,84 消毒液、漂白粉就属于常见的含氯消毒剂。
含氯消毒剂的杀菌威力来源于次氯酸根离子(ClO-)的氧化性,它能够使病原体的蛋白质氧化变性,反应后生成的氯离子又能显著改变病原体的渗透压,使病菌死亡。影响大多数消毒剂消毒效果的因素有:消毒剂的有效浓度、放置时间、温度、酸碱度等,一般规律是有效浓度愈高,放置时间愈短,温度愈高,杀菌效果愈好。
表1为酸碱度对消毒液有效氯浓度的影响。图1为消毒液的放置时间对杀菌效果的影响,图中消毒液1比消毒液2有效氯浓度低。
表1 84消毒液的酸碱度对有效氯浓度的影响
有效氯浓度(%)
pH
0时
15天
30天
45天
8
0.93
0.82
0.66
0.51
9
0.94
0.89
0.83
0.74
10
0.96
0.93
0.88
0.82
11
0.98
0.95
0.92
0.88
12
1.00
0.97
0.95
0.92
13
1.01
1.01
0.95
0.99

日常使用含氯消毒剂时,需要注意以下三点:①含氯消毒剂不能和洁厕灵同时使用,因为洁厕灵的主要成分是盐酸,它遇上含氯消毒剂中的次氯酸钠(NaClO)就会生成氯气(Cl2)、氯化钠和一种常见的氧化物,造成人体皮肤和黏膜损伤,严重的会出现肺水肿等症状。②原液需稀释后才能使用,稀释人员需要带好橡胶手套和防护眼镜。③不推荐和酒精混合后使用,可能会有潜在风险。
含氯消毒剂在日常生活中发挥着重要作用,我们要了解它、正视它才能合理正确地使用。
依据文章内容,回答下列问题。
(1)、次氯酸和75%酒精是否都是纯净物(填“是”、或“否”)。(2)、84消毒液的pH达时其有效氯浓度在45天内最稳定。(3)、含氯消毒剂的杀菌原理为。(4)、写出次氯酸钠与盐酸反应的化学反应方程式。(5)、下列关于含氯消毒剂的说法中,不合理的是_____。A、84消毒液不宜和酒精混合后使用 B、含有氯元素的消毒剂就是含氯消毒剂 C、含氯消毒剂使用时温度越高,杀菌效果越好 D、放置两个小时后,无论有效氯浓度高或低都不会影响杀菌率(6)、从使用的安全角度考虑,请你对使用含氯消毒剂提两条合理的建议: 。四、科学探究题
-
19. 化学实验小组开展活动,他们将在实验室完成两个主题实验。请你参与他们的活动:(1)、制取氧气。下图是他们准备选取的装置

①a仪器的名称。
②小文同学准备用过氧化氢溶液和二氧化锰来制取氧气,写出该化学反应方程式 , 她选取的发生装置为(填序号,下同),收集装置为 , 验证集气瓶中收集的气体是氧气的实验操作为。
(2)、探究酸的化学性质。①小文向以下五只试管中加入稀盐酸,试管中无明显现象的是。(填序号)
A.
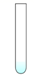 无色酚酞
无色酚酞 B.
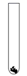 氧化铜
氧化铜 C.
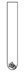 铝
铝 D.
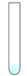 碳酸钠溶液 E.
碳酸钠溶液 E. 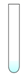 氢氧化钙溶液
氢氧化钙溶液②实验结束后,小文将A、E两支试管中的物质全部倒入一只洁净的烧杯中,充分反应,得到无色澄清溶液。小组成员一起对该溶液的成分进行探究。
(提出问题)该溶液中除水、酚酞外还含有哪些物质?
(查阅资料)氯化钙溶液基本呈中性。
(猜想与假设)Ⅰ.
Ⅱ.CaCl2、HCl
(设计实验)若猜想Ⅱ成立,小霞同学的验证方法是:取上述烧杯中的无色溶液少量于试管中,然后向试管中滴加碳酸钠溶液,观察到先有气泡冒出,然后出现白色沉淀,出现的沉淀的化学反应方程式为。
小组同学经讨论后认为,下列(填字母)药品单独使用也能验证猜想Ⅱ成立。
a pH试纸 b 紫色石蕊试液 c 铜 d 足量的浓氢氧化钠溶液 e 硝酸银溶液
(拓展与迁移)稀盐酸和稀硫酸具有相似的化学性质,是因为它们的溶液中都存在。
(反思与评价)实验室的废液排放前应该做“无害化”处理。
五、计算题
-
20. 已知20g氢氧化钠溶液与10g氯化镁溶液恰好完全反应,反应结束后过滤,滤液的质量为27.1g(不考虑实验过程的损失)。(反应的化学方程式:2NaOH+MgCl2=Mg(OH)2↓+2NaCl)计算:(1)、反应生成的Mg(OH)2的质量为多少。(2)、参加反应的氢氧化钠溶液的溶质质量分数?(写出计算过程)
-
-