四川省成都市青羊区2020年中考化学二模试卷
试卷更新日期:2020-07-01 类型:中考模拟
一、单选题
-
1. 生产、生活中的下列变化,属于物理变化的是( )A、钢铁生锈 B、粮食酿酒 C、汽油挥发 D、木炭燃烧2. 下列中草药煎制步骤中,属于过滤操作的是( )A、冷水浸泡 B、加热煎制 C、箅渣取液 D、灌装保存3. 钛是一种广泛应用于航天和航海工业的金属。已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( )A、4 B、22 C、26 D、484. 改善环境质量,推动绿色发展。下列做法不符合该理念的是( )A、多用一次性餐具 B、垃圾分类处理 C、选择公交出行 D、注意人走灯灭5. 下列食物显碱性的是( )
食物
苹果汁
葡萄汁
牛奶
鸡蛋清
pH
2.9~3.3
3.5~4.5
6.3~6.6
7.6~8.0
A、苹果汁 B、葡萄汁 C、牛奶 D、鸡蛋清6. 有关空气中主要成分的说法错误的是( )A、氮气可作保护气 B、稀有气体可用于制作霓虹灯 C、氧气可与多种物质发生反应 D、二氧化碳是一种空气污染物7. 下列关于CO2 实验室制法的说法中,错误的是( )A、 制CO2的药品
B、
制CO2的药品
B、 发生装置
C、
发生装置
C、 收集装置
D、
收集装置
D、 验满
8. 氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是 ()A、NH4Cl与KCl:观察外观 B、NH4HCO3与KCl:加水 C、K2SO4与Ca3(PO4)2:闻气味 D、(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味9. 20℃时,向100g水中不断加入固体甲或改变温度,得到相应的溶液①—③。下列说法错误的是( )
验满
8. 氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是 ()A、NH4Cl与KCl:观察外观 B、NH4HCO3与KCl:加水 C、K2SO4与Ca3(PO4)2:闻气味 D、(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味9. 20℃时,向100g水中不断加入固体甲或改变温度,得到相应的溶液①—③。下列说法错误的是( ) A、甲的溶解度曲线可用图2中的a表示 B、①中溶质与溶剂的质量比为1:5 C、只有②中的溶液为饱和溶液 D、①—③中溶液的溶质质量分数③>②>①10. 石蕊、硫酸、氢氧化钙、碳酸钠是常见的四种物质,它们的溶液之间的反应关系如图所示。图中两圆相交部分(A,B,C,D)表示物质间反应的主要实验现象,其中描述正确的是( )
A、甲的溶解度曲线可用图2中的a表示 B、①中溶质与溶剂的质量比为1:5 C、只有②中的溶液为饱和溶液 D、①—③中溶液的溶质质量分数③>②>①10. 石蕊、硫酸、氢氧化钙、碳酸钠是常见的四种物质,它们的溶液之间的反应关系如图所示。图中两圆相交部分(A,B,C,D)表示物质间反应的主要实验现象,其中描述正确的是( ) A、石蕊溶液变为蓝色 B、无明显现象 C、生成白色沉淀 D、石蕊呈紫色11. 某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分,反应的微观示意图如下。下列说法正确的是( )
A、石蕊溶液变为蓝色 B、无明显现象 C、生成白色沉淀 D、石蕊呈紫色11. 某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分,反应的微观示意图如下。下列说法正确的是( ) A、四种物质均属于化合物 B、物质丁由原子构成 C、参加反应的甲与生成的丁的分子个数比为2:1 D、参加反应的甲与乙的质量比为1:212. 利用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。下列说法错误的是( )
A、四种物质均属于化合物 B、物质丁由原子构成 C、参加反应的甲与生成的丁的分子个数比为2:1 D、参加反应的甲与乙的质量比为1:212. 利用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。下列说法错误的是( ) A、先推入的是NaOH溶液 B、BC段,CO2与NaOH反应基本停止 C、D点压强比初始瓶内压强大,此时瓶内二氧化碳气体的量比初始多 D、最终压强比初始压强小,可能是因为有部分二氧化碳溶于水13. 下列物质分离方法错误的是( )A、除去KNO3中少量的NaCl:冷却热饱和溶液 B、粗盐提纯的步骤:溶解→ 过滤→蒸发→冷却结晶→过滤 C、除去H2中的HCl:将气体通过装有AgNO3溶液的洗气瓶 D、除去铜粉中的CuO:用足量的稀硫酸浸泡后过滤、洗涤14. 用如图装置,制一氧化碳并还原氧化铜。资料:①HCOOH(甲酸)=H2O+CO↑②CuO+CO Cu+CO2下列说法错误的是( )
A、先推入的是NaOH溶液 B、BC段,CO2与NaOH反应基本停止 C、D点压强比初始瓶内压强大,此时瓶内二氧化碳气体的量比初始多 D、最终压强比初始压强小,可能是因为有部分二氧化碳溶于水13. 下列物质分离方法错误的是( )A、除去KNO3中少量的NaCl:冷却热饱和溶液 B、粗盐提纯的步骤:溶解→ 过滤→蒸发→冷却结晶→过滤 C、除去H2中的HCl:将气体通过装有AgNO3溶液的洗气瓶 D、除去铜粉中的CuO:用足量的稀硫酸浸泡后过滤、洗涤14. 用如图装置,制一氧化碳并还原氧化铜。资料:①HCOOH(甲酸)=H2O+CO↑②CuO+CO Cu+CO2下列说法错误的是( ) A、反应①属于分解反应 B、反应②中各元素的化合价均改变 C、反应过程中a处黑色固体变红 D、气球的作用是收集一氧化碳,防止其污染大气15. 图中连线两端的物质在通常情况下可以相互反应。下列四组选项中,符合该图要求的是( )
A、反应①属于分解反应 B、反应②中各元素的化合价均改变 C、反应过程中a处黑色固体变红 D、气球的作用是收集一氧化碳,防止其污染大气15. 图中连线两端的物质在通常情况下可以相互反应。下列四组选项中,符合该图要求的是( )
①
②
③
④
⑤
⑥
A
CO2
NaOH溶液
稀HCl溶液
Ca(OH)2溶液
CuCl2溶液
Fe
B
CaO
稀HCl溶液
Fe
稀H2SO4溶液
Na2CO3溶液
Ca(OH)2溶液
C
Fe
稀H2SO4溶液
BaCl2溶液
Cu(NO3)2溶液
Ca(OH)2溶液
Na2CO3溶液
D
Zn
稀HCl溶液
CaCO3
CuSO4溶液
NaOH溶液
FeCl3溶液
A、A B、B C、C D、D二、填空题
-
16. 科技改变生活,化学服务生活。(1)、氮气充入食品包装袋防腐,是因为。(2)、宇航员在太空舱中所需的氧气来自电解水,其反应的化学方程式为。(3)、宇航员太空行走时,需要“人造空气”供给呼吸。这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、还有二氧化碳。“人造空气”中供给呼吸的物质是。“人造空气”中的氮气和空气中的氮气化学性质(填“相同”或“不同”)。(4)、修建高铁过程中常用黑火药(含KNO3、S、C)进行工程爆破,黑火药爆炸时产生浓烟,推测该浓烟中含有K2S,从元素守恒角度说明理由。(5)、体积分数为75%的酒精溶液常用作消毒剂,此次疫情中也被广泛使用。
①75%的酒精溶液中的溶质是。
②将75mL酒精和25mL水混合时,发现体积小于100mL,这是因为。
(6)、84消毒液有效成分为NaClO,NaClO中氯元素质量分数的计算式为。三、简答题
-
17. 下表给出了某些金属的信息。如表给出了某些金属的信息。
每吨金属在2020年4月的价格(元)
地壳中的含量(%)
铝
16000
7.73
铂
305 000 000
0.000 000 1
铁
4500
4.75
金
320 000 000
0.000 000 1
(1)、依据表中信息解释,金和铂均很昂贵的原因是。(2)、工业上用含铝、铁的矿石制取铝和铁。①铝抗腐蚀性强的原因是。
②将熔融的氧化铝通电分解,可获得铝和另一种单质。反应的化学方程式是。
③根据化学方程式计算,用赤铁矿(主要成分为Fe2O3)炼铁,若要得到112 t铁,理论上需要Fe2O3的质量为多少t?
四、推断题
-
18. 有关物质的转化关系如图所示,其中A为一种生活中常见的有机化合物,在通常情况下,X、Y为两种气态单质,Z为固态单质,B、C、D为三种常温下状态各不相同的氧化物(个别反应的条件未注明)。
 (1)、写出有关物质的化学式:A可能是(填一种即可);C;(2)、M可能是 , 写出它的一种用途;(3)、写出反应②的化学方程式。反应③的基本反应类型是。
(1)、写出有关物质的化学式:A可能是(填一种即可);C;(2)、M可能是 , 写出它的一种用途;(3)、写出反应②的化学方程式。反应③的基本反应类型是。五、流程题
-
19. NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如下:
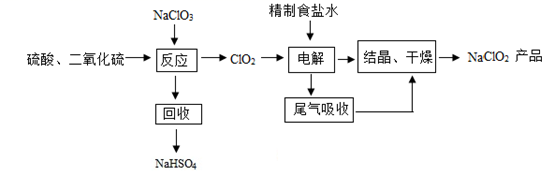 (1)、NaClO2中Cl的化合价为。(2)、补全化学方程式:2NaClO3++=2ClO2+2NaHSO4。(3)、精制食盐水时,用NaOH溶液将杂质MgCl2转化为沉淀除去,该复分解反应的化学方程式为。(4)、该工艺流程中体现环保意识的环节是(填写一条即可)。
(1)、NaClO2中Cl的化合价为。(2)、补全化学方程式:2NaClO3++=2ClO2+2NaHSO4。(3)、精制食盐水时,用NaOH溶液将杂质MgCl2转化为沉淀除去,该复分解反应的化学方程式为。(4)、该工艺流程中体现环保意识的环节是(填写一条即可)。六、实验题
-
20. 用如图装置对人体吸入的空气和呼出的气体进行探究。
 (1)、检查装置气密性:向集气瓶中加水至浸没长导管末端。用止水夹加紧左侧橡胶管,手握集气瓶。能说明装置气密性良好的现象是。(2)、进行实验:向d中加入适量澄清石灰水,实验操作及现象如表。
(1)、检查装置气密性:向集气瓶中加水至浸没长导管末端。用止水夹加紧左侧橡胶管,手握集气瓶。能说明装置气密性良好的现象是。(2)、进行实验:向d中加入适量澄清石灰水,实验操作及现象如表。操作
c处现象
d处现象
从a处缓缓吸气5次
无明显现象
石灰水不浑浊
从b处缓缓吹气5次
出现无色液滴
石灰水变浑浊
①吸气、吹气时,c处现象不同的原因是。
②吹气时,澄清石灰水变浑浊的化学方程式是。
21. 实验室用如图所示装置制取氧气并完成相关实验(夹持仪器已略去)。 (1)、A装置中发生反应的化学方程式为。(2)、用C装置收集氧气的方法是(填序号)。
(1)、A装置中发生反应的化学方程式为。(2)、用C装置收集氧气的方法是(填序号)。①排水法 ②向下排空气法 ③向上排空气法
(3)、检验C中收集满氧气的操作是。(4)、C中收集满氧气后,打开弹簧夹K1、K4 , 关闭K2、K3 , 其中打开K1的目的是)。点燃D中燃烧匙内的红磷后,立即伸入C装置中并把塞子塞紧,待红磷熄灭,C装置冷却后,打开K3观察到的现象是。七、科学探究题
-
22. 化学小组用图1装置验证二氧化碳与水的反应。

盐酸浓度
观察到的现象
甲组
浓盐酸(36.5%)
B中石蕊溶液由紫色变成红色
C中石蕊溶液没有变为紫色
乙组
稀盐酸(13.5%)
B中石蕊溶液由紫色变为红色
C中石蕊溶液变为紫色
(1)、A中反应的化学方程式为。(2)、乙组C中反应的化学方程式为。(讨论与交流)同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
(提出猜想)盐酸的挥发性与浓度有关。
(进行实验)用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。

盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
盐酸浓度(%)
13.5
20
26.2
29.2
32.2
36.5
氯离子浓度(mg/L)
1.1
1.4
3.7
19.0
59.8
209.2
分析表中数据 , 能够得出盐酸的挥发性与浓度的关系是。
(得出结论)猜想正确
(实验反思)甲组石蕊溶液变红不能证明二氧化碳与水反应。
(实验改进)甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→ →→b。选择饱和NaHCO3溶液除杂的原因是。

-
-
-
-