浙教版科学 八年级下册 期末复习专题之简答题
试卷更新日期:2020-06-22 类型:复习试卷
一、解答题
-
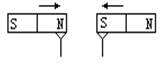
1. 有两个完全相同的磁铁,在不同的磁极上各吸引一只铁钉,如图所示。如果将两磁铁靠近,直至两个磁极相接触,会有什么现象发生?并分析产生有关现象的原因。
 2. 如图甲所示是一家庭燃气报警器的部分电路示意图,其中控制电路中的R1是由气敏电阻制成的传感器,R1的阻值与燃气的浓度的关系如图乙。出厂预设当燃气浓度达到4%时报警,出厂测试时,控制电路的电源电压U1为3伏且保持恒定,闭合开关S1、S2 , 移动滑动变阻器R2滑片P的位置,当控制电路中的电流为0.03安,电磁铁A恰好能将衔铁B吸下,工作电路中相应的灯亮起而报警。(电磁铁线圈的阻值忽略不计)
2. 如图甲所示是一家庭燃气报警器的部分电路示意图,其中控制电路中的R1是由气敏电阻制成的传感器,R1的阻值与燃气的浓度的关系如图乙。出厂预设当燃气浓度达到4%时报警,出厂测试时,控制电路的电源电压U1为3伏且保持恒定,闭合开关S1、S2 , 移动滑动变阻器R2滑片P的位置,当控制电路中的电流为0.03安,电磁铁A恰好能将衔铁B吸下,工作电路中相应的灯亮起而报警。(电磁铁线圈的阻值忽略不计) (1)、当报警器报警时,灯亮。(选填“L1 ”或“L2”)(2)、该报警器要达到出厂预设值,滑动变阻器接入电路的阻值有多大?(3)、某场地安装该报警器后,想在燃气浓度达到3%时就报警,该滑动变阻器滑片P应如何移动,请简述其中的科学原理。3. 为解决妈妈回家晚耽搁收衣服的问题,小科设计了“自动收缩晾衣架”(如图1)。主要部件包括可折叠晾衣架、电动机及控制电路。其中晾衣架下端连杆固定在竖杆上的P点,上端连杆通过滑环可在竖杆上自由移动,R为光敏电阻,电动机M通过拉绳与晾衣架上端连杆相连,S是按钮开关,向上按按钮可切断电路(黑色部分为导体,白色部分为绝缘体)。白天晾衣架展开伸出窗外(如图1),天黑时电动机接通,将连杆向上拉动,使晾衣架自动收缩折叠(如图2),同时连杆上的突起Q将S的按键向上按,使电路切断,停止工作。
(1)、当报警器报警时,灯亮。(选填“L1 ”或“L2”)(2)、该报警器要达到出厂预设值,滑动变阻器接入电路的阻值有多大?(3)、某场地安装该报警器后,想在燃气浓度达到3%时就报警,该滑动变阻器滑片P应如何移动,请简述其中的科学原理。3. 为解决妈妈回家晚耽搁收衣服的问题,小科设计了“自动收缩晾衣架”(如图1)。主要部件包括可折叠晾衣架、电动机及控制电路。其中晾衣架下端连杆固定在竖杆上的P点,上端连杆通过滑环可在竖杆上自由移动,R为光敏电阻,电动机M通过拉绳与晾衣架上端连杆相连,S是按钮开关,向上按按钮可切断电路(黑色部分为导体,白色部分为绝缘体)。白天晾衣架展开伸出窗外(如图1),天黑时电动机接通,将连杆向上拉动,使晾衣架自动收缩折叠(如图2),同时连杆上的突起Q将S的按键向上按,使电路切断,停止工作。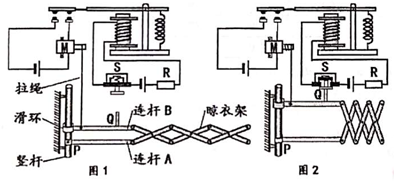 (1)、当光照强度增大时,电磁铁磁性。(选填“变大”、“不变”或“变小”)(2)、已知控制电路中电源电压为3伏,电磁铁线圈的阻值为60欧,光敏电阻的阻值随光照强度的变化情况如下表所示,电磁铁衔铁吸合电流至少达到30毫安,则此晾衣架自动收缩时的光照强度是多少?(写出计算过程)
(1)、当光照强度增大时,电磁铁磁性。(选填“变大”、“不变”或“变小”)(2)、已知控制电路中电源电压为3伏,电磁铁线圈的阻值为60欧,光敏电阻的阻值随光照强度的变化情况如下表所示,电磁铁衔铁吸合电流至少达到30毫安,则此晾衣架自动收缩时的光照强度是多少?(写出计算过程)光照强度(勒克斯)
5
10
15
20
25
30
光敏电阻R阻值(欧)
10
15
20
26
40
60
(3)、小科在实际调试时发现,还没天黑晾衣架就自动缩回,为解决此问题,请提出两种改进方法: , 。4. 我国目前的动车上均安装了烟雾报警器,一旦有吸烟,列车上的烟雾报警系统就会报警,列车就会自动减速甚至停车。小刘在查阅资料后,自行设计了一只“烟雾报警器”,电路如图。该报警器由“控制电路和“工作电路”所组成,其中“控制电路”由光敏电阻R、电磁铁(线圈阻值R0=12Ω)、电源U=6V开关等组成;“工作电路”由工作电源、电铃、导线等组成。小刘的设计思路:当光敏电阻接收到的光强减弱到一定程度时,工作电路接通,电铃报警。已知该光敏电阻的阻值R与光强E之间的关系如表所示。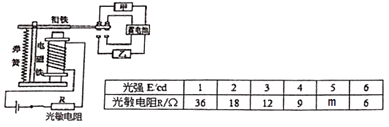 (1)、根据光敏电阻的阻值R与光强E之间的关系,推测m=。(2)、根据报警器的工作原理判断,电铃应接在(填“甲”或“乙”)处。(3)、闭合开关S,如果当线圈中的电流大于或等于250mA时,继电器的衔铁被吸合,则光敏电阻接收到的光照强度需要在多少cd以上?(4)、若要提高该烟雾报警器的灵敏度(即在烟雾更少条件下就能报警),你提出一种改进建议。5. 小明在观看了宾馆等处的光电烟雾探测器后,自己设计了一只“火灾报警器”(如图)。该报警器由“控制电路”和“工作电路”所组成,其中“控制电路”由光敏电阻R、电磁铁(线圈阻值R0=15Ω)、电源U=6V、开关等组成;“工作电路”由工作电源、电铃、导线等组成。小明的设计思想:当光敏电阻接收到的光照减弱到一定程度时,工作电路接通,电铃报警。
(1)、根据光敏电阻的阻值R与光强E之间的关系,推测m=。(2)、根据报警器的工作原理判断,电铃应接在(填“甲”或“乙”)处。(3)、闭合开关S,如果当线圈中的电流大于或等于250mA时,继电器的衔铁被吸合,则光敏电阻接收到的光照强度需要在多少cd以上?(4)、若要提高该烟雾报警器的灵敏度(即在烟雾更少条件下就能报警),你提出一种改进建议。5. 小明在观看了宾馆等处的光电烟雾探测器后,自己设计了一只“火灾报警器”(如图)。该报警器由“控制电路”和“工作电路”所组成,其中“控制电路”由光敏电阻R、电磁铁(线圈阻值R0=15Ω)、电源U=6V、开关等组成;“工作电路”由工作电源、电铃、导线等组成。小明的设计思想:当光敏电阻接收到的光照减弱到一定程度时,工作电路接通,电铃报警。
已知该光敏电阻的阻值R与光强E之间的一组实验数据如下表所示:(“光强”表示光强弱的程度,符号为E,单位为cd。)
光强E/cd
1.0
2.0
3.0
4.0
5.0
6.0
光敏电阻R/Q
36.0
18.0
12.0
9.0
7.2
6.0
(1)、分析上表数据,根据光敏电阻的阻值R随光强E变化的规律,归纳出光敏电阻的阻值R随光强E变化的关系式为R=。(2)、闭合电键S,如果当线圈中的电流大于或等于250mA时,继电器的衔铁被吸合,则光敏电阻接收到的光照强度需要在多少cd以上?(3)、按小明的设计,当室内烟雾增大时,光照减弱,光敏电阻的阻值增大到一定值时,衔铁与 (选填“上方”或“下方”)的M、N接触,电铃工作报警。6. 超市的电动扶梯,有人乘时运行较快,无人乘时运行较慢。某同学想利用电磁继电器设计这样的电路。(1)、力敏电阻R0的阻值与所受压力的关系如图甲所示,则由图甲可得出的结论是:(2)、根据要求请将图乙的工作电路连接完整。(3)、控制电路电源电压为24伏,当电流达到20mA时电磁铁将衔铁吸下。现在要求一个质量为40千克的小朋友站在电梯上,就能使电梯较快运行,则滑动变阻器R1接入电路的阻值为多大?(4)、如果要求质量更小的人站上电梯就能使其较快运行,应该如何改动控制电路?(写出两种方法) 7. 阅读短文,回答问题:
7. 阅读短文,回答问题:漏电保护器
根据安全用电要求,住户家里除了要安装防止电流过大的自动空气开关外,还必须安装如图所示的漏电保护器。其示意图如图甲所示,其内部结构相当于一个自动开关,正常情况下,住户家中没有电流流向地面,即图中I3为零,进户线中流入的电流I1和流出的电流I2相等,漏电保护器内部自动开关处于闭合状态。如果电路中某处发生漏电(漏电是指电流从墙体、人体、接地线或其他路径流向地面),即图中的I3不为零,就会造成I1和I2不相等,当I1和I2的差异达到一定值,保护器内部自动开关就会立即断开。排除漏电故障后,重新合闸即可恢复供电。为确保使用安全,漏电保护器上设置了试验按钮,需要每月试按一次,如果试验按钮按下漏电保护器无动作,说明漏电保护器需要更换。
 (1)、关于漏电保护器,下列说法正确的是 。A、当电路发生短路时,漏电保护器会自动切断电路 B、人站在绝缘物上双手分别触摸火线与零线,漏电保护器不会切断电路 C、正常情况下家庭电路中火线中的电流大于零线中的电流 D、漏电保护器跳闸后按下试验按钮即可恢复供电(2)、如果发生漏电,漏电电流为I3 , 则I1、I2、I3大小关系的表达式为。(3)、站在地面上的人体不小心接触了火线,如图乙所示,该人体的电阻为2000Ω,人与地面、电线等的接触电阻为3500Ω,此时流过人体的电流为mA。(4)、由于安装人员的疏忽,在安装三孔插座时,误将连接零线和地线的孔接反,此时如果将洗衣机的三脚插头插入该插座,漏电保护器(会/不会)断开,理由是。(5)、漏电保护器的试验电路,由一只试验开关S与电阻R组成,闭合试验开关S就能模拟漏电情形,试验电路的连接符合要求的是。
(1)、关于漏电保护器,下列说法正确的是 。A、当电路发生短路时,漏电保护器会自动切断电路 B、人站在绝缘物上双手分别触摸火线与零线,漏电保护器不会切断电路 C、正常情况下家庭电路中火线中的电流大于零线中的电流 D、漏电保护器跳闸后按下试验按钮即可恢复供电(2)、如果发生漏电,漏电电流为I3 , 则I1、I2、I3大小关系的表达式为。(3)、站在地面上的人体不小心接触了火线,如图乙所示,该人体的电阻为2000Ω,人与地面、电线等的接触电阻为3500Ω,此时流过人体的电流为mA。(4)、由于安装人员的疏忽,在安装三孔插座时,误将连接零线和地线的孔接反,此时如果将洗衣机的三脚插头插入该插座,漏电保护器(会/不会)断开,理由是。(5)、漏电保护器的试验电路,由一只试验开关S与电阻R组成,闭合试验开关S就能模拟漏电情形,试验电路的连接符合要求的是。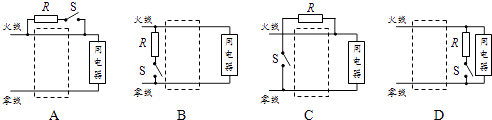 8. 化学用语是学习化学的重要工具,请用正确的化学符号表示:(1)、3个钠原子;(2)、碳酸根离子;(3)、氯化锌;(4)、某化合物只由N、O两种元素组成,且在该化合物中N的化合价为+5,该化合物的化学式是。9. 元素周期表是学习和研究化学的重要工具。如图是元素周期表部分内容,请根据表中信息完成相关问题。
8. 化学用语是学习化学的重要工具,请用正确的化学符号表示:(1)、3个钠原子;(2)、碳酸根离子;(3)、氯化锌;(4)、某化合物只由N、O两种元素组成,且在该化合物中N的化合价为+5,该化合物的化学式是。9. 元素周期表是学习和研究化学的重要工具。如图是元素周期表部分内容,请根据表中信息完成相关问题。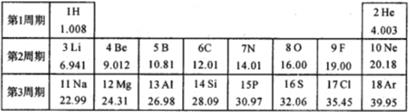 (1)、第三周期中的稀有气体元素的质子数是。(2)、元素周期表的纵行叫做族,分为主族、副族、VⅢ族和0族。主族用字母“A”来表示,共有七个主族,依次用IA族、ⅡA族、ⅢA族、ⅣA族、VA族、ⅥA族、VⅡA族表示。同主族元素化学性质相似。X²+的核外电子数目为18,则X在第四周期第族。(3)、下列各组中的两种元素具有相似化学性质的是 。A、N C B、F Cl C、Mg Al D、Ne Na(4)、核电荷数1-18的非金属元素A和B,可形成原子个数比1:1和2∶1的两种常温下的化合物,写出这两种化合物的化学式。10. “橘生山海间,味道自然甜”,象山红美人皮薄易剥,入口即化,有独特清新的橘香味,香味物质中有一种为戊酸乙酯(C7H14O2),请回答下列问题:(1)、戊酸乙酯属于(填“混合物”或“纯净物”)。(2)、C7H14O2的式量为。(3)、C7H14O2中的数字14表示的意义是。11. 世界卫生组织正式将这次武汉疫情命名为“2019新型冠状病毒肺炎”(英文:COVID-19),简称“新冠肺炎”。国家食品药品监督管理总局药审中心(CDE)批准申请单位中日友好医院和中国医学科学院药物研究所,将瑞德西韦注射液用于治疗新冠肺炎三期临床试验,其申报书中部分内容如下图,据此回答:
(1)、第三周期中的稀有气体元素的质子数是。(2)、元素周期表的纵行叫做族,分为主族、副族、VⅢ族和0族。主族用字母“A”来表示,共有七个主族,依次用IA族、ⅡA族、ⅢA族、ⅣA族、VA族、ⅥA族、VⅡA族表示。同主族元素化学性质相似。X²+的核外电子数目为18,则X在第四周期第族。(3)、下列各组中的两种元素具有相似化学性质的是 。A、N C B、F Cl C、Mg Al D、Ne Na(4)、核电荷数1-18的非金属元素A和B,可形成原子个数比1:1和2∶1的两种常温下的化合物,写出这两种化合物的化学式。10. “橘生山海间,味道自然甜”,象山红美人皮薄易剥,入口即化,有独特清新的橘香味,香味物质中有一种为戊酸乙酯(C7H14O2),请回答下列问题:(1)、戊酸乙酯属于(填“混合物”或“纯净物”)。(2)、C7H14O2的式量为。(3)、C7H14O2中的数字14表示的意义是。11. 世界卫生组织正式将这次武汉疫情命名为“2019新型冠状病毒肺炎”(英文:COVID-19),简称“新冠肺炎”。国家食品药品监督管理总局药审中心(CDE)批准申请单位中日友好医院和中国医学科学院药物研究所,将瑞德西韦注射液用于治疗新冠肺炎三期临床试验,其申报书中部分内容如下图,据此回答: (1)、一个瑞德西韦分子含有个原子,其中碳、氮原子个数比为。(2)、该药品中氧元素的质量分数是(精确到0.1%)。12. 核事故时往往泄漏出污染物(具有放射性的碘原子)。为避免核辐射,需一次性口服100毫克(不具放射性的碘原子),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用。请回答:(1)、“具有放射性的碘原子”和“不具有放射性的碘原子”两者的关系是 。A、同种元素 B、同种物质 C、同种分子 D、同种原子(2)、若所处的环境已受污染,通过服用加碘食盐(注:加碘食盐中的碘为碘酸钾)的方法能否有效起到避免核辐射的目的呢?
(1)、一个瑞德西韦分子含有个原子,其中碳、氮原子个数比为。(2)、该药品中氧元素的质量分数是(精确到0.1%)。12. 核事故时往往泄漏出污染物(具有放射性的碘原子)。为避免核辐射,需一次性口服100毫克(不具放射性的碘原子),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用。请回答:(1)、“具有放射性的碘原子”和“不具有放射性的碘原子”两者的关系是 。A、同种元素 B、同种物质 C、同种分子 D、同种原子(2)、若所处的环境已受污染,通过服用加碘食盐(注:加碘食盐中的碘为碘酸钾)的方法能否有效起到避免核辐射的目的呢?查阅资料:成人每天食用食盐的质量通常为6g;某种加碘食盐的标签如图所示。
配料表:氯化钠、碘酸钾(KIO3)
净含量:500g
碘含量(以I计):20~50mg/kg
问题分析:500g该品牌食盐中,含碘的最大质量是;若要使人体甲状腺中的碘达到饱和,至少需要一次性食用该品牌碘盐。
结论:日常服用加碘食盐(选填“能”或“不能”)起到避免核辐射目的。
13. 在宏观、微观和符号之间建立联系是科学学科的特点。(1)、在水、铜和氯化钠三种物质中,由分子构成的是。(2)、某地违规将有腐蚀性的二甲醚掺入液化石油气。二甲醚的化学式为C2H6O,它是由种元素组成。(3)、A、B、C、D表示4种物质,其中部分物质分子的微观示意图如图所示。
A和B在一定条件下可发生反应A+2B=C+2D,则A的化学式为 , A、B、C、D中属于单质的是(填字母序号)。
14. 伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是:一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。(1)、1803年,近代化学之父,英国科学家道尔顿(Dalton J)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆森通过实验发现了电子,进一步发展了原子、分子论。汤姆森主要是纠正了“道尔顿原子论”中的观点。
1911年,卢瑟福又通过实验,推测原子是由和核外电子构成,并提出了沿用至今的现代原子结构理论。
(2)、道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。在科学研究中,像汤姆森和卢瑟福这样,对实验现象进行解释的过程叫做。原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了来表达他们的理论成果。
15. 尿素[CO(NH2)2]和碳酸氢铵(NH4HCO3)是常见的氮肥。根据资料:某地尿素的市场价格为 2500 元/t,碳酸氢铵的市场价格为 800 元/t。若分别用 10000 元采购尿素和碳酸氢铵, 请通过计算说明哪种化肥所含氮元素的质量多?(要求写计算过程和结果)16. 1989 年世界卫生组织把铝列为食品污染源之一,每人每日的摄入量控制在 0.004g 以下。若在 1kg 米面食品中加入明矾 2g(明矾的化学式为 KAl(SO4)2·12H2O),请回答下列问题:(1)、人从食物中摄入的铝指的是( )(填字母)。A.铝元素 B.铝单质 C.铝合金
(2)、明矾中 K∶S∶H 的质量比= ;铝元素的质量分数为(计算结果精确到0.1%)。(3)、如果某人一天吃了 100g 上述面食品,通过计算说明其摄入的铝的量是否超过安全摄入量?(通过计算说明)17. 在高温条件下,A,B两种物质可以发生化学反应生成C和D。反应前后分子种类变化的微观示意图如图所示。 (1)、一个A分子中共含有个原子;(2)、四种物质中,属于单质的是(填图中的字母序号);(3)、关于该反应,以下叙述正确的是 。A、分子的个数没有改变 B、原子种类没有改变 C、分子的个数发生改变18. 学习空气中氧气含量测定实验后,小明将课本中的实验装置改进为如图甲实验装置。用加热的电烙铁点燃红磷后,立刻拔掉插头,无线气压计实时记录瓶内的气压变化。实验过程中气压变化如图乙。
(1)、一个A分子中共含有个原子;(2)、四种物质中,属于单质的是(填图中的字母序号);(3)、关于该反应,以下叙述正确的是 。A、分子的个数没有改变 B、原子种类没有改变 C、分子的个数发生改变18. 学习空气中氧气含量测定实验后,小明将课本中的实验装置改进为如图甲实验装置。用加热的电烙铁点燃红磷后,立刻拔掉插头,无线气压计实时记录瓶内的气压变化。实验过程中气压变化如图乙。资料:一个密闭容器内气压受温度和气体量的影响,温度越高,气体质量越大,气体气压越大。
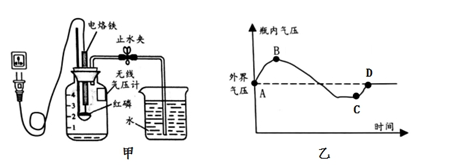
结合以上信息,及所学知识,对图乙中AB段与CD段气压上升原因做出简要说明。
19. 有A、B两种物质组成的混合物四份,总质量均为12克。A和B在一定条件下可发生化合反应生成物质C。四份混合物内含A和B的质量,及它们充分反应后生成C的质量见表。物质
第一份
第二份
第三份
第四份
反应前A的质量(克)
11
8
a
反应前B的质量(克)
1
4
b
反应后生成C的质量(克)
5
10
7.5
(1)、第一份混合物中参加反应的A和B的质量比为。(2)、第二份混合物在反应结束后,反应物中的有剩余。(3)、若第三份混合物恰好能完全反应,则a的值是。(4)、第四份混合物反应前,A和B的质量比为。20. 生活中处处有化学。结合你所学的知识回答下列问题:(1)、最近,小明家做饭时燃气灶火焰呈现黄色,锅底出现黑色。通过维修师傅调节燃气灶的进风口之后,火焰变回淡蓝色。这说明使燃料充分燃烧通常需要考虑两点:一是燃烧时要有;二是燃料与空气要有足够大的接触面积。(2)、请根据下图回答下列问题:工厂排污导致小孩“血铅超标”,工厂方面的辩解错在哪里?。
 (3)、若我们掌握一定的应急避险技能,可通过自救与互救来降低灾害风险。例如身上着火,可快速倒在地上,把身上的火苗压灭。这种灭火方式,利用的原理主要是。(4)、请用文字表述“火场逃生”图所示的火场逃生方法。(答一种即可)21. 下图所示是实验室制取气体的常用装置,请回答下列问题:
(3)、若我们掌握一定的应急避险技能,可通过自救与互救来降低灾害风险。例如身上着火,可快速倒在地上,把身上的火苗压灭。这种灭火方式,利用的原理主要是。(4)、请用文字表述“火场逃生”图所示的火场逃生方法。(答一种即可)21. 下图所示是实验室制取气体的常用装置,请回答下列问题: (1)、写出仪器a和b的名称:a ;b 。(2)、下列哪种操作方法可以得到平稳的氧气流?(填序号)
(1)、写出仪器a和b的名称:a ;b 。(2)、下列哪种操作方法可以得到平稳的氧气流?(填序号)①把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中。②把二氧化锰加入盛有过氧化氢溶液的试管中。
(3)、实验室利用装置A制取氧气时,长颈漏斗下端要插入液面以下,其目的是。(4)、实验室用装置C收集氧气时,验满的方法是木条熄灭。(5)、已知:氨气是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰两种固体的混合物来制取氨气,请你从上图中选出制取并收集一瓶氨气所需的装置组合。22. “水循环”“氧循环”和“碳循环”是自然界存在的三大重要循环。请结合下图回答问题:
 (1)、从物质变化及分子角度看,三种循环中有一种与另外两种在变化上有本质的区别,这种循环主要是由的运动引起的。(2)、用学科观点分析碳循环和氧循环,其中正确的是(填字母序号)。
(1)、从物质变化及分子角度看,三种循环中有一种与另外两种在变化上有本质的区别,这种循环主要是由的运动引起的。(2)、用学科观点分析碳循环和氧循环,其中正确的是(填字母序号)。A.变化观:每个人都在参与碳、氧循环
B.守恒观:碳、氧循环过程中各 元素守恒,其化合价不变
C.平衡观:碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
D.微粒观:绿色植物的作用是使自然界中的氧原子总数增加
(3)、自然界中的碳循环主要是通过二氧化碳来实现的。图中消耗二氧化碳的途径有(填数字序号)。近年来,大气中二氧化碳含量增加,导致温室效应,因此人类要积极采取措施维持循环体系中二氧化碳的相对平衡: (4)、为解决日益加剧的温室效应,有科学家提出“绿色自由”构想:把CO2含量高的气体用氢氧化钠溶液吸收,然后再通过化学反应在分解池内放出二氧化碳进入合成塔,在合成塔内300℃、100kPa和催化剂条件下使之变为甲醇(CH3OH)和水。写出该反应的化学方程式。23. 现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入稀盐酸并不断振荡,首先发生反应:
(4)、为解决日益加剧的温室效应,有科学家提出“绿色自由”构想:把CO2含量高的气体用氢氧化钠溶液吸收,然后再通过化学反应在分解池内放出二氧化碳进入合成塔,在合成塔内300℃、100kPa和催化剂条件下使之变为甲醇(CH3OH)和水。写出该反应的化学方程式。23. 现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入稀盐酸并不断振荡,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后才发生反应:
NaHCO3+HCl=NaCl+CO2↑+H2O。
已知:该温度下CO2密度为1.98g/L,实验测得产生的CO2的与加入稀盐酸的数据如图。
 (1)、当加入g盐酸时,才开始产生CO2;图中V=mL。(2)、请计算:①所加入盐酸中HCl的质量分数为多少?
(1)、当加入g盐酸时,才开始产生CO2;图中V=mL。(2)、请计算:①所加入盐酸中HCl的质量分数为多少?②原样品中Na2CO3和NaHCO3的质量各是多少?
24. 民以食为天,当前人们对食品的质量要求越来越高,绿色有机蔬菜就是大家喜爱的食品之一。为了提高产量的同时又能种出让消费者满意的蔬菜,菜农们有以下的经验分享。
经验一:往菜地的土壤中掺入一定比例沙子,增加土壤的透气性。
经验二:选“发酵”好的农家肥(家禽家畜的粪便及杂草等)作为肥料,“发酵”能杀死其中的一些寄生虫与有害小动物且滋养了大量的微生物。
经验三:搭配种植高矮不同的多品种蔬菜。
结合上述信息,综合运用所学知识,对该菜农能种出高产量与高品质的绿色有机蔬菜作出解释。
25. 根据提供的资料回答问题:我国的人均耕地面积远远低于世界平均水平,所以保护好和合理利用现有的土地资源是我国的一项重要国策。提高单位面积的粮食产量、防止水土流失等都是正在研究并且可行的方法。
(1)、除草可以除去和庄稼争夺生存条件的杂草以保证粮食产量。除草的方法有多种,“锄禾日当午”中的“锄禾”和喷洒除草剂都能除草,但是“锄禾”的方式更有利于庄稼的生长,因为“锄禾”不光能除草,还能。(2)、农民不光除草,有时还种草,例如在冬季农田闲置的时候,种上学名是“紫云英”、俗称“红花草籽”的草,到来年春天犁田毁草,把紫云英翻压在土里,这样可以增加土壤肥力,这是因为。(3)、水土流失已经严重威胁我国的土地资源,请写出防治水土流失提出两个合理建议: , 。26. 有人提出:“行人经常在草坪上行走,会造成土壤因板结而缺少空气,从而影响草的生长。”小乐设计如下方案以初步验证这个观点。步骤1:在校园中选择一块干燥、疏松的土地和一块干燥、被多次踩过的土地,各取长、宽、厚均为5厘米的土块,分别记作甲土块和乙土块;另取一块相同规格的铁块。
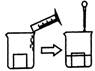
步骤2:将甲、乙土块和铁块分别放入3只相同的烧杯中,用量筒取一定体积的水,沿烧杯壁缓慢地向烧杯内注水;快要浸没土块或铁块时,换用滴管向烧杯内滴水,直到水刚好浸没甲、乙土块和铁块,如图所示;记录用水体积分别为V1、V2和V3。请回答:
 (1)、在步骤2中,“快要浸没土块或铁块时,换用滴管向烧杯内滴水,直到水刚好浸没甲、乙土块和铁块”。这样操作的目的是。(2)、甲土块中的空气体积分数为。(3)、若发现V1V2(填“大于”“小于”或“等于”),说明疏松的土地比踩踏过的土地空气含量高。27. “毒大米”事件让人们认识到了重金属污染的危害,重金属在土壤中的分散范围广、隐蔽性强、难清理,现在科学家利用一类超强金属吸收能力的植物(又叫超富集植物)对土壤进行“排毒”。(1)、双子叶的超富集植物,由根系从土壤中吸取重金属,可通过木质茎中的 (填“韧皮部”“木质部”或“形成层”),转移、贮存到枝叶等地上部分。(2)、一种叫做重雪球的植物,富集金属镍的能力很强。通过改良植株增强重雪球的吸镍性,每克干燥的枝叶可含有0.2克镍。对500千克的重雪球的干燥枝叶进行提纯处理,理论上可获得千克的镍。(3)、超富集植物能帮助人们更好地改善由于采矿等原因而恶化的土壤,使耕地重新焕发生机。植物“排毒”具有的优势是(写出一点即可)。28. 绿色植物通过根从土壤中吸收来的水分,绝大部分通过蒸腾作用散失在大气中。下表中的数据显示了一株植物在一天的主要时段内散失水分的量。
(1)、在步骤2中,“快要浸没土块或铁块时,换用滴管向烧杯内滴水,直到水刚好浸没甲、乙土块和铁块”。这样操作的目的是。(2)、甲土块中的空气体积分数为。(3)、若发现V1V2(填“大于”“小于”或“等于”),说明疏松的土地比踩踏过的土地空气含量高。27. “毒大米”事件让人们认识到了重金属污染的危害,重金属在土壤中的分散范围广、隐蔽性强、难清理,现在科学家利用一类超强金属吸收能力的植物(又叫超富集植物)对土壤进行“排毒”。(1)、双子叶的超富集植物,由根系从土壤中吸取重金属,可通过木质茎中的 (填“韧皮部”“木质部”或“形成层”),转移、贮存到枝叶等地上部分。(2)、一种叫做重雪球的植物,富集金属镍的能力很强。通过改良植株增强重雪球的吸镍性,每克干燥的枝叶可含有0.2克镍。对500千克的重雪球的干燥枝叶进行提纯处理,理论上可获得千克的镍。(3)、超富集植物能帮助人们更好地改善由于采矿等原因而恶化的土壤,使耕地重新焕发生机。植物“排毒”具有的优势是(写出一点即可)。28. 绿色植物通过根从土壤中吸收来的水分,绝大部分通过蒸腾作用散失在大气中。下表中的数据显示了一株植物在一天的主要时段内散失水分的量。时间
散失水分的量/克
时间
散失水分的量/克
7:00-8:00
190
17:00-18:00
213
9:00-10:00
209
19:00-20:00
190
11:00-12:00
221
21:00-22:00
100
13:00-14:00
233
23:00-24:00
90
15:00-16:00
227
(1)、水在植物体中运输的基本路径是 (填字母)。A、叶中筛管→茎中筛管→根中筛管 B、根中筛管→茎中筛管→叶中筛管 C、根中导管→茎中导管→叶中导管 D、叶中导管→茎中导管→根中导管(2)、请根据上表中数据可以发现,该株植物一天中散失水分的量最多的时段是;产生这种现象的原因是。(3)、根据上表中的数据,请你推测该株植物的根从土壤中吸收水分的量的变化情况,并说明理由。29. 某同学表演了一个小魔术:取两块等大的萝卜条,各放入等体积的透明液体中,20分钟后,该同学取出萝卜条发现:A烧杯中的萝卜条变硬了,B烧杯中的萝卜条软了.请你帮他分析其中的原因:(1)、“魔术”的奥秘在于A.B烧杯中的液体,他们分别可能是 .A、清水;清水 B、清水;10%盐水 C、10%盐水;10%盐水 D、10%盐水;清水(2)、萝卜条软硬变化的根本原因,在于细胞吸水和失水.以下C.D两幅图哪一副能说明B图中的现象? . (3)、根是陆生植物吸水的主要器官,在根尖结构(E图)中,(选填序号)是根吸收水分的主要部位.(4)、根细胞吸水的根本原因是土壤溶液浓度(大于或小于)根细胞液浓度.(5)、农民伯伯深层施肥,这有利于农作物根系向土壤深处生长,这说明根具有的特性之一是 .
(3)、根是陆生植物吸水的主要器官,在根尖结构(E图)中,(选填序号)是根吸收水分的主要部位.(4)、根细胞吸水的根本原因是土壤溶液浓度(大于或小于)根细胞液浓度.(5)、农民伯伯深层施肥,这有利于农作物根系向土壤深处生长,这说明根具有的特性之一是 .