2016年安徽省阜阳市中考化学二模试卷
试卷更新日期:2016-05-03 类型:中考模拟
一、选择题(共10小题,每小题2分,满分20分)
-
1. 化学与人类生活、生成及可持续发展密切相关,下列说法不正确是( )A、用甲醛溶液浸泡水产品保鲜 B、小苏打受热分解放出二氧化碳,可用作灭火剂的原料 C、回收废旧金属可以节约金属资源,减少环境污染 D、利用洗涤剂具有乳化作用除去餐具上的油污2. 下列食物中能提供大量维生素的是( )A、
 牛奶
B、
牛奶
B、 大米
C、
大米
C、 鸡蛋
D、
鸡蛋
D、 蔬菜
3. 分类是学习和研究化学的常用方法.下列分类中正确的是( )A、有机物:甲烷、乙醇、乙酸(CH3COOH) B、混合物:煤、石油、冰水共存物 C、复合肥料:KNO3、CO(NH2)2 D、合成材料:合成橡胶、合金、合成纤维4. 安徽黄山盛产茶叶.茶叶中含有茶氨酸(C7H14O3N2)、锌、硒等多种成分,茶树适宜在pH为5﹣6的土壤中生长.下列说法不正确的是( )
蔬菜
3. 分类是学习和研究化学的常用方法.下列分类中正确的是( )A、有机物:甲烷、乙醇、乙酸(CH3COOH) B、混合物:煤、石油、冰水共存物 C、复合肥料:KNO3、CO(NH2)2 D、合成材料:合成橡胶、合金、合成纤维4. 安徽黄山盛产茶叶.茶叶中含有茶氨酸(C7H14O3N2)、锌、硒等多种成分,茶树适宜在pH为5﹣6的土壤中生长.下列说法不正确的是( )
A、茶树不宜在碱性土壤中生长 B、茶氨酸由碳、氢、氧、氨四种元素组成 C、茶叶中所含茶氨酸属于有机物,锌、硒属于单质 D、一个茶氨酸分子中含有25个原子5.二甲醚是一种重要的清洁能源,可以替代氟利昂作制冷剂等,对臭氧层没有破坏作用,工业制备二甲醚(CH3OCH3)化学方程式为3CO+3H2
 CH3OCH3+X,下列说法正确的是( )A、X化学式为O2 B、该反应为置换反应 C、反应前后催化剂的性质不变 D、二甲醚完全燃烧产生二氧化碳和水6.
CH3OCH3+X,下列说法正确的是( )A、X化学式为O2 B、该反应为置换反应 C、反应前后催化剂的性质不变 D、二甲醚完全燃烧产生二氧化碳和水6.铬是人体必需的一种微量元素,但铬过量摄入对人体危害非常大,铬的毒性与其存在形式有关.河北、浙江等多地不法厂家生产的“毒胶囊”中主要含有毒性最大的+6价铬元素,如图为有关铬元素的信息,下列说法错误的是( )
 A、毒胶囊中化学成分可能是K2CrO4 B、铬元素属于非金属元素 C、铬元素的相对原子质量为52.00 D、铬的硬度和抗腐蚀性能都很强7.
A、毒胶囊中化学成分可能是K2CrO4 B、铬元素属于非金属元素 C、铬元素的相对原子质量为52.00 D、铬的硬度和抗腐蚀性能都很强7.下列实验操作能达到实验目的是( )
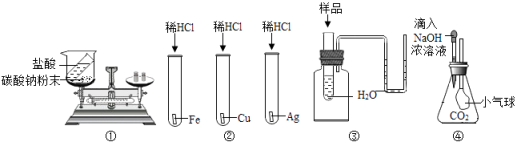 A、①实验可以验证质量守恒定律 B、②实验中可以证明金属活动性为Fe>Cu>Ag C、③U形管中液面变化可以鉴别氯化钠和氢氧化钠 D、④中根据小气球变大可以证明氢氧化钠与二氧化碳发生反应8. 下表列出了除去物质中所含少量杂质的方法,其中正确的选项是( )
A、①实验可以验证质量守恒定律 B、②实验中可以证明金属活动性为Fe>Cu>Ag C、③U形管中液面变化可以鉴别氯化钠和氢氧化钠 D、④中根据小气球变大可以证明氢氧化钠与二氧化碳发生反应8. 下表列出了除去物质中所含少量杂质的方法,其中正确的选项是( )选项
物质
所含杂质
除去杂质的方法
A
铜粉
铁粉
加入过量稀盐酸,过滤
B
二氧化碳
一氧化碳
通入氧气点燃
C
硝酸铜溶液
硝酸银
加入过量铜粉,过滤
D
氢氧化钠溶液
碳酸钠
加入适量稀盐酸
A、A B、B C、C D、D9. 单层石墨称为石墨烯,这种“只有一个碳原子厚的碳薄片”被认为是目前世界上最薄、最坚硬、传导电子速度最快的新型材料,下列关于石墨烯的叙述中正确的是( )A、石墨烯属于化合物 B、石墨烯的化学式为C C、石墨烯中碳元素化合价为+4价 D、石墨烯的硬度小于金刚石10.固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示,下列说法正确的是( )
 A、物质w在乙醇中的溶解度小于其在乙醇中的溶解度 B、t2℃时,物质W溶解在水中和乙醇中的溶质质量分数一定相等 C、t1℃时,mgW分别溶解在100g水和乙醇中,两者都达到了饱和状态 D、将t1℃时物质W的饱和乙醇溶液升温至t2℃,溶质质量分数不变
A、物质w在乙醇中的溶解度小于其在乙醇中的溶解度 B、t2℃时,物质W溶解在水中和乙醇中的溶质质量分数一定相等 C、t1℃时,mgW分别溶解在100g水和乙醇中,两者都达到了饱和状态 D、将t1℃时物质W的饱和乙醇溶液升温至t2℃,溶质质量分数不变二、解答题(共6小题,满分40分)
-
11.
如图是教室里的磁性黑板和黑板擦.
 (1)、属于有机合成材料的是(填编号,一种即可,下同),属于金属材料的是 .(2)、黑板边框由铝合金制成,其优点是较硬、质轻且 , 用化学方程式表示其表面形成氧化物的反应原理 .(3)、墨绿色板是一层不易反光、耐磨易擦且书写流畅的涂层,制作原料之一是磁性材料三氧化二钴,三氧化二钴中钴元素的化合价是 .12.
(1)、属于有机合成材料的是(填编号,一种即可,下同),属于金属材料的是 .(2)、黑板边框由铝合金制成,其优点是较硬、质轻且 , 用化学方程式表示其表面形成氧化物的反应原理 .(3)、墨绿色板是一层不易反光、耐磨易擦且书写流畅的涂层,制作原料之一是磁性材料三氧化二钴,三氧化二钴中钴元素的化合价是 .12.某化学实验小组为了制备少量的氧气.查阅得知双氧水溶液价格最低,在常温下就能够分解放出氧气,该过程中无副产物;氯酸钾价格较高,分解较困难,且常伴有副产物;高锰酸钾价格较高,加热即可快速分解.可供选择的实验装置如图所示:
 (1)、若选择双氧水溶液和二氧化锰混合制备氧气,应选择的发生装置是(填写字母代号),组装好实验装置后因首先进行 .(2)、若选用A装置制取氧气反应的化学方程式是;若采用C装置收集气体,当时开始收集.(3)、你认为在准备工作阶段除应考虑药品的价格、反应的难易、过程的安全性等问题外,还应考虑哪些问题?(至少列举两条) .13.
(1)、若选择双氧水溶液和二氧化锰混合制备氧气,应选择的发生装置是(填写字母代号),组装好实验装置后因首先进行 .(2)、若选用A装置制取氧气反应的化学方程式是;若采用C装置收集气体,当时开始收集.(3)、你认为在准备工作阶段除应考虑药品的价格、反应的难易、过程的安全性等问题外,还应考虑哪些问题?(至少列举两条) .13.安庆高新技术开发区是国家级重点化工基地,园区的泰发新能源科技公司以煤为原料进行如图所示的流程处理,使煤变为清洁能源并生产出其它化工产品.
 (1)、第②步是精煤与水蒸气的反应,其反应类型是 .(2)、第②步生成的产物除了直接做气体燃料和制取甲醇外,还可以利用它们的性来冶炼金属,写出其中一种气体与氧化铁发生反应的化学方程式 .(3)、甲醇与乙醇一样具有可燃性,是一种理想的清洁能源,写出甲醇充分燃烧的化学方程式 .(4)、直接燃煤与煤的深加工综合利用你认为的优点是(答一点即可)14. 某市进行理科实验操作考试,其中化学有关于探究金属的某些物理性质和化学性质的试题,用坩埚钳夹取打磨过的铜片在酒精灯上加热,发现铜片表面变黑,为了探究黑色物质的成分.
(1)、第②步是精煤与水蒸气的反应,其反应类型是 .(2)、第②步生成的产物除了直接做气体燃料和制取甲醇外,还可以利用它们的性来冶炼金属,写出其中一种气体与氧化铁发生反应的化学方程式 .(3)、甲醇与乙醇一样具有可燃性,是一种理想的清洁能源,写出甲醇充分燃烧的化学方程式 .(4)、直接燃煤与煤的深加工综合利用你认为的优点是(答一点即可)14. 某市进行理科实验操作考试,其中化学有关于探究金属的某些物理性质和化学性质的试题,用坩埚钳夹取打磨过的铜片在酒精灯上加热,发现铜片表面变黑,为了探究黑色物质的成分.【查阅资料】①铜的氧化物主要有两种:CuO(黑色);Cu2O(红色)
②酒精在不完全燃烧使会产生炭黑
③炭黑不与稀硫酸反应,也不溶于稀硫酸;氧化铜可与稀硫酸反应而溶解
(1)、【提出假设】猜想1:黑色物质为 .猜想2:黑色物质为炭黑
猜想3:黑色物质为
(2)、【设计方案】操作步骤
实验中可能出现的现象
实验结论
取少量黑色固体于试管中,加入足量(填物质名称)
①
猜想1成立
②黑色固体没有减少,溶液颜色不变
猜想2成立
③
猜想3成立
(3)、【得出结论】通过实验现象,得出猜想3成立,此黑色固体为混合物,请写出实验中发生的化学方程式 .15. 小组在用盐酸和大理石制取二氧化碳时,发现产生气泡的速率不一样,同学们展开了探究.所用盐酸浓度为10%、20%,大理石有细颗粒与粗颗粒两种规格,实验温度为20℃、30℃,每次实验盐酸的用量为100mL、大理石用量为10.0g.【提出问题】盐酸与大理石反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与盐酸浓度有关;b.可能与温度有关;c.可能与大理石规格有关
(1)、【设计并实验】请完成以下实验设计表,并在实验目的一栏中填写对应的实验编号.
实验
编号
温度(℃)
大理石
规格
盐酸浓度(均取100mL)
实验目的
①
20
粗颗粒
20%
(Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响;
(Ⅱ)实验①和探究温度对该反应速率的影响;
(Ⅲ)实验①和探究大理石规格(粗、细)对该反应速率的影响;
②
20
粗颗粒
10%
③
细颗粒
20%
④
粗颗粒
请写出大理石与盐酸反应的化学方程式
(2)、【数据整理】实验①中CO2质量随时间变化的关系如图.

【分析数据】
以上图形中有四条曲线,其中实验③对应的曲线为B,即③﹣B.请写出能反映其它三组实验对应的曲线 , , .
(3)、【拓展】以上方法是通过测量产生气体快慢来判断化学反应的快慢,还可以借助其它反应现象来判断反应的快慢,你认为是 .
16.硝酸钾是重要的农用化肥,也是制造黑火药的原料之一.在某一温度下加热硝酸钾产生了亚硝酸钾(KNO2),同时还产生了一种气体,其化学方程式为2KNO3
 2KNO2+ . (1)、请将上述化学方程式补充完整.(2)、求101g硝酸钾完全分解产生气体的质量.
2KNO2+ . (1)、请将上述化学方程式补充完整.(2)、求101g硝酸钾完全分解产生气体的质量.