2015年湖南省郴州市中考化学真题试卷
试卷更新日期:2016-04-28 类型:中考真卷
一、单项选择题(本题包括20小题,每小题2分,共40分)
-
1. 物质世界在不断变化,下列变化中属于化学变化的是( )
A、晾干衣服 B、食物腐败 C、灯泡发光 D、压榨果汁2. 空气成分中主要含有的两种物质是( )
A、氮气和氧气 B、氮气和氢气 C、二氧化碳和氧气 D、氧气和稀有气体3. 自来水厂的净水过程中没有涉及到的净水方法是( )A、沉淀 B、吸附 C、过滤 D、蒸馏4. 下列各图中是初中化学中常见的几个实验操作,其中错误的是( )
A、 B、
B、 C、
C、 D、
D、 5.
5.在化学反应6CO2+6H2O
 C6H12O6+6O2中没有涉及到的物质类别是( )A、单质 B、氧化物 C、盐 D、有机化合物6. 化学方程式2Na2O2+2H2O=4X+O2↑中X的化学式为( )
C6H12O6+6O2中没有涉及到的物质类别是( )A、单质 B、氧化物 C、盐 D、有机化合物6. 化学方程式2Na2O2+2H2O=4X+O2↑中X的化学式为( )
A、NaOH B、Na2O C、NaH D、Na4(OH)47. 学校禁止吸烟,是因为燃着的香烟产生的烟气有害学生健康,其中含有一种能与血液中血红蛋白结合的有毒气体,它是( )A、CO2 B、CO C、N2 D、SO28. 下列灭火方法不合理的是( )
A、不慎碰倒酒精灯,酒精在桌面上燃烧,立即用湿抹布扑盖 B、森林发生火灾,可砍掉部分树木,形成隔离带 C、堆放杂物的纸箱着火,用水浇灭 D、油锅着火,泼水灭火9. 从环境保护角度考虑,下列燃料中最理想的是( )
A、酒精 B、天然气 C、煤气 D、氢气10. 下列粒子结构示意图中,表示阴离子的是( )A、
B、
B、
C、
C、
D、
D、
11. 下列可用于验证Fe、Cu、Ag三种金属的活动性顺序的一组药品是( )A、Fe、Cu、H2SO4溶液 B、Cu、Ag、FeSO4溶液 C、Fe、Ag、CuSO4溶液 D、Ag、FeSO4溶液、CuSO4溶液12. 下列利用了乳化原理的是( )A、用汽油除去衣服上的油污 B、用稀硫酸除铁锈 C、用洗洁精除去餐具上的油污 D、用盐酸除去水垢13. 下列没有运用中和反应原理的是( )A、服用含氢氧化镁的药物,可以治疗胃酸过多症 B、用熟石灰改良酸性土壤 C、蚊虫叮咬处涂上肥皂水,可减轻痛痒 D、用生石灰做干燥剂14. 下列肥料属于复合肥料的是( )A、NH4NO3 B、KNO3 C、KCl D、Ca(H2PO4)215. 下列食物中富含蛋白质的是( )A、米饭 B、鸡蛋 C、酸豆角 D、苹果16. 下列说法正确的是( )A、在房间里放一盆水可以防止煤气中毒 B、发霉的花生蒸煮后可食用 C、加入活性炭可使硬水变软水 D、用燃烧并闻气味的方法鉴别衣料中的羊毛纤维和棉纤维17. 下列各图象能正确反映其对应变化关系的是( )A、向氢氧化钠溶液中不断加水
11. 下列可用于验证Fe、Cu、Ag三种金属的活动性顺序的一组药品是( )A、Fe、Cu、H2SO4溶液 B、Cu、Ag、FeSO4溶液 C、Fe、Ag、CuSO4溶液 D、Ag、FeSO4溶液、CuSO4溶液12. 下列利用了乳化原理的是( )A、用汽油除去衣服上的油污 B、用稀硫酸除铁锈 C、用洗洁精除去餐具上的油污 D、用盐酸除去水垢13. 下列没有运用中和反应原理的是( )A、服用含氢氧化镁的药物,可以治疗胃酸过多症 B、用熟石灰改良酸性土壤 C、蚊虫叮咬处涂上肥皂水,可减轻痛痒 D、用生石灰做干燥剂14. 下列肥料属于复合肥料的是( )A、NH4NO3 B、KNO3 C、KCl D、Ca(H2PO4)215. 下列食物中富含蛋白质的是( )A、米饭 B、鸡蛋 C、酸豆角 D、苹果16. 下列说法正确的是( )A、在房间里放一盆水可以防止煤气中毒 B、发霉的花生蒸煮后可食用 C、加入活性炭可使硬水变软水 D、用燃烧并闻气味的方法鉴别衣料中的羊毛纤维和棉纤维17. 下列各图象能正确反映其对应变化关系的是( )A、向氢氧化钠溶液中不断加水
B、电解水
B、电解水 C、在恒温条件下,将饱和的NaCl溶液蒸发适量水
C、在恒温条件下,将饱和的NaCl溶液蒸发适量水
D、向一定量的稀盐酸和氯化铜的混合溶液中不断滴入氢氧化钠溶液至过量
D、向一定量的稀盐酸和氯化铜的混合溶液中不断滴入氢氧化钠溶液至过量
18. 下列除杂方法正确的是( )
18. 下列除杂方法正确的是( )选项
物质(括号内为杂质)
除杂方法
A
CO2(CO)
点燃
B
Fe(Cu)
加硫酸铜溶液
C
NaCl(Na2CO3)
加适量稀盐酸
D
CaO(CaCO3)
加水
A、A B、B C、C D、D19. 下列各组离子在pH=1的溶液中能大量共存的是( )A、NH4+ NO3﹣ Na+ Cl﹣ B、CO32﹣ K+ Na+ SO42﹣ C、Cu2+ OH﹣ Cl﹣ Ba2+ D、Ag+ NO3﹣ Cl﹣ Na+20. 某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将50g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( )
A、6g B、8g C、13.2g D、20g二、填空题(本题包括4小题,共20分)
-
21. 用化学用语表示:
(1)2个氧分子 ;
(2)人体中含量最高的金属元素 ;
(3)写出硫酸钠的化学式并标出其中硫元素的化合价 ;
(4)2个亚铁离子 .
22. 用下列常见物质来完成以下各题:(填序号)①干冰 ②葡萄糖 ③石墨 ④硝酸铵固体 ⑤水银
(1)溶于水后溶液温度降低的是 ;
(2)可做干电池电极的是 ;
(3)用于人工降雨的是 ;
(4)温度计中含有的物质是 ;
(5)人体主要的供能物质的是 .
23. 如图是元素周期表的一部分,请回答相关问题:第一周期
1H
2He
第二周期
3Li
4Be
5B
6C
7N
8O
9F
10Ne
第三周期
11Na
12Mg
13Al
14Si
15P
16S
17Cl
18Ar
(1)氟元素与氯元素位于同一纵行的原因是 , 它们在化学反应中都易(填“得到”或“失去”)电子,铝元素与氯元素形成化合物的化学式是 .
(2)M2﹣与Ne核外电子排布相同,则M元素的名称为 . 已知M元素的相对原子质量为a,则M元素原子核内的中子数为 .
24.如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:
(1)若使a、c的饱和溶液同时析出晶体,方法是 .
(2) ℃时,a、c两物质的溶解度相等.气体的溶解度随温度的变化规律与 (填“a”、“b”或“c”)相似.
(3)在t2℃时,a、b、c三种饱和溶液降温至t1℃时溶质的质量分数由大到小的顺序是 ,析出晶体最多的是 (填“a”、“b”或“无法确定”).
(4)在t2℃时,将150克a的饱和溶液稀释成质量分数为20%的溶液需加水 克.

三、简答题
-
25. 化学与生活息息相关.
(1)在农村常用井水作生活用水,加入可检验井水是否为硬水.
(2)下列节水措施正确的是 .
A.农业上改大水漫灌为滴灌 B.用淘米水浇花 C.使用节水龙头 D.用大量的水冲洗汽车
(3)过多的二氧化碳会导致温室效应增强,而绿色植物的却吸收二氧化碳.为减缓温室效应,你的建议是(写一条).
(4)自行车的支架刷有油漆用以防锈,是因为油漆可以使铁与空气中的和隔绝.
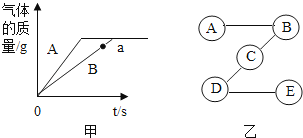
26.(1)等质量的A、B两种物质分别与等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如甲图所示.请回答下列问题:
①若A、B为Mg、Zn中的一种,则A是 , 反应结束后只有一种金属剩余,则剩余金属为 .
②若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,反应结束后,则它们消耗的酸 (填“A多”、“B多”或“相等”).B反应至a点时,所得溶液的溶质为 (写化学式).
(2)如乙图所示,A、B、C、D、E分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A是硝酸铜溶液.(“﹣”相连两物质能发生反应)请回答:
①D的化学式为 ,E物质的一种用途: .
②A与B反应的化学方程式 ,基本反应类型是 .
 27.
27.如图是实验室制取和收集气体的部分装置图.
 (1)、写出装置图中标号仪器的名称:① , ② .
(1)、写出装置图中标号仪器的名称:① , ② .
(2)、用高锰酸钾制取氧气的发生装置为 (填装置字母),该反应的化学方程式为 .(3)、实验室制取二氧化碳,若要收集到纯净干燥的二氧化碳气体,可通过F、G装置除去杂质,则接口顺序:a连( )( )连( )( )连b(填小写字母).28.化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH如下表
溶液
Na2SO4
NaHCO3
Na2CO3
pH
pH=7
pH>7
pH>7
 (1)、小新同学认为该溶液不可能的是 , 理由是 .(2)、标签破损的原因 .(3)、为确定其成分,小新同学设计如下方案进行探究
(1)、小新同学认为该溶液不可能的是 , 理由是 .(2)、标签破损的原因 .(3)、为确定其成分,小新同学设计如下方案进行探究实验步骤
现象
结论
取该溶液少许于试管中,滴加过量的BaCl2溶液,振荡.
①
则该溶液是Na2CO3溶液
过滤,向滤渣滴加稀盐酸.
②
(4)、小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论).29. 丙酸钠是一种常用的食品添加剂,其化学式为C3H5OxNa.已知该化合物中碳元素与氧元素的质量比为9:8,请计算:(1)丙酸钠由 种元素组成;
(2)X= ;
(3)该物质的相对分子质量是 .
30. 一定质量的碳酸钠和氯化钠固体混合物,加入101克水完全溶解后,再往其中加入100g氯化钙溶液,恰好完全反应.过滤,将滤渣干燥,称得其质量为10g,测得滤液中溶质的质量分数为10%.试计算:
(1)、100g氯化钙溶液中溶质的质量;(2)、原固体混合物中碳酸钠的质量分数.31. 已知:镁在空气中燃烧生成氧化镁和氮化镁(Mg3N2),氮化镁与水反应生成氢氧化镁和氨气.(1)、写出氮化镁与水反应的化学方程式 ;(2)、a克镁在空气中完全燃烧生成固体的总质量m为 ;(用含a的式子表示m的取值范围)(3)、某学生对该混合物中氮化镁的质量分数进行测定,设计如下实验装置.

【查阅资料】
Ⅰ.碱石灰是固体氧化钙和氢氧化钠的混合物,常用作干燥剂,不与NH3反应.
Ⅱ.2NH3+H2SO4=(NH4)2SO4
Ⅲ.NH3是一种极易溶于水的气体.
【实验步骤】①检查装置的气密性;②精确称量镁在空气中燃烧后的固体5.00g放入锥形瓶中,称量装置C,连接好装置;③关闭活塞K,打开A中分液漏斗活塞,逐滴加入水,至样品恰好完全反应;④打开活塞K,鼓入空气;⑤再次称量装置C,装置C增重0.34g.请回答:
(一)装置B的作用是;
(二)装置D的作用是 ;
(三)实验步骤④中鼓入空气的目的是;
(四)固体混合物中Mg3N2的质量分数为 ;
(五)实验证明此方法测定的结果偏低,可能原因是(写一条).