2016年济南市市中区中考化学一模试卷
试卷更新日期:2016-04-27 类型:中考模拟
一、单项选择题(每小题2分,共22分)
-
1. 下列过程中没有发生化学变化的是( )A、菜刀生锈 B、榨取果汁 C、火柴燃烧 D、光合作用2. 济南市城市轨道交通的建设时全城人民的生活、工作环境更加便捷、美丽,下列做法中,不利于改善我市环境质量的是( )A、使用清洁能源代替煤和石油 B、提高城市道路机扫率,增加洒水频次,控制道路扬尘 C、提倡使用一次性发泡塑料餐具和塑料袋 D、全面禁止秸秆露天焚烧,加大秸秆综合利用力度3. 下列化学实验操作中,正确的是( )A、稀释稀硫酸时,把浓硫酸慢慢注入成有水的量筒中,并不断搅拌 B、用漏斗过滤时,使用玻璃棒搅拌,加快过滤速度 C、向燃着的酒精灯里添加酒精 D、点燃氢气等可燃性气体前,一定要检验气体的纯度4. 化学与人类健康的关系十分密切.下列做法中,不会危害人体健康的是( )A、用霉变的花生榨取花生油 B、用“干冰”冷藏食品 C、香烟的过滤嘴可滤除CO等有害物质,故吸烟对身体无害 D、青少年正在长身体,应多吃富含蛋白质的肉类,可以不吃蔬菜5.
如图是四种微粒结构示意图,下列有关各微粒的说法中,错误的是( )
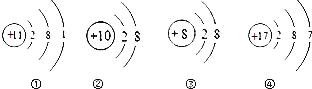 A、①在化合物中的化合价通常为+1价 B、②的化学性质比较稳定 C、③是一种阳离子 D、④容易得到电子6. 下列有关生活、生产常识的说法中,不正确的是( )A、室内放盐水可防止煤气中毒 B、改良酸性土壤可撒熟石灰 C、使用燃煤脱硫技术防止二氧化硫污染 D、高层建筑物起火,不要乘坐电梯,应从安全通道撤离7.
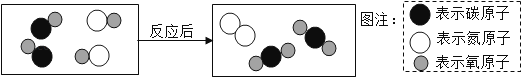
A、①在化合物中的化合价通常为+1价 B、②的化学性质比较稳定 C、③是一种阳离子 D、④容易得到电子6. 下列有关生活、生产常识的说法中,不正确的是( )A、室内放盐水可防止煤气中毒 B、改良酸性土壤可撒熟石灰 C、使用燃煤脱硫技术防止二氧化硫污染 D、高层建筑物起火,不要乘坐电梯,应从安全通道撤离7.如图是表示治理汽车尾气所涉及反应的微观过程,下列说法不正确的是( )
 A、该反应类型为置换反应 B、反应中生成的单质和化合物的质量之比为7:22 C、该反应使有毒气体转化为无毒气体 D、该反应前后氮元素的化合价发生了变化8. 要除去下列物质中的杂质(括号内物质为杂质),下列实验方案设计中合理的是( )A、NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 B、H2(HCl):将气体通过足量氢氧化钠溶液,再经浓硫酸干燥 C、CaO(CaCO3):加水溶解,过滤后洗涤干燥 D、NaOH溶液(Na2CO3):加入适量的CaCl2 , 过滤9. 下列各组物质的鉴别中,所选的鉴别试剂,不正确的是( )
A、该反应类型为置换反应 B、反应中生成的单质和化合物的质量之比为7:22 C、该反应使有毒气体转化为无毒气体 D、该反应前后氮元素的化合价发生了变化8. 要除去下列物质中的杂质(括号内物质为杂质),下列实验方案设计中合理的是( )A、NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 B、H2(HCl):将气体通过足量氢氧化钠溶液,再经浓硫酸干燥 C、CaO(CaCO3):加水溶解,过滤后洗涤干燥 D、NaOH溶液(Na2CO3):加入适量的CaCl2 , 过滤9. 下列各组物质的鉴别中,所选的鉴别试剂,不正确的是( )选项
待鉴别物质
鉴别试剂
A
氢氧化钠溶液和氢氧化钙溶液
二氧化碳
B
鉴别硫酸铵和硫酸钠固体
氢氧化钡溶液
C
食盐溶液和稀盐酸
紫色石蕊
D
氮气和二氧化碳气体
燃着的木条
A、A B、B C、C D、D10. 小明同学为了探究金属与盐溶液的反应规律,将一定质量Fe和Ag组成的混合粉末放入一定量的Cu(NO3)2溶液中,过滤,向滤渣中加入稀盐酸无现象,向滤液中加入铁粉也无现象,小明得出的以下结论中,正确的是( )A、滤液中可能含有Cu2+、Ag+ B、滤渣中一定只含有单质Ag、Cu C、滤液中一定含有Fe3+ D、反应后所得滤渣经洗涤、晾干后,比反应前的固体混合粉末质量减小了11. 将足量的溶质质量分数为20%的盐酸溶液逐渐加入到硫酸钡和碳酸钡组成的100克固体混合物中,直到气体不再产生为止,蒸干后称量所得固体质量为102.2克,则和碳酸钡反应用去的盐酸溶液的质量是( )A、5.25g B、18.25g C、36.5g D、73g二、非选择题(共7小题,共38分)
-
12. 物质的性质决定物质的用途,按要求从氢气、纯碱、硫酸、氧化铜、氢氧化镁、甲烷中选择合适的物质,将其化学式填写在下列空格中.
一种可燃的有机物 ; 一种难溶于水的碱; 一种可作干燥剂的酸 ; 一种可溶于水的盐 .
13. 位于我市西南部的平阴县是全国著名的“玫瑰之乡”,玫瑰花,蔷薇科,落叶灌木,夏季开花“香腻馥郁,愈干愈烈”,玫瑰花中含有多种挥发性物质,主要成分为芳樟醇,化学式为C10H12O2 , 无色液体,既有紫丁香,铃兰与玫瑰的花香,又有木香、果香气息,在全世界每年生产的最常用和用量最大的香料中,芳樟醇几乎年年排在首位.(1)、微粒的观点解释,人们闻到花香气味的主要原因: .(2)、在芳樟醇中,碳元素与氢元素的原子个数比为(填最简答整数比).(3)、玫瑰花的病害主要有,白粉病,锈病,黑斑病、枯枝病、花叶病等,可以在花后每隔半月喷一次一定浓度的波尔多液,逐喷4次,有经验的种植者知道配好的波尔多液盛放在铁桶内会降低药效,请用化学方程式表示其中的原因: .(4)、科学的肥水管理能增强玫瑰的长势,磷酸二氢铵、尿素[CO(NH2)2]、KNO3等化肥的使用,提高了鲜花的产量和质量,下列有关说法中正确的是(填选项序号)①尿素中的氢元素的质量分数最大 ②尿素是一种复合肥
③化肥使用越多越好 ④氨态氮肥不能和碱性物质混合使用.
14.“创新”是一个民族的灵魂,是人类发展的不竭动力.
 (1)、“中国高铁”成了中国创新的一面旗帜,让世人瞩目,高速铁路离不开无缝钢轨,钢铁属于(填“单质”“合金”“复合材料”中的一项)(2)、“改进实验”也是化学实验中的创新,如上图是小明同学在完成铁丝在氧气中燃烧的实验,请指出实验中的不足之处; , 写出铁丝在氧气中燃烧的化学方程式;(3)、我国计划在2020年建成自己的空间站,宇航员呼出的热气,分泌的汗水,潮湿抹布在干燥时产生的水汽,全部都会在空间站上安装的在升冷凝水系统中,转变成引用水,实现名副其实的水循环,水是生命之源,有关水的说法不正确的是(填选项序号)
(1)、“中国高铁”成了中国创新的一面旗帜,让世人瞩目,高速铁路离不开无缝钢轨,钢铁属于(填“单质”“合金”“复合材料”中的一项)(2)、“改进实验”也是化学实验中的创新,如上图是小明同学在完成铁丝在氧气中燃烧的实验,请指出实验中的不足之处; , 写出铁丝在氧气中燃烧的化学方程式;(3)、我国计划在2020年建成自己的空间站,宇航员呼出的热气,分泌的汗水,潮湿抹布在干燥时产生的水汽,全部都会在空间站上安装的在升冷凝水系统中,转变成引用水,实现名副其实的水循环,水是生命之源,有关水的说法不正确的是(填选项序号)①水是最常用的溶剂
②蒸馏水不含杂质,长期饮用有益健康
③水通电分解实验可证明化学反应中分子可分
④水在天然循环过程中发生了物理变化.
15.在工业上用纯碱和石灰石为原料制备,主要流程如图1所示:
 (1)、在①﹣④四个过程中,发生了化合反应的为(填序号).(2)、③中实验操作过程的名称为 , 经搅拌后,得到石灰水.(3)、NaCl、KNO3、Ca(OH)2三物质的溶解度曲线图分别如图2、图3所示,请回答:
(1)、在①﹣④四个过程中,发生了化合反应的为(填序号).(2)、③中实验操作过程的名称为 , 经搅拌后,得到石灰水.(3)、NaCl、KNO3、Ca(OH)2三物质的溶解度曲线图分别如图2、图3所示,请回答:①由图2可知,20℃时,KNO3溶液的溶质质量分数NaCl溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一).
②由图2可知,将20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向其中加入氢氧化钠固体,结合图3分析石灰水中可出现的现象.
16. 如图所示为实验室中常见的气体制备、干燥、净化和收集实验的部分仪器,试根据题目要求,回答下列问题: (1)、若用Zn和稀硫酸反应制取并收集干燥的氢气.
(1)、若用Zn和稀硫酸反应制取并收集干燥的氢气.①所选仪器的连接顺序为: .
②生成氢气时,发生反应的化学方程式为 .
③经测定,装置A中锌粒和稀硫酸反应后溶液的pH7(填“变大”“变小”“不变”之一).
(2)、若以H2O2溶液为原料(MnO2为催化剂)在实验室中制备干燥的氧气,并用来测定,CuO和Cu的混合物样品中CuO的质量分数,仪器的连接顺序为,A→B1→C→B2 , (B1、B2为浓硫酸洗气瓶),并检验装置的气密性,所设计的实验装置中气体流向是从左向右,小明同学取了氧化铜和铜的混合物样品ag,进行实验:①根据完全反应后的C装置的质量变化测定CuO的质量分数,若测得C处大玻璃管内的物质总质量增加bg,则混合物样品中CuO的质量分数(计算结果可为a和b表示的代数式)
②若C处大玻璃管中红色的固体还没有完全消失就测定,则样品CuO的质量分数的测算结果将(填“偏大”“偏小”“不受影响”之一).
③二氧化锰是H2O2溶液制氧气反应的 ,反应后的二氧化锰还可以进行回收重复利用,可采用的操作方法是 ,洗涤,干燥.
17. 一包固体粉末,可能由CaCO3、CuSO4、Na2SO4、NaOH、KCl五种物质中的两种或多种组成,为确定其组成,进行以下实验,请根据实验现象做出分析推理(设过程中所有发生的反应都恰好完全反应).Ⅰ.取一定质量的固体粉末,加适量水搅拌后过滤,得到沉淀A和无色溶液B.
Ⅱ.向所得沉淀A中加入足量稀盐酸,得到无色气体和蓝色溶液.
Ⅲ.取所得无色溶液B加入适量的Ba(NO3)2溶液和足量稀硝酸,然后过滤,得白色沉淀C和无色溶液D.
Ⅳ.取所得无色溶液D,滴入适量AgNO3溶液后又得白色沉淀E和无色溶液F.
根据上述实验过程和发生的现象作出相应推理,填写以下空白:
(1)、白色沉淀E的化学式是 .(2)、无色溶液F中的溶质共有种,肯存在的酸根离子为(写离子符号)(3)、写出步骤Ⅲ中生成白色沉淀C的化学方程式 .(4)、由实验过程及现象还不能判断出该包粉末中含有的物质为(写化学式),得此结论的理由是 .18. 在一烧杯中盛有21.2gCaCO3和CaCl2的粉末状混合物,向其中加入178.8g水,使混合物中的可溶物完全溶解,然后再向其中逐滴加入溶质的质量分数为20%的稀盐酸,烧杯中放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答下列问题:
 (1)、在滴入稀盐酸的过程中,观察到的一条明显实验现象是;(2)、当滴加了20%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式).
(1)、在滴入稀盐酸的过程中,观察到的一条明显实验现象是;(2)、当滴加了20%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式).
(3)、当滴入20%的稀盐酸73g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量(计算结果精确至0.1g).