天津市西青区2020年中考化学一模试卷
试卷更新日期:2020-05-27 类型:中考模拟
一、选择题
-
1. 下列关于空气的说法中,不正确的是( )A、工业上采用分离液态空气法获得氧气 B、二氧化硫是空气污染物之一 C、空气中氧气质量占空气质量的21% D、空气中的氧气来源于绿色植物的光合作用2. 下列变化中,属于化学变化的是( )A、粉笔折断
 B、棉纱织布
B、棉纱织布  C、木材燃烧
C、木材燃烧  D、汽油挥发
D、汽油挥发  3. 下列物质中,属于氧化物的是( )A、O2 B、H2O C、KMnO4 D、Ca(HCO3)24. 下列实验操作正确的是( )A、
3. 下列物质中,属于氧化物的是( )A、O2 B、H2O C、KMnO4 D、Ca(HCO3)24. 下列实验操作正确的是( )A、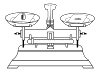 称量氯化钠
B、
称量氯化钠
B、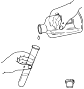 倾倒液体
C、
倾倒液体
C、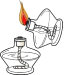 点燃酒精灯
D、
点燃酒精灯
D、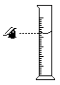 读取液体体积
5. 高铁酸钠(Na2FeO4)是一种“绿色环保高效”的饮用水消毒剂.高铁酸钠中铁元素的化合价为( )A、+2 B、+3 C、+5 D、+66. 在我们生活中有“加碘食盐”“高钙牛奶”等商品,这里的碘、钙应理解为( )A、元素 B、单质 C、分子 D、原子7. 下列利用了乳化原理的是( )A、用汽油除去衣服上的油污 B、用稀硫酸除铁锈 C、用洗洁精除去餐具上的油污 D、用盐酸除去水垢8. 共享单车为了方便我们绿色出行,夏季期间气温升高共享单车的充气轮胎最容易发生爆炸的主要原因是( )
读取液体体积
5. 高铁酸钠(Na2FeO4)是一种“绿色环保高效”的饮用水消毒剂.高铁酸钠中铁元素的化合价为( )A、+2 B、+3 C、+5 D、+66. 在我们生活中有“加碘食盐”“高钙牛奶”等商品,这里的碘、钙应理解为( )A、元素 B、单质 C、分子 D、原子7. 下列利用了乳化原理的是( )A、用汽油除去衣服上的油污 B、用稀硫酸除铁锈 C、用洗洁精除去餐具上的油污 D、用盐酸除去水垢8. 共享单车为了方便我们绿色出行,夏季期间气温升高共享单车的充气轮胎最容易发生爆炸的主要原因是( )
A、分子体积变大 B、分子质量变大 C、分子数目变大 D、分子间的间隙变大9. 下列气体与空气混合后遇明火,可能发生爆炸的是( )
A、甲烷 B、氮气 C、氧气 D、二氧化碳10. 已知A+3B=2C+3D中,已知2.3gA跟4.8gB恰好完全反应生成4.4gC。又知D的相对分子质量为18,则A的相对分子质量为( )
A、23 B、46 C、92 D、9611. 2.4g有机物在足量氧气中完全燃烧,生成6.6gCO2和5.4gH2O,下列说法正确的是( )A、该有机物中一定含有碳、氢元素,可能含有氧元素 B、该有机物只含碳、氢两种元素 C、该有机物中一定含有碳、氢、氧三种元素 D、无法确定12. 下列物质的鉴别方法不正确的是( )A、用燃着的木条鉴别氧气和二氧化碳 B、用水鉴别食盐和碳酸钙粉末 C、用稀盐酸鉴别铜和金 D、用铜片鉴别硝酸银溶液和硫酸锌溶液13. 下列实验的操作、现象、结论均正确的是实验操作
现象
结论
A
向收集满CO2的软塑料瓶中加入约三分之一体积的NaCl溶液,旋紧瓶盖,振荡
塑料瓶变瘪
CO2能与NaCl反应
B
用玻璃棒取少量待测液滴在湿润的pH试纸上,与标准比色卡对照并读出待测液的pH
pH试纸显示pH=1对应的红色
待测液显酸性
C
将白磷浸没在热水中,再向热水中的白磷通氧气
通氧气前白磷不燃烧,通氧气后白磷燃烧
氧气是燃烧需要的条件之一
D
点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯。
烧杯内壁有无色液滴产生
该气体一定是CH4
A、A B、B C、C D、D14. 下列各组药品,可用于验证锌、铁、铜三种金属活动性顺序的是( )A、Zn、Cu、FeSO4溶液 B、Fe、ZnSO4溶液、CuSO4溶液 C、Cu、ZnSO4溶液、FeSO4溶液 D、Fe、Cu、ZnSO4溶液15. 下列说法不正确的是( )A、在化学反应中只有燃烧反应才能放出热量 B、在过氧化氢分解反应中,二氧化锰起催化作用 C、空气中的氮气、氧气经混合,它们的化学性质发生改变 D、向盛有粉尘的金属罐中快速鼓入空气,点火发生爆炸,该粉尘可能是面粉二、非选择题
-
16. 化学就在我们身边。现有①石墨 ②氯化钠 ③稀硫酸 ④碳酸钙 ⑤熟石灰 ⑥二氧化碳,选择适当的物质填空(填序号)。
(1)、可作气体肥料的是。(2)、可用于金属表面除锈的是。(3)、可作补钙剂的是。(4)、可用于配制生理盐水的是。(5)、可作干电池电极的是。(6)、可用于改良酸性土壤的是。17. 请按照要求完成下列各题。(1)、不论是自来水还是纯净水,你认为保持水化学性质的最小粒子是。(2)、今天是小红爸爸的生日:①妈妈为爸爸斟了满满一杯白酒,小红远远就闻到了酒的特殊香味,请从微观的角度解释能闻到香味的原因;爸爸点燃了生日蜡烛。许愿后大家一起将蜡烛吹灭。这种熄灭蜡烛火焰的原理是。
②小红用压岁钱给爸爸买了一条羊毛围巾。日常生活中可以用的方法检验羊毛纤维和合成纤维;妈妈说面粉是制作蛋糕的主要原料,面粉中富含的营养素为。
(3)、航母外壳使用的是钢铁材料井用涂料将钢铁材料覆盖,使用涂料是为了防止钢铁材料与接触而锈蚀。(4)、我国科技迅猛发展,航海及军事领域取得重大突破。建造航母用到了钛合金,工业制钛有一种反应为:TiF4+2H2SO4 4HF+2X+TiO2 , X的化学式为。18. A~H是初中化学常见的物质,其中A为石灰石的主要成分,E为黑色固体,H为蓝色沉淀,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略。回答下列问题: (1)、写出下列物质的化学式:A , E , H.(2)、化学反应常伴有能量变化,物质B与水反应时会(“吸收”或“放出”热量)。(3)、A→B+C的化学反应方程式为(4)、G+F→H的化学反应方程式为19. 构建知识网络是一种重要的学习方法,(1)、将“分子”、“原子”、“元素”填入如图序号所对应的横线上。
(1)、写出下列物质的化学式:A , E , H.(2)、化学反应常伴有能量变化,物质B与水反应时会(“吸收”或“放出”热量)。(3)、A→B+C的化学反应方程式为(4)、G+F→H的化学反应方程式为19. 构建知识网络是一种重要的学习方法,(1)、将“分子”、“原子”、“元素”填入如图序号所对应的横线上。
①②③。
(2)、蔗糖是贮藏在某些植物(如糖、甜菜等)中的糖,其化学式为C12H22O11 , 它由种元素组成,每个蔗糖分子由个原子构成。(3)、根据要求写出相应的化学符号:①锌元素被称为“智力之花”,该元素符号是;
②某种气体在空气中的体积分数占78%,表示出它的8个分子。
20. 按下列要求完成化学方程式(1)、木炭在氧气中燃烧。(2)、过氧化氢溶液与二氧化锰混合。(3)、氢氧化钠和硫酸溶液反应。21. 如图为A,B,C三种固体物质在水中的溶解度曲线示意图,请回答有关问题。 (1)、t1℃时,A,B,C三种固体物质的溶解度分别是a、b、c,则它们由大到小的顺序是;(2)、t1℃时,一定质量的A,C两种固体物质的饱和溶液,当温度由t1℃升高到t2℃时,A物质的溶液中溶质的质量分数(填“增大”、“减小”、“不变”,下同),C物质的溶液中溶质的质量分数。(3)、t1℃时,要使接近饱和的C物质的溶液变为饱和溶液,通常可采用三种方法,它们分别是、、。22. 水是人类宝贵的自然资源。(1)、下列选项中能确认水是由氢元素和氧元素组成的实验是(填序号,下同)。
(1)、t1℃时,A,B,C三种固体物质的溶解度分别是a、b、c,则它们由大到小的顺序是;(2)、t1℃时,一定质量的A,C两种固体物质的饱和溶液,当温度由t1℃升高到t2℃时,A物质的溶液中溶质的质量分数(填“增大”、“减小”、“不变”,下同),C物质的溶液中溶质的质量分数。(3)、t1℃时,要使接近饱和的C物质的溶液变为饱和溶液,通常可采用三种方法,它们分别是、、。22. 水是人类宝贵的自然资源。(1)、下列选项中能确认水是由氢元素和氧元素组成的实验是(填序号,下同)。A 水的蒸馏
B 水的蒸发
C 水的电解
D 水的净化
(2)、天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和(填仪器名称)。(3)、硬水给生活和生产带来很多麻烦,生活中常用的方法降低水的硬度。检验软水和硬水的常用方法是使用。(4)、电解水实验中,如果用va和vb分别表示与负极端和正极端相连的试管中收集到的气体体积,则va:vb的体积比大约是。23. 根据下图所示实验装置进行回答: (1)、写出图中有标号仪器的名称:①。(2)、实验室利用高锰酸钾制取并收集氧气,可选用装置组合,其反应的化学方程式为。收集干燥的氧气需通过多功能装置F,F中应装有 , 氧气需从(填“a”或“b”)端通入。(3)、用完酒精灯后,不能用嘴吹灭,应用灯帽盖灭。为了下次使用时容易打开灯帽,盖灭后应趁热。(4)、实验室制取并收集二氧化碳,可用装置的组合为 , 反应的化学方程式为。24. 溶液具有广泛的用途,根据溶液有关知识,回答下列问题:(1)、在20℃时,向盛有40g氯化钠固体的烧杯中加入100g水,充分搅拌后,仍有4g固体未溶解.
(1)、写出图中有标号仪器的名称:①。(2)、实验室利用高锰酸钾制取并收集氧气,可选用装置组合,其反应的化学方程式为。收集干燥的氧气需通过多功能装置F,F中应装有 , 氧气需从(填“a”或“b”)端通入。(3)、用完酒精灯后,不能用嘴吹灭,应用灯帽盖灭。为了下次使用时容易打开灯帽,盖灭后应趁热。(4)、实验室制取并收集二氧化碳,可用装置的组合为 , 反应的化学方程式为。24. 溶液具有广泛的用途,根据溶液有关知识,回答下列问题:(1)、在20℃时,向盛有40g氯化钠固体的烧杯中加入100g水,充分搅拌后,仍有4g固体未溶解.①所得溶液是20℃时氯化钠的溶液(填“饱和”或“不饱和”)
②20℃时,氯化钠的溶解度为g.
(2)、现用质量分数为12%的氯化钠溶液(密度约为1.09g/cm3),配制20g质量分数为6%的氯化钠溶液.①需要质量分数为12%的氯化钠溶液mL(计算结果精确到0.1),需要水mL(水的密度为1g/cm3).
②该溶液配制过程中用到的仪器除了量筒、烧杯玻璃棒外,还需要量取所需要的12%的氯化钠溶液时,应选用(填“10mL”或“20mL”或“50mL”)规格的量筒.
③把配制好的上述溶液装入中(填“广口瓶”或“细口瓶”),盖好瓶塞并贴上标签.