浙江省杭州市2018-2019学年高二下学期化学期末考试试卷
试卷更新日期:2020-05-26 类型:期末考试
一、选择题
-
1. 2018年3月5日,《Nature》连刊两文报道了21岁的中国留美博士曹原等研究人员制得了具有超导特性的双层石墨烯新材料。以下对石墨烯的推测不正确的是( )A、石墨烯性质稳定,不能在氧气中燃烧 B、石墨烯与石墨都具有导电性 C、石墨烯与金刚石互为同素异形体 D、石墨烯与石墨都具有较高的熔点2. 《梦溪笔谈》是北宋沈括的著作,被誉为“中国科学史上的里程碑”,下列都是摘自该著作的内容,其中没有涉及氧化还原反应的是( )A、烹胆矾则成铜,熬胆矾铁签,久之亦化为铜 B、又石穴中水,所滴皆为钟乳、殷孽 C、鄜、延境内有石油……颇似淳漆,燃之如麻,但烟甚浓 D、取精铁锻之百余火,每锻称之,一缎一轻,至累锻而斤两不减,则纯钢也3. 化学与生活密切相关。下列说法不正确的是( )A、用铁粉作食品袋内的脱氧剂 B、食用一定量的油脂能促进人体对某些维生素的吸收 C、明矾水解时产生具有吸附性的胶体粒子,可作净水剂 D、自行车钢架生锈主要是化学腐蚀所致4. 下列关于实验原理或操作方法的叙述中,正确的是( )A、实验室用乙酸,乙醇和浓硫酸制乙酸乙酯时,必须将温度控制在170℃ B、向滴有酚酞的 溶液中逐滴加 溶液,红色褪去,说明 在水溶液中存在水解平衡 C、实验室金属钠应保存在煤油中,也可保存在无水酒精中 D、可以用澄清石灰水鉴别失去标签的 溶液和 溶液5. 下列物质制备方案可行的是( )A、 B、 C、 D、6. 2019年是国际化学元素周期表年,元素周期表诞生的150年间,指导人们不断探索化学的奥秘。下列有关元素周期表、元素周期律的说法正确的是( )A、元素周期表中,元素性质随着相对原子质量的递增呈现周期性变化 B、同周期主族元素性质的递变,主要是原子半径变化和核电荷数变化双重作用的结果 C、从左到右,同周期非金属元素的气态氢化物,其热稳定性,还原性逐渐增强 D、第七周期,VIIA族元素的非金属性比碘元素的非金属性强7. 下列有关物质结构和性质的表述正确的是( )A、某微粒的结构示意图为
 ,该元素位于周期表第三周期零族
B、工业上用 的反应来制备钾,是因为钠比钾更活泼
C、 的沸点高于 的沸点,原因与 分子间存在氢键有关
D、糖类物质溶液中,蛋白质溶液中加硫酸铵都会产生盐析现象
8. 实验室回收废水中苯酚的过程如图所示。下列说法不正确的是( )
,该元素位于周期表第三周期零族
B、工业上用 的反应来制备钾,是因为钠比钾更活泼
C、 的沸点高于 的沸点,原因与 分子间存在氢键有关
D、糖类物质溶液中,蛋白质溶液中加硫酸铵都会产生盐析现象
8. 实验室回收废水中苯酚的过程如图所示。下列说法不正确的是( ) A、操作Ⅰ为萃取,分液,萃取剂也可以用选用 B、苯酚钠在苯中的溶解度比在水中的小 C、操作Ⅱ中得到的苯,可在操作Ⅰ中循环使用 D、操作Ⅲ中要用蒸馏方法分离出苯酚9. 下列指定反应的离子方程式正确的是( )A、氢氧化镁与盐酸反应: B、将铝片打磨后立即放入氢氧化钠溶液中: C、 溶液中加入足量稀 (必要时可加热): D、硫酸氢铵溶液中滴加少量 溶液:10. 设 为阿伏加德罗常数的值,下列说法正确的是( )A、3.0g甲醛和乙酸的混合物中所含的原子数为 B、 与 充分反应,转移的电子数为 C、 的稀硫酸中含有的氢离子数目为 D、4.6g有机物 的分子结构中碳氢键数目一定为11. 对氨基苯甲酸乙酯是止痛止痒药物的重要成分,其结构简式如图。已知苯环上的氨基具有较强的还原性,下列关于该物质说法不正确的是( )
A、操作Ⅰ为萃取,分液,萃取剂也可以用选用 B、苯酚钠在苯中的溶解度比在水中的小 C、操作Ⅱ中得到的苯,可在操作Ⅰ中循环使用 D、操作Ⅲ中要用蒸馏方法分离出苯酚9. 下列指定反应的离子方程式正确的是( )A、氢氧化镁与盐酸反应: B、将铝片打磨后立即放入氢氧化钠溶液中: C、 溶液中加入足量稀 (必要时可加热): D、硫酸氢铵溶液中滴加少量 溶液:10. 设 为阿伏加德罗常数的值,下列说法正确的是( )A、3.0g甲醛和乙酸的混合物中所含的原子数为 B、 与 充分反应,转移的电子数为 C、 的稀硫酸中含有的氢离子数目为 D、4.6g有机物 的分子结构中碳氢键数目一定为11. 对氨基苯甲酸乙酯是止痛止痒药物的重要成分,其结构简式如图。已知苯环上的氨基具有较强的还原性,下列关于该物质说法不正确的是( ) A、核磁共振氢谱出现5组峰 B、该物质应与酸、碱、氧化剂等分开存储 C、该物质水解后有天然氨基酸生成 D、该物质能发生加成、取代等多种反应12. NaCl是我们生活中必不可少的物质,将NaCl晶体溶于水,其溶解过程示意图如图所示,下列说法正确的是( )
A、核磁共振氢谱出现5组峰 B、该物质应与酸、碱、氧化剂等分开存储 C、该物质水解后有天然氨基酸生成 D、该物质能发生加成、取代等多种反应12. NaCl是我们生活中必不可少的物质,将NaCl晶体溶于水,其溶解过程示意图如图所示,下列说法正确的是( ) A、对比甲、乙两图,图甲中水合b离子的结构示意图不科学 B、图中a离子为 、b离子为 C、氯化钠晶体中存在离子键和分子间作用力 D、水分子对氯化钠晶体表面离子的作用不可能克服离子键的作用13. 科研工作者对甘油(丙三醇)和辛酸合成甘油二酯的酶法合成工艺进行了研究。发现其它条件相同时,不同脂肪酶(Ⅰ号、Ⅱ号)催化合成甘油二酯的效果如图所示,此实验中催化效果相对最佳的反应条件是( )
A、对比甲、乙两图,图甲中水合b离子的结构示意图不科学 B、图中a离子为 、b离子为 C、氯化钠晶体中存在离子键和分子间作用力 D、水分子对氯化钠晶体表面离子的作用不可能克服离子键的作用13. 科研工作者对甘油(丙三醇)和辛酸合成甘油二酯的酶法合成工艺进行了研究。发现其它条件相同时,不同脂肪酶(Ⅰ号、Ⅱ号)催化合成甘油二酯的效果如图所示,此实验中催化效果相对最佳的反应条件是( )
 A、12h,I号 B、24h,I号 C、12h,II号 D、24h,II号14. 常温下,向 溶液中滴加 的氨水,溶液的pH随氨水的体积关系如图所示。下列说法不正确的是( )
A、12h,I号 B、24h,I号 C、12h,II号 D、24h,II号14. 常温下,向 溶液中滴加 的氨水,溶液的pH随氨水的体积关系如图所示。下列说法不正确的是( ) A、HA的电离方程式为 B、B点时加入HA和氨水恰好完全反应 C、A点所示溶液中: D、C点所示溶液中:15. 某小组比较Cl-、Br-、I- 的还原性,实验如下:
A、HA的电离方程式为 B、B点时加入HA和氨水恰好完全反应 C、A点所示溶液中: D、C点所示溶液中:15. 某小组比较Cl-、Br-、I- 的还原性,实验如下:实验1
实验2
实验3
装置
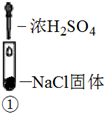
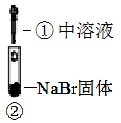
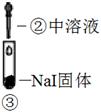
现象
溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟
溶液变黄;把湿KI淀粉试纸靠近试管口,变蓝
溶液变深紫色;经检验溶液含单质碘
下列对实验的分析不合理的是( )
A、实验1中,白烟是NH4Cl B、根据实验1和实验2判断还原性:Br->Cl- C、根据实验3判断还原性:I->Br- D、上述实验利用了浓H2SO4的强氧化性、难挥发性等性质16. 对于反应 在容积为10L的密闭容器中进行。起始时 和 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确的是( ) A、实验c条件下,从反应开始至达到平衡时 B、实验a条件下,用浓度表示的平衡常数为100 C、该反应的 D、比较实验a、c可判断升高温度反应速率加快
A、实验c条件下,从反应开始至达到平衡时 B、实验a条件下,用浓度表示的平衡常数为100 C、该反应的 D、比较实验a、c可判断升高温度反应速率加快二、填空题
-
17. X、Y、Z为元素周期表中原子序数依次增大的三种短周期元素,Y与X、Z均相邻,X、Y与Z三种元素原子的最外层电子数之和为19;W的单质为生活中一种常见的金属,在Z元素的单质中燃烧产生棕黄色的烟,生成 。回答下列问题:(1)、Z元素在元素周期表中的第周期。(2)、 与足量的 的水溶液发生反应生成两种强酸,写出该反应的离子方程式。(3)、 易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是 , 判断的依据是。18. 据不完全统计,全世界每年约有10%~20%的农副产品,水产品会因腐败变质而无法食用,经济损失巨大,所以研究安全无害的食品防腐剂很重要,山梨酸及其盐,尼泊金酯等可作为食品防腐剂,其结构简式如图:
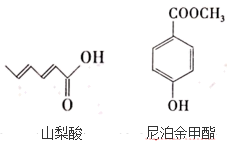
按要求回答下列问题:
(1)、写出山梨酸中含氧官能团的名称。(2)、常温下,等物质的量的山梨酸、尼泊金甲酯分别与足量溴水反应,消耗Br2的物质的量之比为。(3)、写出尼泊金甲酯与NaOH溶液反应的化学方程式。19. 人体的血液的pH需控制在7.35~7.45之间,过高过低都会引起身体不适,甚至危及生命。人体血液能维持在稳定的pH范围主要是人血浆中一定浓度的 和 起调节作用。按要求回答下列问题。(1)、用离子方程式解释血液呈弱碱性的原因;(2)、当血液的 (即 浓度为 )时, 和 浓度比值约为20:1,计算此时碳酸的 ;查阅资料得常温下碳酸的 ,解释与计算所得数据存在差异的原因。20. 某铜制品在潮湿环境中发生的电化学腐蚀过程可表示为如图,腐蚀后有A物质生成,某小组为分析A物质的组成,进行了如下实验:实验①:取A样品,加过量稀硝酸完全溶解后,再加入 溶液,有白色沉淀生成。
实验②:另取A样品4.29g,加入含 的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
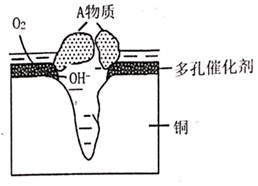 (1)、该粉状锈中除了铜元素外还含有(写元素符号)元素,该铜制品发生电化学腐蚀生成粉状锈时其正极电极反应式为。(2)、写出该粉状锈溶于稀硫酸反应的离子方程式。(3)、加热条件下,实验②中所得的黑色固体能与乙醇反应,化学方程式为。21. 某种半水煤气中主要含 、CO、 、 和少量 ,经“脱硫”、转换反应可制得合成氨原料气。(1)、这种半水煤气跟空气按一定比例混合后通入 、 的混合溶液中完成“脱硫”,其转化过程如图所示,该过程中发生多个反应,总反应为 ,该转化过程中起催化作用的离子为 , 写出该过程中属于非氧化还原反应的离子方程式。
(1)、该粉状锈中除了铜元素外还含有(写元素符号)元素,该铜制品发生电化学腐蚀生成粉状锈时其正极电极反应式为。(2)、写出该粉状锈溶于稀硫酸反应的离子方程式。(3)、加热条件下,实验②中所得的黑色固体能与乙醇反应,化学方程式为。21. 某种半水煤气中主要含 、CO、 、 和少量 ,经“脱硫”、转换反应可制得合成氨原料气。(1)、这种半水煤气跟空气按一定比例混合后通入 、 的混合溶液中完成“脱硫”,其转化过程如图所示,该过程中发生多个反应,总反应为 ,该转化过程中起催化作用的离子为 , 写出该过程中属于非氧化还原反应的离子方程式。 (2)、脱硫后的半水煤气与水蒸气以1:15比例混合后通入转换塔中,变换反应为: 。该反应用氧化铁作催化剂,其活性组分是四氧化三铁。研究发现,变换反应经下列两步完成:
(2)、脱硫后的半水煤气与水蒸气以1:15比例混合后通入转换塔中,变换反应为: 。该反应用氧化铁作催化剂,其活性组分是四氧化三铁。研究发现,变换反应经下列两步完成:第一步: (慢反应)
第二步: (快反应)
①在下图中绘制变换反应(经上述催化反应过程)的“能量~反应过程”示意图。

②由于 和CO还原性较强,能够将氧化铁直接还原成铁而使催化剂失活,但实际生产中一般不会发生这种情况,请从反应速率,化学平衡角度解释可能的反应过程原因是。
(3)、半水煤气处理后得到的混合气中,可通过在熔融碳酸盐中经电化学还原消除其中的二氧化碳,并得到高纯度的碳,写出生成碳的电极反应式为。22. 盐酸多巴胺可用作选择性血管扩张药,是临床上常有的抗休克药。某研究小组按如下路线合成盐酸多巴胺。
已知:
a.
b.
按要求回答下列问题:
(1)、B的结构简式。(2)、下列有关说法正确的是____。A、有机物A能与 溶液反应产生无色气体 B、反应①、②、③均为取代反应 C、有机物F既能与HCl反应,也能与NaOH反应 D、盐酸多巴胺的分子式为(3)、盐酸多巴胺在水中的溶解性比多巴胺( )强的原因是。 (4)、写出多巴胺(分子式为 )同时符合下列条件的所有同分异构体的结构简式。
)强的原因是。 (4)、写出多巴胺(分子式为 )同时符合下列条件的所有同分异构体的结构简式。①分子中含有苯环,能使氯化铁溶液显色
②H–NMR谱和IR谱显示分子中有4种化学环境不同的氢原子,没有-N-O-键
(5)、设计以 和 为原料制备 的合成路线(用流程图表示,无机试剂任选)。23. 高纯无水 是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是 ,含少量 杂质)为原料,以乙二醇为溶剂,采用氨络合法制备 (白色块状固体或粉末,溶于水,易潮解),再转化为无水 的新工艺,其流程图如图:
已知:①常压下, 的初始分解温度为399℃, 的初始分解温度为896℃;
②煅烧温度是影响MgO活性的关键因素;
③乙二醇的沸点197.3℃。
(1)、步骤Ⅰ中工业上一般不选择800℃以上来完成这一步原因是。(2)、步骤Ⅱ中反应方程式为。(3)、步骤IV中蒸馏的目的是。(4)、步骤V中的洗涤是为了除去晶体表面的杂质,最好选用下列哪种作为洗涤剂____。A、氯化铵饱和溶液 B、乙二醇 C、冷水 D、氨气饱和的乙醇溶液(5)、实验过程需要测定 浓度,可通过EDTA滴定(与 以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→→e(用操作步骤前的字母表示)。a.移取25.00mL待测溶液于锥形瓶中,加入10mL水,摇匀
b.用0.1000mol/L的EDTA标准溶液滴定至终点,记录消耗标准液的体积
c.称取一定质量的样品,配制250mL待测溶液
d.滴加1-2滴指示剂
e.舍弃不可靠数据、取平均值等