甘肃省永昌县2019年中考化学一模试卷
试卷更新日期:2020-05-14 类型:中考模拟
一、选择题
-
1. 下列物质的名称、俗名或主要成分与化学式对应不正确的是( )A、氯化钠 食盐 NaCl B、碳酸氢钠 纯碱 NaHCO3 C、氧化钙 生石灰 CaO D、氢氧化钠 火碱 NaOH2. 一些食物的近似pH如下:
食物
葡萄汁
苹果汁
牛奶
鸡蛋清
pH
3.5~4.5
2.9~3.3
6.3~6.6
7.6~8.0
其中显碱性的食物是( )
A、葡萄汁 B、苹果汁 C、牛奶 D、鸡蛋清3. 某化学课外活动小组开展下列实验活动:取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔5分钟测一次pH,其数据如下表所示。下列对测定结果的分析中正确的是( )测定时刻
17∶05
17∶10
17∶15
17∶20
17∶25
17∶30
17∶35
pH
4.95
4.94
4.92
4.88
4.86
4.85
4.85
A、在测定期间,该雨水的酸性逐渐减弱 B、该雨水对农作物的生长没有影响 C、若在17:40测定,pH一定小于4.85 D、pH=4.95与某些工厂排放的酸性气体有关4. 由表中提供的信息判断,衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如下表所示:洗净衣服上的碘污渍的最佳选择是( )溶质
碘
溶剂
水
酒精
汽油
苯(有毒)
溶解性
微溶
可溶
易溶
易溶
A、水 B、酒精 C、汽油 D、苯5. 园林工人在树干下部涂上一层石灰浆,这里石灰浆的作用是( )A、美观大方 B、杀菌作用 C、标记作用 D、以上说法都不对6. 下列生产实践中,没有用熟石灰的是( )A、降低土壤的酸性,改良土壤 B、建筑工业上制三合土 C、干燥气体 D、处理工厂中含硫酸的废水7. 人的汗液中含有盐分,法医做指纹实验,常用某溶液喷洒指纹,该溶液是( )A、酒精 B、碘酒 C、AgNO3溶液 D、BaCl2溶液8. 厕所清洁剂的主要成分是盐酸,炉具清洁剂的主要成分是氢氧化钠.关于这两种清洁剂的叙述正确的是( )A、测得厕所清洁剂的pH=13 B、测得炉具清洁剂的pH=1 C、厕所清洁剂能使紫色石蕊溶液变蓝 D、炉具清洁剂能使无色酚酞溶液变红9. 下列药品需要密封保存的原因,解释不正确的是( )A、浓盐酸—— 防止挥发 B、氢氧化钠溶液 ——防止与二氧化碳反应 C、浓硫酸 ——防止吸水 D、生石灰 —— 防止与氧气反应10. 中和反应广泛应用于生活和生产中,下列做法不科学的是( )A、用熟石灰改良酸性土壤 B、印染厂的废水呈碱性,可加入硫酸进行处理 C、蚊虫在叮咬人的过程中会分泌出一种酸,可用氢氧化钠溶液擦拭 D、新制的松花蛋往往因为碱性过重而带有涩味,食用时可加适量的食醋11. 以下是一些食物的近似pH:①苹果3.3~4.5 ②鸡蛋清7.6~8.0 ③番茄4.0~4.4 ④玉米粥6.8~8.0 ⑤柑橘汁3.4~4.2,胃酸过多的人宜经常食用的是( )A、①④ B、④⑤ C、②④ D、③⑤12. 在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,充分反应后过滤,留在滤纸上的物质中一定含有( )A、Cu B、Ag C、Cu、Ag D、Zn、Ag13. 某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛.在氢氧化镁与胃酸作用的过程中,胃液pH变化的情况是( )A、 B、
B、 C、
C、 D、
D、 14. 下列各组物质中,不能发生复分解反应的是( )A、氢氧化钠和盐酸 B、碳酸钠和硫酸 C、氯化钡和硫酸铜 D、硝酸钠和氯化钾15. 下列物质在使用过程中与化学性质无关的是( )A、用小苏打治疗胃酸过多 B、用食醋除去暖水瓶中的水垢 C、用干冰进行人工降雨 D、用熟石灰改良酸性土壤16. 推理是一种重要的化学思维方法,以下推理合理的是( )
14. 下列各组物质中,不能发生复分解反应的是( )A、氢氧化钠和盐酸 B、碳酸钠和硫酸 C、氯化钡和硫酸铜 D、硝酸钠和氯化钾15. 下列物质在使用过程中与化学性质无关的是( )A、用小苏打治疗胃酸过多 B、用食醋除去暖水瓶中的水垢 C、用干冰进行人工降雨 D、用熟石灰改良酸性土壤16. 推理是一种重要的化学思维方法,以下推理合理的是( )
A、单质中只含有一种元素,但是只含有一种元素的物质不一定是单质 B、中和反应一定有盐生成,所以有盐生成的反应一定是中和反应 C、H2O和H2O2的组成元素相同,所以它们的化学性质相同 D、氧化物一定含氧元素,含氧元素的物质一定是氧化物17. 有一种“即热即食型食品”适合外出旅游时使用,其内层用铝箔包装食品,外层则是包装两种化学物质。使用预留在外的开关,使两种物质发生化学反应,此时便可以对食品进行加热,这两种化学物质最适合的选择是( )A、熟石灰与水 B、浓硫酸与水 C、食盐与水 D、生石灰与水18. 下列物质长时间敞口放置在空气中,质量增加并发生化学反应的是:①烧碱 ②生石灰 ③浓盐酸 ④浓硫酸 ⑤熟石灰 ⑥铁钉( )A、①②④ B、①②⑤ C、①②⑤⑥ D、①②④⑤⑥19. X、Y、Z、W是四种不同的金属,为比较金属活动性的强弱,某同学利用这四种金属单质、盐酸、Z的硝酸盐、W的硝酸盐,进行有关实验,结果如下表(能发生置换反应的记为“√”,不能反应的记为“一”,无标记的表示未做该实验)。这四种金属的活动性顺序为 ( )X
Y
Z
W
盐酸
√
—
—
√
Z的硝酸盐
√
W的硝酸盐
√
—
A、X>W>Y>Z B、X>Y>W>Z C、W>X>Y>Z D、Y>W>Z>X20. 下列离子组能在pH=1的无色溶液中大量共存的是( )
A、NO3- Fe3+ Na+ OH- B、K+ SO42- Na+ NO3- C、Cl- K+ SO42- Ba2+ D、Ca2+ Cl- CO32- Na+21. 镧(La)是一种活动性比锌更强的元素,它的氧化物的化学式为La2O3 , La(OH)3是不溶于水的碱,而LaCl3、La(NO3)3都可溶于水。由此判断下列几组物质,不能直接反应制取LaCl3的是A、La(OH)3和 HCl B、La2O3和 HCl C、La 和 HCl D、NaCl 和 La(OH)322. 向烧杯中逐滴加入x溶液至过量(图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )
烧杯中的物质
x溶液
A
HCl和FeCl3溶液
NaOH溶液
B
碳酸氢钠和氯化钠溶液
稀HCl
C
镁铝合金
稀HCl
D
稀盐酸和稀硫酸
BaCl2溶液
A、A B、B C、C D、D23. 有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④FeCl3 , 不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是( )A、④③②① B、④①②③ C、①③④② D、①④②③24. 分离、提纯是化学实验的重要环节,下列实验设计不能达到实验目的的是( )选项
实验目的
实验设计
A
除去CO中的少量H2O和CO2
先通过浓硫酸,再通过氢氧化钠溶液
B
除去NaCl固体中的少量Na2CO3
先加足量水溶解,再加适量稀盐酸,蒸发结晶
C
除去KNO3溶液中的少量K2SO4
加入适量的Ba(NO3)2溶液,过滤
D
除去铜粉中混有的少量铁粉
用磁铁吸引
A、A B、B C、C D、D25. 如图所示,处于连线两端的物质,在一定的条件下都能发生化学反应的物质组别是( )
甲
乙
丙
丁
A
C
O2
H2SO4
CuO
B
Fe
H2SO4
CuCl2
NaOH
C
NaOH
CO2
KOH
CuCl2
D
Na2SO4
Ba(OH)2
HCl
Ba(NO3)2
A、A B、B C、C D、D二、非选择题
-
26. 在H、O、C、Cl、Na、Ca六种元素中选择适当元素,组成符合下列要求的物质,将其中化学式填入空格中。(1)、人工降雨的氧化物;(2)、可用于金属表面除锈的酸;(3)、改良酸性土壤的碱;(4)、可用作发酵粉和治疗胃酸过多症的是;(5)、可做建筑材料的盐;(6)、可消除公路积雪的盐。27. 在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
 (1)、室温时,(选填“甲”、“乙”或“丙”)溶液可能是不饱和溶液.(2)、图2中能表示乙物质的溶解度曲线的是(填“a”、“b”或“c”,下同。)(3)、t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中水的质量由大到小的顺序是(4)、小强同学要在实验室配制15%的氯化钠溶液50g.需要氯化钠的质量为克,该同学按下图所示步骤依次操作:
(1)、室温时,(选填“甲”、“乙”或“丙”)溶液可能是不饱和溶液.(2)、图2中能表示乙物质的溶解度曲线的是(填“a”、“b”或“c”,下同。)(3)、t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中水的质量由大到小的顺序是(4)、小强同学要在实验室配制15%的氯化钠溶液50g.需要氯化钠的质量为克,该同学按下图所示步骤依次操作: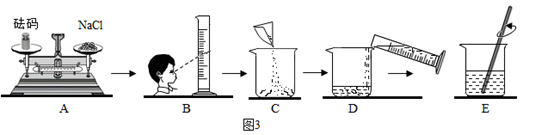
其中操作不正确的步骤是(填字母);E中玻璃棒的作用是 . 若上图A中砝码的质量为5g,游码为2.5g,则小明称得的氯化钠质量实际为克.
28. 下列是初中化学中常见的物质:铁、氢气、氧化铜、二氧化碳、硫酸、氢氧化钠、氯化铜。它们进行击鼓传花游戏,条件是相互之间能发生反应就可以进行传递。请把上述物质分别安排在A~G的位置上,使花束能从A传到G。其中A的固本俗称干冰。请回答: (1)、氢氧化钠应放在位置上。(2)、C和D反应的化学方程式为 , 反应类型为反应。
(1)、氢氧化钠应放在位置上。(2)、C和D反应的化学方程式为 , 反应类型为反应。上述物质除了发生从A到G的化学反应外,常温下还能相互发生化学反应的是(写名称)。
(3)、当G换成另一个同类别物质时就能将花传回起点A,它是(写名称)。29. 请你根据所学知识并结合下图所示装置回答有关问题: (1)、指出标号仪器的名称:①;②。(2)、用高锰酸钾制取氧气的化学方程式为 , 应选择的发生装置是 , 可以用E装置收集氧气的原因是 , 当观察到现象时,说明氧气已收满;集满氧气的集气瓶应(填“正”或“倒”)放在桌面上。(3)、制取并收集一定量的二氧化碳,应选择的发生装置是 , 欲制得干燥的二氧化碳,还需将气体通过盛有(填药品名称)的洗气瓶F。(4)、用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量水的原因是 , H中喷有紫色石蕊溶液的纸花显色。(5)、兴趣小组用纯净干燥的氢气和金属钙制取氢化钙,所选装置图如下:
(1)、指出标号仪器的名称:①;②。(2)、用高锰酸钾制取氧气的化学方程式为 , 应选择的发生装置是 , 可以用E装置收集氧气的原因是 , 当观察到现象时,说明氧气已收满;集满氧气的集气瓶应(填“正”或“倒”)放在桌面上。(3)、制取并收集一定量的二氧化碳,应选择的发生装置是 , 欲制得干燥的二氧化碳,还需将气体通过盛有(填药品名称)的洗气瓶F。(4)、用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量水的原因是 , H中喷有紫色石蕊溶液的纸花显色。(5)、兴趣小组用纯净干燥的氢气和金属钙制取氢化钙,所选装置图如下:
查阅资料:
①钙易与水反应生成碱和气体。
②无水氯化钙能作干燥剂。
(Ⅰ)请按气流方向连接顺序i接 , 接 , 接 , k接a.(填仪器接口的字母编号)。写出C中可能发生的化学方程式。
(Ⅱ)实验结束后,某同学取少量生成物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色。该同学据此判断,上述实验的确有CaH2生成。另一位同学认为该同学的判断不准确,原因是。
(Ⅲ)氢化钙作为能源提供剂,与直接用氢气相比,其优点是。
30. 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。(1)、(演示实验)将一定量稀盐酸加入到盛有氢氧化钙溶液的小烧杯中。该反应的化学方程式是。(2)、(查阅资料)CaCl2溶液显中性(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2
猜想Ⅱ:有
猜想Ⅲ:有CaCl2和Ca(OH)2
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
(3)、乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是。(4)、(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。实验方案
滴加紫色
石蕊溶液
通入CO2
滴加
Na2CO3溶液
实验操作



实验现象
产生白色沉淀
实验结论
溶液中含有Ca(OH)2
溶液中含有Ca(OH)2
溶液中含有Ca(OH)2
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(5)、(评价反思)①丙组同学认为滴加Na2CO3溶液产生沉淀,并不能证明溶液中一定含有Ca(OH)2 , 请你帮助他们说明原因。
②在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑。
31. 将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答: (1)、a点溶液中大量存在的离子有;(2)、计算稀盐酸中溶质的质量分数(3)、当恰好完全反应时,所得溶液的溶质质量分数?
(1)、a点溶液中大量存在的离子有;(2)、计算稀盐酸中溶质的质量分数(3)、当恰好完全反应时,所得溶液的溶质质量分数?