2016年四川省成都市高新区中考化学一诊试卷
试卷更新日期:2016-04-25 类型:中考模拟
一、选择题(每小题3分,共42分)
-
1. 李林同学在不同季节的制作过程中,一定发生了化学变化的是( )A、春天花朵掰成花瓣 B、夏天粮食酿成美酒 C、秋天水果榨成果汁 D、冬天冰砖凿成冰雕2. 下列对氧气的各种叙述中,不正确的是( )A、氧气参加的化学反应都是化合反应 B、液态氧用于火箭发动机,以促使燃料迅速燃烧 C、氧气的化学性质比较活泼,可与许多金属与非金属反应 D、在钢铁冶炼中,吹入富氧空气可以提高炉温,加速冶炼过程3. 下列灭火方法是利用“降温到着火点以下”原理熄灭蜡烛的是( )A、
 B、
B、 C、
C、 D、
D、 4. 下列有关溶液的说法不正确的是( )A、可口可乐汽水和白蒲黄酒都属于溶液 B、固体物质的溶解度不一定都随温度升高而增大 C、一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液 D、某物质在100g溶剂里达到饱和状态时所溶解的质量就是该物质的溶解度5. 2011年3月22日是第十九届“世界水日”,联合国确定今年“世界水日”的宣传主题是“城市用水:应对都市化挑战”.下列用水行为符合节水的是( )
4. 下列有关溶液的说法不正确的是( )A、可口可乐汽水和白蒲黄酒都属于溶液 B、固体物质的溶解度不一定都随温度升高而增大 C、一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液 D、某物质在100g溶剂里达到饱和状态时所溶解的质量就是该物质的溶解度5. 2011年3月22日是第十九届“世界水日”,联合国确定今年“世界水日”的宣传主题是“城市用水:应对都市化挑战”.下列用水行为符合节水的是( )①将工业冷却水进行循环利用 ②用未经处理的工业废水灌溉农田 ③利用太阳能、离子交换树脂、半透膜等技术,使海水淡化
④用喷淋节水龙头代替用水较多的旧式龙头 ⑤用大量的水冲洗汽车代替人工擦洗.
A、②③④ B、①③④ C、③④⑤ D、①②⑤6.将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为2Mg+CO2
 2MgO+C,下列有关叙述错误的是( )A、该反应中Mg发生了氧化反应 B、镁条着火不能用CO2扑灭 C、该反应的实验现象是生成白色的氧化镁和黑色的碳 D、燃烧并不一定需要氧气7. 下列关于金属的说法正确的是( )A、波尔多液的配制可以在铁质容器中进行 B、铝制品抗腐蚀能力较铁制品强 C、用FeSO4溶液、Cu和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序 D、铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O48. 下列方法可使海水转化为饮用水的是( )A、过滤 B、静置沉淀 C、活性炭吸附 D、蒸馏9. 将混有少量高锰酸钾的铜绿固体混合物,放入试管中加热,完全反应后,试管中剩余固体共有( )A、2种 B、3种 C、4种 D、5种10. 下列各项:①原子的数目;②分子的数目;③元素的种类;④物质的种类;⑤物质的分子个数;⑥各种原子的总数;⑦反应物和生成物的总质量.在化学反应前后,肯定没有变化的是( )A、②③⑤ B、①⑥ C、①③⑥⑦ D、①③⑥11. 把甲、乙、丙三种金属分别加入稀硫酸中,甲、乙表面有气泡产生,丙无变化;再把甲放到乙的硫酸盐溶液中,甲表面析出乙.则三种金属的活动性顺序是( )A、甲>乙>丙 B、乙>甲>丙 C、丙>甲>乙 D、丙>乙>甲12.
2MgO+C,下列有关叙述错误的是( )A、该反应中Mg发生了氧化反应 B、镁条着火不能用CO2扑灭 C、该反应的实验现象是生成白色的氧化镁和黑色的碳 D、燃烧并不一定需要氧气7. 下列关于金属的说法正确的是( )A、波尔多液的配制可以在铁质容器中进行 B、铝制品抗腐蚀能力较铁制品强 C、用FeSO4溶液、Cu和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序 D、铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O48. 下列方法可使海水转化为饮用水的是( )A、过滤 B、静置沉淀 C、活性炭吸附 D、蒸馏9. 将混有少量高锰酸钾的铜绿固体混合物,放入试管中加热,完全反应后,试管中剩余固体共有( )A、2种 B、3种 C、4种 D、5种10. 下列各项:①原子的数目;②分子的数目;③元素的种类;④物质的种类;⑤物质的分子个数;⑥各种原子的总数;⑦反应物和生成物的总质量.在化学反应前后,肯定没有变化的是( )A、②③⑤ B、①⑥ C、①③⑥⑦ D、①③⑥11. 把甲、乙、丙三种金属分别加入稀硫酸中,甲、乙表面有气泡产生,丙无变化;再把甲放到乙的硫酸盐溶液中,甲表面析出乙.则三种金属的活动性顺序是( )A、甲>乙>丙 B、乙>甲>丙 C、丙>甲>乙 D、丙>乙>甲12.甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )
 A、依据溶解度曲线可判断:甲的溶解度比乙的大 B、将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 C、将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法 D、t1℃时,甲和乙的饱和溶液各100g,其溶质的溶解度相等13.
A、依据溶解度曲线可判断:甲的溶解度比乙的大 B、将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 C、将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法 D、t1℃时,甲和乙的饱和溶液各100g,其溶质的溶解度相等13.下列实验方案及现象与结论一致的是( )
项目
A
B
C
D
方案




现象
蜡烛由低到高依次熄灭
干冷烧杯内壁出现无色液滴,澄清石灰水变浑浊
振荡后,塑料瓶变瘪
水中的铁钉生锈,植物油中的铁钉没生锈
结论
一般情况下,二氧化碳不燃烧也不支持燃烧,密度比空气大
气体中一定有碳、氢元素、氧元素
二氧化碳能溶于水也能和水发生反应
铁生锈只需要与氧气接触
A、A B、B C、C D、D14.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图.下列说法中不正确的是( )
 A、该反应为分解反应 B、丙可能为该反应的催化剂 C、参加反应的乙、丁质量比为3:2 D、丁相对分子质量是甲的2倍
A、该反应为分解反应 B、丙可能为该反应的催化剂 C、参加反应的乙、丁质量比为3:2 D、丁相对分子质量是甲的2倍二、填空题(共26分)
-
15. 矿泉水中元素及国标含量如表所示,请用化学用语回答下列问题.
矿物质水中主要成分(mg/1L)
偏硅酸(H2SiO3)≥25
钙≥0.2
硫酸根≥0.05
钠≥0.2
氯离子≤5
镁≥0.2
①矿泉水中含有的镁元素;
②久置的水中溶有一定量的氧气,请表示出n个氧分子;
③表中的一种阴离子等;
④硫酸钙中钙元素的化合价 .
16. 亮亮做家务时接触到下列用品.脱氧剂
洁厕灵
炉灶清洁剂
有效成分
还原铁粉
盐酸
氢氧化钠(分解油污,有强烈的腐蚀性)
(1)、他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是: , 生锈的化学式是 , 把还原铁粉在纯氧中燃烧,生成物黑色的(填化学式);(2)、他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理.(3)、他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是 .17. 归纳与比较,是学习化学的重要方法之一,对比CO和CO2 , 它们的组成元素(填“相同”或“不同”,下同),但它们的化学性质:工业上CO可用来炼铁,请写出反应的化学方程式 , 废气不能随意排放,处理方法是 .18. 铝具有良好的抗腐蚀性,请用化学方程式解释原因 .19. 遂宁市新增“中国红海”和“圣莲岛湿地公园”两处4A级景区,初三、二班的几位同学在一个周末实地感受了圣莲岛湿地公园之美.(1)、刚进入公园,阵阵花香便扑鼻而来,让几位同学兴奋不已,用微粒观点解释闻到花香是因为;(2)、随后他们来到了天桥,发现坚固的钢材表面喷上了红色漆,在阳光下分外耀眼,同学们感叹:“这颜色真美!”,喷漆的主要目的是为了防止;(3)、大伙一路谈笑,口渴了,拿出随身带来的塑料瓶装的矿泉水,饮后观察了标签,上面有一项写着:含钙、镁、钠、钾等成分,这里的“钙”、“镁”、“钠”、“钾”指的是(填“原子”、“离子”、“元素”、“物质”): .20. 生活中处处有化学,化学与生活密切相关.(1)、某饼干包装袋中用干燥剂的是生石灰,请用化学方程式表示其原理.(2)、森林火灾时,常砍伐处一条隔离带的目的是 .(3)、我们常用洗涤剂洗涤餐具上的油污,这是因为洗涤剂具有功能,用汽油洗油污属现象,(4)、雾霾是一种灾害性天气现象,由于人类生产、生活向大气中排放大量细颗粒物,如果超过大气的自净能力,就会出现雾霾现象.请分析下列污染物中,会导致雾霾的是(填序号)( )A、二氧化碳 B、臭氧 C、一氧化碳 D、PM2.5(5)、厨房中的下列物品锁使用的主要材料属于金属材料的( )A、不锈钢炊具 B、橡胶手套 C、纯棉围裙(6)、天然气作燃料 (用化学方程式表示).(7)、根据如图所提供的信息,写出在催化式排气净化器中发生的一个反应(用化学方程式表示).
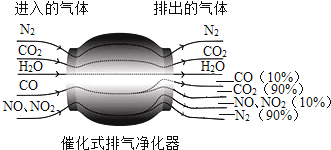 (8)、当汽车受撞击后,汽车安全气囊中的NH4NO3固体瞬间分散成N2O 和一种常温下的无色液体,反应方程式是 .
(8)、当汽车受撞击后,汽车安全气囊中的NH4NO3固体瞬间分散成N2O 和一种常温下的无色液体,反应方程式是 .三、计算题(共7分)
-
21. 发射通信卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,生成物不会对大气造成污染.(1)、反应的化学方程式为2N2H4+N2O4=3+4H2O.
(2)、请计算9.6gN3H4完全燃烧需要助燃物N2O4的质量.四、流程工艺题(共7分)
-
22.
绿矾又名七水硫酸亚铁(FeSO4•7H2O),其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等.绿矾(FeSO4•7H2O)的一种综合利用工艺如下:
 (1)、分离得碳酸亚铁固体和母液方法是 , 所需玻璃仪器为(至少两种).(2)、绿矾与NH4HCO3在溶液中反应,有CO2和H2O等四种物质生成,反应的化学方程式为 .(3)、
(1)、分离得碳酸亚铁固体和母液方法是 , 所需玻璃仪器为(至少两种).(2)、绿矾与NH4HCO3在溶液中反应,有CO2和H2O等四种物质生成,反应的化学方程式为 .(3)、隔绝空气进行“焙烧”,铁元素的转化途径是
 FeO
FeO , 实际作还原剂的是CO,写出“焙烧”过程中各反应的化学方程式: a.FeCO3
, 实际作还原剂的是CO,写出“焙烧”过程中各反应的化学方程式: a.FeCO3 FeO+CO2↑b. CO2+C
FeO+CO2↑b. CO2+C 2CO ;该反应为(吸热或放热)c. FeO+CO
2CO ;该反应为(吸热或放热)c. FeO+CO . (4)、母液“除杂”后,就得到(NH4)2SO4粗产品,操作步骤依次为蒸发浓缩、、过滤、洗涤、干燥.
. (4)、母液“除杂”后,就得到(NH4)2SO4粗产品,操作步骤依次为蒸发浓缩、、过滤、洗涤、干燥.五、实验题及探究题(共2小题,共18分)
-
23. 实验设计时化学实验的重要环节,请根据下列实验要求回答相关问题:
(1)、实验一
实验二

2

【活动与探究一】用对比实验方法探究二氧化碳的性质.
实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为;对比A瓶与(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(2)、实验二观察到C装置中发生的现象是 , 结论是(用化学方程式表示).
(3)、【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
实验三
实验四


实验三目的是探究对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响,该实验中需要控制的变量是温度和 .
(4)、【活动与探究三】定量测定空气中氧气的含量.
实验五


实验五中,反应的原理为(用化学方程式表示);装置一比装置二更合理,理由是;
根据下表提供的实验数据,完成下表:
硬质玻璃管中空气的体积
反应前注射器中空气体积
反应后注射器中气体体积
实验测得空气中氧气的体积分数
30mL
20mL
12mL
定量实验操作中易产生误差,如果反应前气球中存在气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果(填“偏小”、“偏大”或“无影响”).
24. 叠氮化钠(NaN3)倍广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究:【应用研究】
(1)、汽车经撞击后,30毫秒内引发NaN3迅速分解为Na、N2 , 反应方程式为: .(2)、【制备研究】
将金属钠与液态氨反应得NaNH2 , 再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O═NaN3+NaOH+X,X气体的化学式 .
【Na2CO3质量分数测定】
工业级NaN3中常含有少量的Na2CO3 , 为测定样品中Na2CO3的质量分数设计如图1装置.
(已知H2SO4溶液与NaN3 , 反应不生成气体.与碳酸钠反应生成二氧化碳气体).
提示:碱石灰是NaOH和CaO固体,能吸水和二氧化碳气体,氢氧化钠与二氧化碳反应生成碳酸和水.
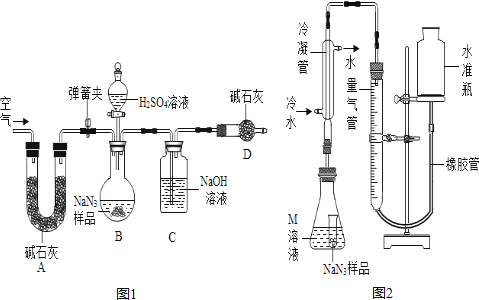 (3)、装置A的作用是 . 设计的实验步骤为:
(3)、装置A的作用是 . 设计的实验步骤为:①精确称量样品,检查装置气密性;
②打开弹簧夹,鼓入空气,称量装置C;
③关闭弹簧夹,打开分液漏斗活塞;
④再打开弹簧夹,鼓入空气;此次鼓入空气的作用是 .
⑤再次称量装置C.计算碳酸钠含量至少需要测定(填数字)个数据.如不用装置C后的球型干燥管装置,则得到的碳酸钠的含量(填“偏小”、“偏大”或“无影响”).
【NaN3纯度测定】
精确称量0.140gNaN3样品,设计如图2装置,测定其纯度.已知2NaN3→3N2(NaN3中的N全部转化为N2 , 其他产物略),反应中放出大量的热.
(4)、检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差(填“变大”、“变小”或“不变”),说明气密性良好.(5)、若一定条件下氮气的密度为1.2g/L,现测得量器管中气体体积相同条件下为70mL,则NaN3纯度为(保留一位小数).
-
-