贵州省黔南州贵定县旧治农中2019年中考化学三模试卷
试卷更新日期:2020-05-09 类型:中考模拟
一、选择题
-
1.
如图所示,在盛有稀硫酸的烧杯中,滴加几滴氯化钡溶液后,在烧杯里的溶液中离子数目的变化是( )
 A、Cl﹣增多了,SO42﹣减少了 B、Ba2+增多了,H+减少了 C、Cl﹣增多了,H+减少了 D、H+减少了,SO42﹣减少了2. 人类每年要向自然界索取大量的金属矿物资源,以提取数以亿吨计的金属.下列有关金属资源的说法,不正确的是( )A、自然界中除少量不活泼的金属如金铂等以单质形式存在外,其余都以化合态存在 B、合理开发金属矿物,寻找金属替代品,回收利用废金属都是保护金属资源的方法 C、采用合理的方法防止金属锈蚀,可以有效的保护金属资源 D、自然界中的金属资源是取之不尽,用之不竭的3. 野外旅行时,根据季节可以带上“即热饭盒”或“化学冰箱”.“化学冰箱”即把一种化学试剂放入容器中,加一定量的水,就可以形成低温小环境,这种试剂可以是下列物质中的( )A、浓硫酸 B、硝酸铵 C、固体氢氧化钠 D、食盐4. 为验证Fe、Cu、Ag 3种金属的活动性顺序,某小组同学设计了如图所示的4种实验方案(不做其他实验).其中不能达到目的是( )A、
A、Cl﹣增多了,SO42﹣减少了 B、Ba2+增多了,H+减少了 C、Cl﹣增多了,H+减少了 D、H+减少了,SO42﹣减少了2. 人类每年要向自然界索取大量的金属矿物资源,以提取数以亿吨计的金属.下列有关金属资源的说法,不正确的是( )A、自然界中除少量不活泼的金属如金铂等以单质形式存在外,其余都以化合态存在 B、合理开发金属矿物,寻找金属替代品,回收利用废金属都是保护金属资源的方法 C、采用合理的方法防止金属锈蚀,可以有效的保护金属资源 D、自然界中的金属资源是取之不尽,用之不竭的3. 野外旅行时,根据季节可以带上“即热饭盒”或“化学冰箱”.“化学冰箱”即把一种化学试剂放入容器中,加一定量的水,就可以形成低温小环境,这种试剂可以是下列物质中的( )A、浓硫酸 B、硝酸铵 C、固体氢氧化钠 D、食盐4. 为验证Fe、Cu、Ag 3种金属的活动性顺序,某小组同学设计了如图所示的4种实验方案(不做其他实验).其中不能达到目的是( )A、 B、
B、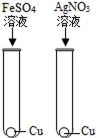 C、
C、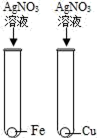 D、
D、 5. 菱铁矿的主要成分是FeCO3 . 下列有关说法正确的是( )A、菱铁矿是铁的合金 B、菱铁矿中铁元素的质量分数为48.3% C、FeCO3中铁的化合价为+3 D、FeCO3是含有氧元素的化合物6. 化学行业中把材料分为:金属材料、无机非金属材料、有机高分子材料等.金属材料在现实生活中有极为重要的作用.下列金属材料的运用与金属所具有的性质不一致的是( )A、制造白炽灯灯丝﹣﹣熔点高 B、制造飞机﹣﹣坚硬而质轻 C、制造保险丝﹣﹣硬度大 D、制造装化工原料的容器﹣﹣耐腐蚀7. 下列关于生铁和钢的叙述正确的是( )A、生铁和钢都是纯净物 B、生铁是炼钢的主要原料 C、生铁和钢都是铁的单质 D、生铁是铁和碳的化合物8. 我县历史悠久,物产丰富,下列特产中富含维生素的是( )A、富官庄小米 B、王庄大樱桃 C、沙沟水库鲤鱼 D、崔家峪豆腐9. 金属防锈既可以节约资源,又能美化环境.下列钢铁制品经过如下处理后,防锈效果最差的是()A、经常在表面涂油的大型钢制机械 B、涂上防锈漆后的“辽宁”号航母舰体外壳 C、擦洗干净后长期存放在室外的大型铁制农机具 D、经过“烤蓝”,在表面形成致密氧化膜的钢制枪管10. 下列图像与对应的表述不吻合的是 ( )A、
5. 菱铁矿的主要成分是FeCO3 . 下列有关说法正确的是( )A、菱铁矿是铁的合金 B、菱铁矿中铁元素的质量分数为48.3% C、FeCO3中铁的化合价为+3 D、FeCO3是含有氧元素的化合物6. 化学行业中把材料分为:金属材料、无机非金属材料、有机高分子材料等.金属材料在现实生活中有极为重要的作用.下列金属材料的运用与金属所具有的性质不一致的是( )A、制造白炽灯灯丝﹣﹣熔点高 B、制造飞机﹣﹣坚硬而质轻 C、制造保险丝﹣﹣硬度大 D、制造装化工原料的容器﹣﹣耐腐蚀7. 下列关于生铁和钢的叙述正确的是( )A、生铁和钢都是纯净物 B、生铁是炼钢的主要原料 C、生铁和钢都是铁的单质 D、生铁是铁和碳的化合物8. 我县历史悠久,物产丰富,下列特产中富含维生素的是( )A、富官庄小米 B、王庄大樱桃 C、沙沟水库鲤鱼 D、崔家峪豆腐9. 金属防锈既可以节约资源,又能美化环境.下列钢铁制品经过如下处理后,防锈效果最差的是()A、经常在表面涂油的大型钢制机械 B、涂上防锈漆后的“辽宁”号航母舰体外壳 C、擦洗干净后长期存放在室外的大型铁制农机具 D、经过“烤蓝”,在表面形成致密氧化膜的钢制枪管10. 下列图像与对应的表述不吻合的是 ( )A、 向氢氧化钠溶液中不断加水
B、
向氢氧化钠溶液中不断加水
B、 氯酸钾和二氧化锰混合加热制取氧气
C、
氯酸钾和二氧化锰混合加热制取氧气
C、 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
D、
向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
D、 某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
11. 下列有关物质用途的说法中,不正确的是( )A、用氢氧化钠改良酸性土壤 B、二氧化锰作过氧化氢制取氧气的催化剂 C、氢氧化铝用于治疗胃酸过多 D、用稀盐酸除去金属表面的锈12. 下列有关说法中正确的是( )A、水是取之不尽、用之不竭的,因此可以任意使用 B、用扇子扇煤炉火,由于鼓入了大量的空气而温度没有降至煤的着火点以下,因而越扇越旺 C、使用化肥能够提高粮食产量,因此农业上要大量施用化肥 D、石油是一种重要的化工产品13. 金属材料在现实生活中有极为重要的作用.下列金属材料的运用与金属所具有的性质不一致的是( )A、制造白炽灯灯丝﹣﹣熔点高 B、制造飞机﹣﹣坚硬而质轻 C、制造装化工原料的容器﹣﹣耐腐蚀 D、制造保险丝﹣﹣硬度大14. 化学对人类生活和社会发展做出了巨大贡献。下列有关主题知识与应用不正确的是( )
某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
11. 下列有关物质用途的说法中,不正确的是( )A、用氢氧化钠改良酸性土壤 B、二氧化锰作过氧化氢制取氧气的催化剂 C、氢氧化铝用于治疗胃酸过多 D、用稀盐酸除去金属表面的锈12. 下列有关说法中正确的是( )A、水是取之不尽、用之不竭的,因此可以任意使用 B、用扇子扇煤炉火,由于鼓入了大量的空气而温度没有降至煤的着火点以下,因而越扇越旺 C、使用化肥能够提高粮食产量,因此农业上要大量施用化肥 D、石油是一种重要的化工产品13. 金属材料在现实生活中有极为重要的作用.下列金属材料的运用与金属所具有的性质不一致的是( )A、制造白炽灯灯丝﹣﹣熔点高 B、制造飞机﹣﹣坚硬而质轻 C、制造装化工原料的容器﹣﹣耐腐蚀 D、制造保险丝﹣﹣硬度大14. 化学对人类生活和社会发展做出了巨大贡献。下列有关主题知识与应用不正确的是( )选项
主题
知识与应用
A
化学与生活
预防坏血病﹣﹣服用维生C
B
化学与能源
改善能源结构﹣﹣开发太阳能、氢能
C
化学与环境
减少白色污染﹣﹣禁止使用塑料制品
D
化学与安全
进入久未开启的菜窖﹣﹣先做灯火试验
A、A B、B C、C D、D15. 将X、Y、Z三种金属分别投入足量的稀硫酸中,只有X、Z能发生反应,并放出氢气。将Z投入X的硝酸盐溶液中,有金属X产生。则X、Y、Z三种金属的活动性由强到弱的顺序为()A、Z>Y>X B、Z>X>Y C、X>Z>Y D、Y>Z>X16. 下列化学反应中,不属于置换反应的是A、 B、 C、 D、17. 下列反应属于中和反应的是( )A、2HCl+CuO═CuCl2+H2O B、2NaOH+CO2═Na2CO3+H2O C、2HCl+Cu(OH)2═CuCl2+2H2O D、CaO+H2O═Ca(OH)218. 对如图实验的分析说明不正确的是( ) A、该实验说明一氧化碳具有还原性 B、该实验说明生成物二氧化碳的密度比空气大 C、该实验说明一氧化碳和氧化铜的反应需要加热 D、该实验可以防止有毒的一氧化碳气体对空气的污染,同时又可以充分利用能源19. 下列垃圾可放入“可回收物”垃圾箱的是( )
A、该实验说明一氧化碳具有还原性 B、该实验说明生成物二氧化碳的密度比空气大 C、该实验说明一氧化碳和氧化铜的反应需要加热 D、该实验可以防止有毒的一氧化碳气体对空气的污染,同时又可以充分利用能源19. 下列垃圾可放入“可回收物”垃圾箱的是( )①废铜线②打碎的陶瓷③纸皮箱④吃剩的饭菜.
A、①③ B、②④ C、②③ D、①④20. 把X、Y、Z三种金属片分别加入稀硫酸中,X、Y表面有气泡产生,Z无变化;把X加入Y的化合物溶液中,X表面析出Y.则三种金属活动顺序为( )A、Y>X>Z B、X>Y>Z C、Z>Y>X D、X>Z>Y二、非选择题
-
21. A,B,C,D,E是初中化学中常见的五种无色气体,其中有两种是单质,另三种是化合物,它们之间有如图所示的转化关系(图中未注明反应条件):
 (1)、写出A、B、C、D、E的化学式:A、 , B、 , C、 , D、 , E、 .(2)、在上述五种气体中,不含有组成A气体的元素的是(填化学式).(3)、D与CuO发生反应的化学方程式为 . 冶炼金属常用(填字母)与氧化铁来发生反应(填反应类型).(4)、通常烧烤时意外着火不能用水浇灭木炭,会生成水煤气,试写出发生反应的化学方程式 .22. 硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).
(1)、写出A、B、C、D、E的化学式:A、 , B、 , C、 , D、 , E、 .(2)、在上述五种气体中,不含有组成A气体的元素的是(填化学式).(3)、D与CuO发生反应的化学方程式为 . 冶炼金属常用(填字母)与氧化铁来发生反应(填反应类型).(4)、通常烧烤时意外着火不能用水浇灭木炭,会生成水煤气,试写出发生反应的化学方程式 .22. 硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).查阅资料:①Fe+2HCl═FeCl2+H2↑;②单质硅不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑);③红棕色粉末E为一种含有铁元素的氧化物.

根据以上信息,回答下列问题:
(1)、固体A的成分为 , 滤液B中的金属阳离子为;(2)、写出步骤③中加入 NaOH溶液的作用是;(3)、在过滤操作中用到的玻璃仪器有烧杯、漏斗和 , 若操作规范、装置完好,发现滤液浑浊,应;(4)、写出步骤⑦中发生反应的化学方程式 .23. a、b、c三种固体物质(均不含结晶水)的溶解度曲线如图所示,请回答: (1)、t1℃时,三种物质的溶解度最大的是。(2)、t2℃时,将50g固体a加入到50g水中,充分搅拌后所得溶液的质量为g。(3)、将t2℃溶液质量相等的a、b、c三种物质的饱和溶液降温至t1℃,此时溶液的质量由大到小的顺序是。(4)、下列有关说法正确的有。(填序号)
(1)、t1℃时,三种物质的溶解度最大的是。(2)、t2℃时,将50g固体a加入到50g水中,充分搅拌后所得溶液的质量为g。(3)、将t2℃溶液质量相等的a、b、c三种物质的饱和溶液降温至t1℃,此时溶液的质量由大到小的顺序是。(4)、下列有关说法正确的有。(填序号)①其它条件不变,升高温度可使c的饱和溶液变成不饱和溶液
②t1℃时,a、c两种物质的饱和溶液中溶质的质量分数相等
③若a物质中混有少量b,可采用降温结晶的方法提纯a物质
④t2℃时,a、b、c三种物质配成的等质量饱和溶液中含溶剂质量最多的是a溶液
24. Na2SO4是制造纸张、药品、染料稀释剂等的重要原料。某Na2SO4样品中含有少量CaCl2和MgCl2 , 实验室提纯Na2SO4的流程如图所示。 (1)、操作a的名称是。(2)、加入NaOH溶液可除去的是 , 其反应的化学方程式为:。若添加的NaOH溶液和Na2CO3溶液过量,可加入适量(填“稀盐酸”或“稀硫酸”)除去。25. 如图所示为A,B,C三种物质的溶解度曲线:
(1)、操作a的名称是。(2)、加入NaOH溶液可除去的是 , 其反应的化学方程式为:。若添加的NaOH溶液和Na2CO3溶液过量,可加入适量(填“稀盐酸”或“稀硫酸”)除去。25. 如图所示为A,B,C三种物质的溶解度曲线: (1)、T2℃时,A,B,C三种物质的溶解度大小顺序是。(2)、将C物质的不饱和溶液变为饱和溶液的方法为(写一种)。(3)、T1℃时,完全溶解15gA物质最少需g水。(4)、A中含有少量B时,可通过的方法提纯A。(5)、T2℃时,B物质溶液中溶质的质量分数不可能为。
(1)、T2℃时,A,B,C三种物质的溶解度大小顺序是。(2)、将C物质的不饱和溶液变为饱和溶液的方法为(写一种)。(3)、T1℃时,完全溶解15gA物质最少需g水。(4)、A中含有少量B时,可通过的方法提纯A。(5)、T2℃时,B物质溶液中溶质的质量分数不可能为。A 20% b 25% c 33.3% d 50%
26. 在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中钠在其中继续燃烧,反应后冷却,瓶底附着有黑色颗粒,同时瓶壁上粘附着白色物质.老师告诉甲同学瓶底附着黑色颗粒是碳单质,但没有告诉瓶壁上粘附着白色物质是什么,让同学们继续探究.(1)、(进行猜想)甲同学认为:白色物质可能是Na2O或Na2CO3乙同学认为:白色物质可能是NaOH
甲同学立刻认为乙同学的猜想是不正确的,其理由是 .
(2)、(查阅资料)氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O═2NaOH(实验探究)甲同学对白色物质进行实验探究.
实验方案
实 验 操 作
实验现象
结 论
方案1
取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液
溶液变成红色
白色物质
为Na2O
方案2
取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入适量溶液
白色物质
是Na2CO3
(3)、(反思评价)丙同学认为方案1得到的结论不符合题意,理由是 .(4)、(得出结论)钠在二氧化碳中燃烧的化学方程式为 .通过以上探究,你对燃烧和灭火有什么新的认识,请写出一点. .
27. 某学习小组的同学做实验,向盛有少量氢氧化钠溶液的试管中通入二氧化碳,未看到明显的实验现象。
(提出问题)氢氧化钠能否与二氧化碳反应?
(猜想与假设)亮亮同学认为氢氧化钠能与二氧化碳反应;莉莉同学认为氢氧化钠不能与二氧化碳反应。
(1)、(设计与实验)亮亮同学设计了两个装置并进行实验。请你和他一起验证他的猜想。实验步骤
实验现象
实验结论
如图一,将收集满二氧化碳的试管倒置于氢氧化钠溶液中
如图二,
(2)、(反思与评价)莉莉同学提出质疑,认为上述现象可能是二氧化碳溶于水的结果。(设计与实验)请你设计一个实验,证明氢氧化钠确实与二氧化碳反应。
实验步骤
实验现象
实验结论
氢氧化钠与二氧化碳反应
(3)、(交流与提高)实验证明氢氧化钠还能与二氧化硫反应,化学方程式为:2NaOH+SO2=X+H2O,X的化学式是。
28. 某研究小组为验证铁、铜、锌、银的金属活动性顺序,设计如图甲所示三个实验(三种金属均已用砂纸打磨过,其形状和大小相同,稀盐酸的浓度和用量也相同)。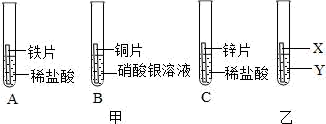 (1)、实验前用砂纸打磨金属的目的是。(2)、一段时间后,观察到实验B的铜片表面有银白色固体附着,且溶液由无色变为色,这说明铜比银的金属活动性(填“强”或“弱”),该反应的化学方程式为。(3)、甲同学认为通过实验A和C可比较锌和铁的金属活动性,他依据的实验现象是。(4)、乙同学认为仅仅通过上述实验不足以得出四种金属的活动性顺序,因此在上述实验的基础上,乙同学又补做了一个实验,装置如图乙所示,且实现了探究目的。乙同学的实验:X是金属 , Y是溶液。29. 安琪同学为探究铁制品锈蚀的条件,进行如下实验:
(1)、实验前用砂纸打磨金属的目的是。(2)、一段时间后,观察到实验B的铜片表面有银白色固体附着,且溶液由无色变为色,这说明铜比银的金属活动性(填“强”或“弱”),该反应的化学方程式为。(3)、甲同学认为通过实验A和C可比较锌和铁的金属活动性,他依据的实验现象是。(4)、乙同学认为仅仅通过上述实验不足以得出四种金属的活动性顺序,因此在上述实验的基础上,乙同学又补做了一个实验,装置如图乙所示,且实现了探究目的。乙同学的实验:X是金属 , Y是溶液。29. 安琪同学为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器收集20mL O2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝表面的现象如表所示。
观察对象
现象
①干燥的普通铁丝
没有明显变化
②潮湿的普通铁丝
③潮湿的纯铁丝
没有明显变化
(1)、步骤1中,检查U形管内是否已充满O2的方法是。(2)、铁制品锈蚀的条件之一是需要O2 , 在此实验中能支持此条件的证据是。(3)、通过对比实验现象,此实验还可得出铁制品锈蚀的条件是和。(4)、雨后郊外的路比较泥泞,如果你的交通工具是自行车,你回来进行清洗后,采取的防锈措施是(填字母)A 立即晾晒干 B 涂油漆 C 链条传动部件涂上油
30. 若要生产含杂质4%的生铁100 t,需要含氧化铁60%的赤铁矿石的质量是多少?(要求:写出计算过程,计算结果保留小数点后1位)