贵州省黔西南州望谟县2019年中考化学二模试卷
试卷更新日期:2020-05-07 类型:中考模拟
一、选择题
-
1. 美丽的望谟周围无时无刻都在发生着各种各样的变化,下列变化中不属于物理变化是( )A、雪花飘落 B、点灯发光 C、铁护栏生锈 D、水的蒸发2. 下列实验操作不正确的是( )A、蒸发结晶
 B、检查气密性
B、检查气密性  C、滴管用毕即插回
C、滴管用毕即插回  D、测定溶液的pH
D、测定溶液的pH  3. 2018年2月,在马来西亚吉隆坡举办的第九届世界城市论坛上,常德分享了“海绵城市”建设﹣﹣水治理的成功经验,下列与水有关的说法不正确的是( )A、淡水资源是取之不尽、用之不竭的 B、为减少水体污染,农药、化肥要合理使用 C、工业上应该对废水做处理使之符合标准后再排放 D、为节约用水,农业、园林浇灌改大水漫灌为喷灌、滴灌4. 豆浆中的异黄酮(C15H10O2)具有防癌功能,下列关于异黄酮说法正确的是( )A、异黄酮完全燃烧只生成二氧化碳 B、异黄酮中碳元素的质量分数最大 C、异黄酮分子中含有氧分子 D、异黄酮中共含有27个原子5. 某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示.下列说法正确的是( )
3. 2018年2月,在马来西亚吉隆坡举办的第九届世界城市论坛上,常德分享了“海绵城市”建设﹣﹣水治理的成功经验,下列与水有关的说法不正确的是( )A、淡水资源是取之不尽、用之不竭的 B、为减少水体污染,农药、化肥要合理使用 C、工业上应该对废水做处理使之符合标准后再排放 D、为节约用水,农业、园林浇灌改大水漫灌为喷灌、滴灌4. 豆浆中的异黄酮(C15H10O2)具有防癌功能,下列关于异黄酮说法正确的是( )A、异黄酮完全燃烧只生成二氧化碳 B、异黄酮中碳元素的质量分数最大 C、异黄酮分子中含有氧分子 D、异黄酮中共含有27个原子5. 某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示.下列说法正确的是( )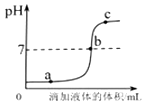 A、图中a点所示溶液中,含有的溶质是NaCl和NaOH B、由a点到b点的pH变化过程证明酸和碱发生了中和反应 C、向图中c点所示溶液中滴加无色酚酞,溶液不变色 D、该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中6. 某溶液能使紫色石蕊溶液变红,下列各组离子在该溶液中能大量共存的是( )A、Ag+、Na+、 Cl﹣、NO3﹣ B、Na+、K+、OH﹣、SO42﹣ C、K+、Na+、CO32﹣、 Cl﹣ D、Ba2+、Mg2+、NO3﹣、Cl﹣
A、图中a点所示溶液中,含有的溶质是NaCl和NaOH B、由a点到b点的pH变化过程证明酸和碱发生了中和反应 C、向图中c点所示溶液中滴加无色酚酞,溶液不变色 D、该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中6. 某溶液能使紫色石蕊溶液变红,下列各组离子在该溶液中能大量共存的是( )A、Ag+、Na+、 Cl﹣、NO3﹣ B、Na+、K+、OH﹣、SO42﹣ C、K+、Na+、CO32﹣、 Cl﹣ D、Ba2+、Mg2+、NO3﹣、Cl﹣二、非选择题
-
7. 用化学用语填空:(1)、3个铵根离子。(2)、2个钾原子。(3)、氢氧化铝中铝元素的化合价。(4)、3个二氧化碳分子。(5)、人体中含量最高的金属元素是。(6)、保持二氧化硫化学性质的是。8. 生活与化学密切相关,生活中处处有化学,请你根据所学化学知识回答下列问题:(1)、我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于(填“金属材料”或“合成材料”)。(2)、铁在有水和的条件下会生锈,用稀盐酸除去铁锈的化学反应方程式为。(3)、能源合作是“一带一路”的重要内容中缅油气管道将石油和天然气输入中国,石油是由多种化合物组成的(选填“混合物”或“纯净物”);天然气是较清洁的能源,其燃烧的化学方程式为:。(4)、可以用的方法区分天然纤维和合成纤维。9. 下图中图甲为硒元素在元素周期表中的信息示意图,图乙、A,B,C,D是五种粒子的结构示意图。
 (1)、硒元素属于元素(填“金属”或“非金属”)。(2)、C粒子属于(填“原子”、“阴离子”或“阳离子”);图乙中X=。(3)、A,B,C,D中属于同种元素的是(填序号)。(4)、A粒子的化学性质与B,C,D中哪一种粒子的化学性质相似(填序号)10. 如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)、硒元素属于元素(填“金属”或“非金属”)。(2)、C粒子属于(填“原子”、“阴离子”或“阳离子”);图乙中X=。(3)、A,B,C,D中属于同种元素的是(填序号)。(4)、A粒子的化学性质与B,C,D中哪一种粒子的化学性质相似(填序号)10. 如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题: (1)、A点的含义是。(2)、若乙中混有少量甲,最好采用的方法提纯乙(填“降温结晶”或“蒸发结晶”)。(3)、将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是。11. A~J是初中化学中常见的物质,其中A为气体,B为红棕色粉末,E为浅绿色溶液,G是一种建筑材料,它们之间的关系如下图(部分反应物或生成物已略去)。
(1)、A点的含义是。(2)、若乙中混有少量甲,最好采用的方法提纯乙(填“降温结晶”或“蒸发结晶”)。(3)、将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是。11. A~J是初中化学中常见的物质,其中A为气体,B为红棕色粉末,E为浅绿色溶液,G是一种建筑材料,它们之间的关系如下图(部分反应物或生成物已略去)。 (1)、写出化学式:D , I;(2)、A+B→C+D的化学反应方程式是;(3)、F+I→G+J反应的基本类型为反应。12. 下列装置常用于实验室制取气体。根据给出的装置回答下列问题。
(1)、写出化学式:D , I;(2)、A+B→C+D的化学反应方程式是;(3)、F+I→G+J反应的基本类型为反应。12. 下列装置常用于实验室制取气体。根据给出的装置回答下列问题。 (1)、指出编号仪器名称:① , ②。(2)、实验室利用A装置制取氧气,反应原理用化学方程式表示为。(3)、制取并收集二氧化碳应选择的装置是(从A-E中选择),使用该套装置制取气体的突出优点是 , 该反应原理用化学方程式表示为。改用F装置收集二氧化碳,则气体应从端进入。制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上杂质气体除去则装置正确的连接顺序是:混合气体→(用端口字母表示)。13. 皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
(1)、指出编号仪器名称:① , ②。(2)、实验室利用A装置制取氧气,反应原理用化学方程式表示为。(3)、制取并收集二氧化碳应选择的装置是(从A-E中选择),使用该套装置制取气体的突出优点是 , 该反应原理用化学方程式表示为。改用F装置收集二氧化碳,则气体应从端进入。制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上杂质气体除去则装置正确的连接顺序是:混合气体→(用端口字母表示)。13. 皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。[提出问题] (1)白色沉淀 A是什么?(2)无色滤液B中的溶质有哪些?
[查阅资料] (1)腌制皮 蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物。(2)氯化钠、硝酸钡水溶液显中性。
(1)、[理论推理]①白色沉淀 A是CaCO3 , 请写出生成该沉淀的化学方程式。
②滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
(2)、[实验验证]为证明滤液 B中存在的三种溶质,同学们进行了如下实验。步骤
实验操作
实验现象
实验结论
Ⅰ
取少量滤液B于试管中,加入过量的Ba(NO3)2溶液,过滤
滤液B中含有Na2CO3、NaOH、NaCl
Ⅱ
取少量步骤I中所得滤液于试管中,加入酚酞溶液
Ⅲ
另取少量步骤I中所得滤液于试管中,先加入足量的稀硝酸,再加入溶液
产生白色沉淀
(3)、[拓展提升]①向步骤I中加入过量Ba(NO3)2溶液的目的是。
②小妮同学认为若将步骤I中的Ba(NO3)2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理(填“合理”或“不合理”)。
③小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的Ba(NO3)2溶液,也能得出滤液B的溶质中含有Na2CO3和NaOH的结论,你是(填“同意”或“不同意”)理由。
14. 某校化学兴趣小组在参加社会实践活动时,环保组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保组的同学进行了以下实验:取废水300g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,请分析计算: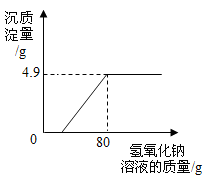 (1)、实验中生成氢氧化铜的质量为g。(2)、300g该废水中硫酸铜的质量。(3)、该废水中硫酸的溶质质量分数。(计算结果精确到0.1%)
(1)、实验中生成氢氧化铜的质量为g。(2)、300g该废水中硫酸铜的质量。(3)、该废水中硫酸的溶质质量分数。(计算结果精确到0.1%)