贵州省贵阳市花溪区2019年中考化学模拟试卷
试卷更新日期:2020-05-07 类型:中考模拟
一、选择题
-
1. 在2018年中国十大避暑名城中被誉为避暑之都的贵州省贵阳市排名第二,为了保护我们“爽爽的贵阳”的美丽环境,下列做法不正确的是( )A、街道照明,大量使用太阳能LED灯 B、提倡垃圾焚烧处理 C、推广使用无磷洗衣粉 D、回收利用废旧金属、废旧书报及废弃塑料2. 下列实验操作中,正确的是( )A、
 点燃酒精灯
B、
点燃酒精灯
B、 过滤
C、
过滤
C、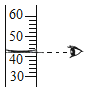 量取液体体积读数
D、
量取液体体积读数
D、 称量NaCl固体
3. 毒品是人类社会的公害,尤其是青少年更应“珍惜生命,远离毒品”。海洛因是我国政府明令严禁的毒品,一级海洛因的主要成分是二乙酰吗啡(化学式为C21H23NO5)。下列有关二乙酰吗啡说法不正确的是( )A、二乙酰吗啡碳元素的质量分数最高 B、二乙酰吗啡由四种元素组成 C、一个二乙酰吗啡分子含50个原子 D、二乙酰吗啡中C、H、N的质量比为21:23:14. 某同学对所学部分化学知识归纳如下,完全正确的一组是( )
称量NaCl固体
3. 毒品是人类社会的公害,尤其是青少年更应“珍惜生命,远离毒品”。海洛因是我国政府明令严禁的毒品,一级海洛因的主要成分是二乙酰吗啡(化学式为C21H23NO5)。下列有关二乙酰吗啡说法不正确的是( )A、二乙酰吗啡碳元素的质量分数最高 B、二乙酰吗啡由四种元素组成 C、一个二乙酰吗啡分子含50个原子 D、二乙酰吗啡中C、H、N的质量比为21:23:14. 某同学对所学部分化学知识归纳如下,完全正确的一组是( )A化学与生产
B化学与材料
①用煮沸的方式,降低水的硬度
②用尿素当做钾肥使用
①用钛合金广泛用于火箭、导弹、航天飞机等,是利用其熔点高、密度大,耐腐蚀能好等性质
②装食品用的聚乙烯塑料袋具有热塑性
C化学与能源
D化学与健康
①利用燃烧等化学反应产生的能量可做饭、取暖、发电、烧制陶瓷、冶金等
②氢气被认为是理想清洁、高能燃料,已被广泛应用。
①青少年食欲不振,生长迟缓,发育不良应多食海产品、瘦肉等含锌的食物
②医疗上可将乙醇配制成体积分数为75%的酒精用于消毒。
A、A B、B C、C D、D5. 下列四个实验都设计了两种方案,其中两种方案均合理的是( )选项
实验目的
方案1
方案2
A
鉴别氯化钠溶液和稀盐酸
加锌粒
加石蕊试液
B
区别水和醋酸
看颜色
闻气味
C
除去氯化钙中少量的碳酸钙
溶解、过滤、洗涤、干燥
加稀硫酸
D
检验一氧化碳中是否混有少量二氧化碳
点燃
通入澄清石灰水
A、A B、B C、C D、D6. 甲、乙、丙三种物质间的转化关系如图所示,则甲、乙、丙的顺序不可能是( ) A、H2O 、H2O2 、O2 B、Ca(OH)2、CaCO3、CaO C、Al2O3、Al、Al2(SO4)3 D、CO、C、CO2
A、H2O 、H2O2 、O2 B、Ca(OH)2、CaCO3、CaO C、Al2O3、Al、Al2(SO4)3 D、CO、C、CO2二、非选择题
-
7. 改革开放40年来,贵阳发生了翻天覆地的变化,得到巨大发展,请从化学的视角回答下列问题:(1)、2018年4月26日“贵阳一号”卫星在中国酒泉卫星发射中心成功发射。
①“贵阳一号”卫星可以为“一带一路”经济发展提供信息服务。新“丝绸之路”可以把我市的富硒茶、阳朗辣子鸡等特色食品推广到国外。阳朗辣子鸡中鸡肉主要富含的营养素是;富硒茶中“硒”属于元素(填“金属”或“非金属”)。
②火箭的燃料采用了含有聚丁二烯(化学式为(C4H6)n)的固体推进剂,聚丁二烯属于(填“有机物”或“无机物”)。
③“贵阳一号”遥感卫星大数据还能服务环境,为贵阳的饮用水进行实时监控。在水的净化过程中,活性炭可以除去水中的异味和色素,这利用了活性炭性。
(2)、贵阳已进入高铁时代①高铁列车车体中钢铁部分一般都会刷上油漆,其作用为。
②修建铁路需要大量钢铁。雨后的铁轨表面易产生锈迹,实验室常用盐酸除铁锈,其化学方程式为。
③高铁列车车厢是密闭的空间,提供清洁空气、保持车厢卫生非常重要。空气中能供给呼吸的物质是 , 高铁酸钠(Na2FeO4)是高铁上常用的一种“绿色环保高效”消毒剂,Na2FeO4中铁元素的化合价为。
8. 从微观的角度认识物质及其变化,请根据图示回答下列问题。(1)、从宏观上看,图1所示变化属于变化(填“物理”或“化学”),从微观角度解释图1、图2所示的两个变化的本质区别是。 (2)、写出符合图2所示变化的化学方程式 , 该反应的基本反应类型是。(3)、图3中,B,C,D三种物质属于氧化物的是(填化学式);若一定质量的A和6.4g的B恰好完全反应,可生成4.4gC和3.6gD,则组成A的元素是。
(2)、写出符合图2所示变化的化学方程式 , 该反应的基本反应类型是。(3)、图3中,B,C,D三种物质属于氧化物的是(填化学式);若一定质量的A和6.4g的B恰好完全反应,可生成4.4gC和3.6gD,则组成A的元素是。 9. 请根据如图中有关信息,回答下列问题:
9. 请根据如图中有关信息,回答下列问题: (1)、C装置中,仪器a、b的名称:a , b。(2)、若用装置A制取氧气,其反应的化学方程式;若要收集到较纯净的氧气,其收集装置应选 , 待收集完毕后应进行的操作。(3)、实验制取CO2 , 为了控制反应的发生与停止,选择最佳的发生装置是(填装置编号);制取二氧化碳的化学方程式。(4)、装置G可以用于收集气体,也可以净化气体。若用装置G用排水法收集氧气,气体应该从(填a或b)端通入。若要除去CO2中混有的少量HCl气体,装置G中应装入的药品是。10. 水是生活中最常见的物质之一,也是实验室常用的试剂。请用所学的化学知识回答问题并完成以下实验。
(1)、C装置中,仪器a、b的名称:a , b。(2)、若用装置A制取氧气,其反应的化学方程式;若要收集到较纯净的氧气,其收集装置应选 , 待收集完毕后应进行的操作。(3)、实验制取CO2 , 为了控制反应的发生与停止,选择最佳的发生装置是(填装置编号);制取二氧化碳的化学方程式。(4)、装置G可以用于收集气体,也可以净化气体。若用装置G用排水法收集氧气,气体应该从(填a或b)端通入。若要除去CO2中混有的少量HCl气体,装置G中应装入的药品是。10. 水是生活中最常见的物质之一,也是实验室常用的试剂。请用所学的化学知识回答问题并完成以下实验。 (1)、如图中甲、乙实验可观察到的现象是 , 此实验说明。(2)、从丙图溶解度曲线能获取有关物质的信息是(写出两条),T3℃时,甲、乙、丙三种物质的饱和溶液中溶质的质量分数由大到小的顺序是。(3)、根据丙图信息,将甲溶液从状态B改变为状态A有多种途径。试设计并简述一操作简单、结果最准确的实验途径:。11. 金属与生活息息相关,认识金属的性质对我们至关重要,认真阅读,回答问题。(1)、材料一:镓(Ga)是灰蓝色或银白色的金属,熔点很低,沸点很高。其化学性质与铝相似,能与氧气在加热时反应。金属镓广泛应用于半导体材料,光电子工业和微波通讯工业等领域。镓的原子结构示意图如图所示。
(1)、如图中甲、乙实验可观察到的现象是 , 此实验说明。(2)、从丙图溶解度曲线能获取有关物质的信息是(写出两条),T3℃时,甲、乙、丙三种物质的饱和溶液中溶质的质量分数由大到小的顺序是。(3)、根据丙图信息,将甲溶液从状态B改变为状态A有多种途径。试设计并简述一操作简单、结果最准确的实验途径:。11. 金属与生活息息相关,认识金属的性质对我们至关重要,认真阅读,回答问题。(1)、材料一:镓(Ga)是灰蓝色或银白色的金属,熔点很低,沸点很高。其化学性质与铝相似,能与氧气在加热时反应。金属镓广泛应用于半导体材料,光电子工业和微波通讯工业等领域。镓的原子结构示意图如图所示。
镓的物理性质有。
(2)、写出镓与氧气反应的化学方程式。(3)、材料二:金属活动顺序在工农业生产和科学研究中有重要应用。现有铜、银、锌三种金属,某小组同学为了探究这三种金属的活动性,设计了以下实验:
试管A中反应的化学方程式是 , 由实验A、B、C可推断出Ag、Zn、Cu三种金属的活动性由强到弱的顺序为。
(4)、向C完全反应后的试管里加入一定质量的锌粒(如D试管)。D试管中一定会发生的反应是的化学方程式是。12. 某小组同学在实验室进行实验,请你参与。(1)、同学们先取少量在空气中久置的氢氧化钠固体样品加水配制成溶液,另取2mL该溶液于小烧杯中,然后滴加几滴酚酞溶液,振荡,此时观察到的实验现象为:。接着向烧杯中逐滴加入稀盐酸并用玻璃棒搅拌,溶液的颜色改变,同时观察到有气泡产生。结论:氢氧化钠变质。请化学方程式解释氢氧化钠变质的原因:。(2)、针对氢氧化钠变质的程度做了进一步探究。(作出猜想)猜想一:样品部分变质,成分为NaOH、Na2CO3;
猜想二:样品完全变质,成分为。
(3)、(查阅资料)①BaCl2溶液显中性,BaCO3难溶于水。②向碳酸钠溶液中逐滴加入稀盐酸的反应是分步反应,会发生生成碳酸氢钠和氯化钠的反应。(实验探究)为验证猜想,同学们设计了两个方案,并进行实验。
①定性方案设计,请你将该实验设计补充完整。
实验内容
实验现象
得出结论
取少量样品溶液,加入足量BaCl2溶液,静置,向上层清液中滴加几滴无色酚酞溶液
猜想一正确
(4)、②定量方案设计 先准确称取 11.95g 变质的NaOH样品放入锥形瓶中,用电子秤称得锥形瓶及样品的总质量为46.95g,再把 150.00 g7.3 %稀盐酸平均分成 6等份,每份25.00g依次在充分摇动锥形瓶时,加入样品中,每次充分反应后用电子秤称得锥形瓶及所盛物质的质量,实验数据记录如下:加入盐酸的次数
第一次
第二次
第三次
第四次
第五次
第六次
锥形瓶及所盛物质总质量/g
71.95
96.95
120.85
144.75
168.65
193.65
(实验结论)请根据上述实验数据,计算样品中氢氧化钠的质量分数为(精确到0.1%),猜想一正确。
(5)、(反思交流)①在如图的直角坐标系中画出产生气体的质量与所加稀盐酸质量的关系曲线。

②请判断第二次加入盐酸过程中发生反应的化学方程式 , 原因。
13. 碳在高温时可以还原氧化铜,计算要使80g氧化铜完全还原,需要碳的质量至少是多少?