四川省成都市郫都区2019年中考化学模拟试卷
试卷更新日期:2020-05-07 类型:中考模拟
一、选择题
-
1. 下列属于化学变化的是( )A、木柴燃烧 B、酒精挥发 C、河水结冰 D、胆矾研碎2. 2018年世界环境日主题为“塑战速决”。下列做法不符合这主题的是( )A、用布袋代替塑料袋 B、就地焚烧塑料垃圾 C、回收利用废弃塑料 D、使用新型可降解塑料3. 下列做法不能达到目的的是( )A、利用活性炭净水,可以软化硬水 B、利用洗涤剂清洗餐具,可以去除油污 C、使用无磷洗衣粉,可以减少水体污染 D、食用铁强化酱油,可以预防缺铁性贫血4. 下列物质属于氧化物的是( )A、纯碱(Na2CO3) B、酒精(C2H5OH) C、干冰(CO2) D、苛性钠(NaOH)5. 下列客现事实对应的微观解释正确的是( )A、把液化气压缩进钢瓶——分子体积变小 B、公园里闻到花的香味——分子不断运动 C、电解水得到氢气和氧气——水由氢分子和氧分子构成 D、金刚石和石墨的物理性质差异大——碳原子结构不同6. 长途运输活鱼,常用过氧化钙增氧。CaO2中Ca是+2价,则O的化合价为( )A、+2 B、0 C、-2 D、-17. 下列实验操作正确的是( )A、
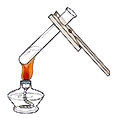 给液体加热
B、
给液体加热
B、 读取液体体积
C、
读取液体体积
C、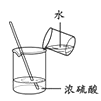 稀释浓硫酸
D、
稀释浓硫酸
D、 检查装置气密性
8. 下列实验现象描述不正确的是( )A、硝酸铵溶于水,溶液温度升高 B、红磷在空气中燃烧,产生大量白烟 C、浓硫酸涂在木棒上,木棒变黑 D、点燃羊毛纤维,闻到烧焦羽毛气味9. 人剧烈运动后,血液中产生较多乳酸(化学式为C3H6O3)。下则有关乳酸说法正确的是( )A、乳酸不属于有机化合物 B、一个乳酸分子中含有12个原子 C、乳酸的相对分子质量为90g D、乳酸中C,H,O三种元素的质量比为1:2:110. 下列各组离子在水中能大量共存的是( )A、K+、CO32-、H+ B、Ca2+、NO3-、Na+ C、Fe3+、OH-Cl- D、Ba2+、SO42-、K+11. 分别把X、Y、Z三种金属加入稀盐酸中,只有Z表面无现象。Y加入X的硝酸盐溶液中,有X析出。则三种金属的活动性顺序是( )A、Y>X>Z B、X>Y>Z C、X>Z>Y D、Z>Y>X12. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
检查装置气密性
8. 下列实验现象描述不正确的是( )A、硝酸铵溶于水,溶液温度升高 B、红磷在空气中燃烧,产生大量白烟 C、浓硫酸涂在木棒上,木棒变黑 D、点燃羊毛纤维,闻到烧焦羽毛气味9. 人剧烈运动后,血液中产生较多乳酸(化学式为C3H6O3)。下则有关乳酸说法正确的是( )A、乳酸不属于有机化合物 B、一个乳酸分子中含有12个原子 C、乳酸的相对分子质量为90g D、乳酸中C,H,O三种元素的质量比为1:2:110. 下列各组离子在水中能大量共存的是( )A、K+、CO32-、H+ B、Ca2+、NO3-、Na+ C、Fe3+、OH-Cl- D、Ba2+、SO42-、K+11. 分别把X、Y、Z三种金属加入稀盐酸中,只有Z表面无现象。Y加入X的硝酸盐溶液中,有X析出。则三种金属的活动性顺序是( )A、Y>X>Z B、X>Y>Z C、X>Z>Y D、Z>Y>X12. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( ) A、t1℃时,甲、乙的溶液中所含溶质质量相等 B、t2℃时,将50g甲加入5Og水中,可得到100g溶液 C、甲中含有少量乙时,可用降温结晶法提纯甲 D、t1℃时分别将甲、乙的饱和溶液升温至t2℃时,所得溶液的溶质质量分数甲>乙13. 下图为汽车尾气处理所涉及反应的微观过程,下列说法不正确的是( )
A、t1℃时,甲、乙的溶液中所含溶质质量相等 B、t2℃时,将50g甲加入5Og水中,可得到100g溶液 C、甲中含有少量乙时,可用降温结晶法提纯甲 D、t1℃时分别将甲、乙的饱和溶液升温至t2℃时,所得溶液的溶质质量分数甲>乙13. 下图为汽车尾气处理所涉及反应的微观过程,下列说法不正确的是( ) A、反应前后元素种类不变 B、反应前后原子数目没有增减 C、生成物的分子个数比为1: 1 D、该反应能减少有害气体排放14. 除去下列各物质中少量杂质,选用的方案不合理的是( )
A、反应前后元素种类不变 B、反应前后原子数目没有增减 C、生成物的分子个数比为1: 1 D、该反应能减少有害气体排放14. 除去下列各物质中少量杂质,选用的方案不合理的是( )选项
物质
所含杂质
方案
A
H2
H2O(气)
混合气体通过浓硫酸
B
KCl
MnO2
加水溶解、过滤、蒸发
C
CuO
C
在氧气流中加热
D
NaOH溶液
Ca(OH)2
加入过量K2CO3溶液,过滤
A、A B、B C、C D、D15. 有一包金属粉末,可能由Mg、Zn、Fe、Al、Ag等金属中的一种或几种组成,取该样品2.4g,加入100g稀硫酸恰好完全反应,得0.2gH2和无色溶液。下列说法正确的是( )A、样品中定只含有Mg B、样品中一定不含有Ag,可能含有Fe C、无色溶液中溶质总质量量为12g D、稀硫酸的溶质质量分数为19.6%二、填空题
-
16. 从下列选项中,选择一种适当的物质填空,并将字母序号填写在横线上。
A.维生素 B.氧气(或空气) C.尿素[CO(NH2)2]
D.一氧化碳(CO) E.氮气(N2) F.小苏打(NaHCO3)
(1)、空气中含量最多的气体是;(2)、油锅着火用锅盖盖火的原理是;(3)、黄瓜富含的营养素是;(4)、与血红蛋白结合使人中毒的气体是;(5)、植物叶色发黄可施用的化肥是;(6)、焙制糕点用的发酵粉主要成分之是。17. 请根据下列实验装置图回答问题: (1)、仪器a的名称是 , 仪器b的名称是。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,发生反应的化学方程式为 , 用装置C收集氧气,证明集满的方法是。(3)、实验室制取CO2 , 发生反应的化学方程式为 , 装置F是小亮制取CO2的气体发生装置,用它代替B装置的优点是(答出一点即可)。(4)、加热氯化铵和熟石灰固体混合物制取NH3 , 可选用的发生装置是 (填字母序号)。
(1)、仪器a的名称是 , 仪器b的名称是。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,发生反应的化学方程式为 , 用装置C收集氧气,证明集满的方法是。(3)、实验室制取CO2 , 发生反应的化学方程式为 , 装置F是小亮制取CO2的气体发生装置,用它代替B装置的优点是(答出一点即可)。(4)、加热氯化铵和熟石灰固体混合物制取NH3 , 可选用的发生装置是 (填字母序号)。已知NH3能使湿润的红色石蕊试纸变蓝。某同学用干燥的红色石蕊试纸检验反应生成的NH3 , 试纸变蓝,原因是。
18. 化学在改善人类生存环境,提高生活质量方面起着重要作用。(1)、(改善环境)温室效应和酸雨会威胁珊瑚礁生存。我国开展了南海珊瑚礁生态修复工作。我们把pH(填“>”、“<”或“=”)5.6的降雨称为酸雨。
(2)、为改善生存环境,倡导“低碳”生活。建议使用清洁能源。写出一种常见的清洁能源。(3)、(探测资源)近期,我国向月球背面成功发射一颗中继通信卫星,助力探测月球资源。月球上有丰富的核能原料He-3。He的原子结构示意图为_____(填字每序号)。
A、 B、
B、 C、
C、 (4)、月球土壤中有天然的铁、铝、银等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不易锈蚀的原因可能是。(5)、(研发材料)中国芯彰显中国“智”造。芯片的基材主要是高纯硅。
(4)、月球土壤中有天然的铁、铝、银等金属颗粒。根据铁锈蚀的条件分析,铁在月球上不易锈蚀的原因可能是。(5)、(研发材料)中国芯彰显中国“智”造。芯片的基材主要是高纯硅。硅元素在元素周期表中的信息如图所示,据图可得到的信息是______(填字母序号)。
 A、硅元素是非金属元素 B、硅元素的元素符号为Si C、硅元素在地壳里的含量排第二位(6)、下图是一种制备高纯硅的工艺流程图:
A、硅元素是非金属元素 B、硅元素的元素符号为Si C、硅元素在地壳里的含量排第二位(6)、下图是一种制备高纯硅的工艺流程图:
(查阅资料)常温下,氯化镁溶液呈中性。
①反应I的化学方程式: 2Mg+SiO2 Si+2MgO,该反应属于 (填基本反应类型)。反应II要在无氧气环境中进行,原因是(答出一种即可)。
②操作I的名称是过滤。过滤时液面应(填“高于”或“低于”) 滤纸边缘。所得粗硅应充分洗涤,以除去表面可能含有的盐酸、 (填化学式)。
③简要叙述检验盐酸已过量的方法。
④上述已知生产流程中,可以循环利用的物质是(填化学式)。
三、综合题
-
19. 盐城盛产海盐。某化学兴趣小组同学在市场购到粗盐,带回实验室进行提纯。(1)、①在溶解,过滤,蒸发等操作中,均用到的玻璃仪器是(填仪器名称)。
②配制50g质量分数为6%的NaCl溶液,需称量NaCl固体g,若用粗盐配制上述解液,则所配溶液中NaCl的质量分数会(填“偏大”、偏小”或“无影响“)。
(2)、探究活动:以NaCl为原料可以制取金属钠。兴趣小组同学认为Na是活泼金属,能与CuSO4等盐溶液反应,生成相应的金属单质。(提出问题)Na与CuSO4溶液反应,是否有Cu生成?
(设计实验)兴趣小组同学在老师的指导下,设计如图装置进行实验。

I.向大试管中加入一定体积煤油。
II.用小刀切一小块钠,放入大试管,塞上橡皮塞。
III.打开活塞,通过长颈漏斗向试管中加入CuSO4溶液。使煤油的液面升至胶塞,关闭活塞,观察现象。
(实验现象)(1)Na在煤油与溶液交界处上下来回振动。表面产生气泡,逐渐变小直至消失。(2)溶液颜色逐渐变淡,有蓝色絮状沉淀和少量黑色固体生成。(3)打开活塞,用燃着的木条放在尖嘴管口处,气体被点燃。
(查阅资料)①Na通常存放在煤油中;②煤油不溶于水且不与水反应;
③2Na+2H2O=2NaOH+H2↑;④Cu(OH)2 CuO+H2O。
(实验分析)
根据上述信息,可获知金属钠的物理性质是(答出一点即可)。
(3)、实验中长颈漏斗的作用(填数字序号)。①便于添加CuSO4溶液 ②收集气体 ③防止压强过大冲开活塞
(4)、对于产生的气体,有些同学猜想是H2 , 有些同学猜想是SO2。小组同学经过讨论,排除了SO2 , 理由是。经过进一步实验,确认气体是H2.(5)、将反应后的混合物过滤,向滤渣滴加足量稀硫酸,滤渣完全溶解。写出滤渣与稀硫酸反成的化学方程式(写出一个即可)。(实验结论)Na与CuSO4溶液反应,无Cu生成。
(实验反思)Na与CuSO4溶液无Cu生成,原因可能是。
(定量分析)另取一定量上述CuSO4溶液。完成下列实验。利用数据,计算无色溶液的溶质质量分数。(写出计算过程,滴入的酚酞溶液质量忽略不计。)
