2016年黑龙江省哈尔滨市松北区中考化学一模试卷
试卷更新日期:2016-04-22 类型:中考模拟
一、选择题(每题只有一个正确答案,共15分.)
-
1. 如图所示是四名同学宣传“化学与健康”的图片,叙述正确的是( )A、
 B、
B、 C、
C、 D、
D、 2. 厨房里发生的下列变化中,属于物理变化的是( )A、
2. 厨房里发生的下列变化中,属于物理变化的是( )A、 苹果腐烂
B、
苹果腐烂
B、 榨取果汁
C、
榨取果汁
C、 面包发霉
D、
面包发霉
D、 菜刀生锈
3. 在生活中,下列做法或说法正确的是( )A、用厨房清洁洗涤剂除去水垢 B、炒菜时食盐放多了可以用食醋中和 C、用合成纤维做内衣比用天然纤维做内衣穿着舒适 D、炒菜时油锅中的油不慎着火.用锅盖或加入青菜灭火4. 下列实验操作正确的是( )A、
菜刀生锈
3. 在生活中,下列做法或说法正确的是( )A、用厨房清洁洗涤剂除去水垢 B、炒菜时食盐放多了可以用食醋中和 C、用合成纤维做内衣比用天然纤维做内衣穿着舒适 D、炒菜时油锅中的油不慎着火.用锅盖或加入青菜灭火4. 下列实验操作正确的是( )A、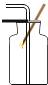 验满氧气
B、
验满氧气
B、 倾倒液体
C、
倾倒液体
C、 读取液体体积
D、
读取液体体积
D、 点燃酒精灯
5. 下列物质的应用不正确的是( )A、
点燃酒精灯
5. 下列物质的应用不正确的是( )A、 石墨做电刷
B、
石墨做电刷
B、 二氧化碳做气体肥料
C、
二氧化碳做气体肥料
C、 氧气供给呼吸
D、
氧气供给呼吸
D、 氮气填充闪光灯
6. 下列实验现象描述正确的是( )
氮气填充闪光灯
6. 下列实验现象描述正确的是( )
A、高温条件下木炭还原氧化铜:黑色固体逐渐变成光亮的铜 B、铁丝在氧气中燃烧:银白色固体剧烈燃烧,火星四射,放出大量的热,生成黑色固体 C、电解水实验:两个电极附近产生气泡,一段时间后,正、负极产生的气体体积比约为2:1 D、铜片放人硝酸银溶液中:紫红色固体表面有银白色固体产生,溶液由蓝色逐渐变为无色7. 下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )A、用稀盐酸除铁锈 Fe2O3+6HCl═2FeCl2+3H2O 复分解反应 B、用二氧化碳制碳酸饮料 CO2+H2O═H2CO3 化合反应 C、用铜和稀硫酸溶液反应制备铜:Cu+H2SO4═H2+CuSO4 置换反应 D、用氢氧化钠制碳酸钠 Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 复分解反应8. 以人为本,关注健康是人类永恒的主题.下列叙述正确的是( )
A、健康人体内胃液的pH范围是7.35﹣7.45 B、钾、铁、锌、碘都是人体所需的微量元素 C、烹调食物时不能用亚硝酸钠代替食盐 D、人体缺少维生素C会引起夜盲症9.液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
 A、丙烷是由3个碳原子和8个氢原子构成的 B、丙烷中碳、氢元素的质量比为3:8 C、一个丙烷分子中有26个电子 D、丙烷属于无机化合物10. 下列有关资源的叙述正确的是( )A、保护金属资源唯一的途径是防止金属的腐蚀 B、大气资源中含量最少的物质是稀有气体 C、人类可以利用的淡水量不到总水量的1% D、金属资源都以化合物形式存在11. 下列相关说法用粒子的知识解释错误的是( )
A、丙烷是由3个碳原子和8个氢原子构成的 B、丙烷中碳、氢元素的质量比为3:8 C、一个丙烷分子中有26个电子 D、丙烷属于无机化合物10. 下列有关资源的叙述正确的是( )A、保护金属资源唯一的途径是防止金属的腐蚀 B、大气资源中含量最少的物质是稀有气体 C、人类可以利用的淡水量不到总水量的1% D、金属资源都以化合物形式存在11. 下列相关说法用粒子的知识解释错误的是( )相关说法
解释
A
品红在水中扩散
分子不断运动
B
酒精和水混合后体积小于二者之和
分子之间有间隔
C
盐酸、硫酸溶液显酸性
溶液中都含有酸根离子
D
一氧化碳和二氧化碳化学性质不同
分子构成不同
A、A B、B C、C D、D12. 区分下列各组物质所用的两种方法都正确的是( )选项
需要区分的物质
方法一
方法二
A
氯化铵与氯化钾
分别与熟石灰混合研磨
观察颜色
B
食盐和纯碱
加食醋
溶解,滴加氯化钙溶液
C
硝酸钠与亚硝酸钠
溶解,滴加酚酞试液
尝味道
D
羊毛与涤纶
点燃,闻气味
观察色泽
A、A B、B C、C D、D13.甲、乙两种物质的溶解度曲线如图所示,下列有关叙述正确的是( )
 A、t1℃时,甲、乙溶液的溶质质量分数相等 B、t1℃时,甲的饱和溶液中含50g溶质 C、t1℃时,甲的饱和溶液升高温度后溶解度变大,溶质质量分数不变 D、甲物质的溶解度大于乙物质的溶解度14. 除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
A、t1℃时,甲、乙溶液的溶质质量分数相等 B、t1℃时,甲的饱和溶液中含50g溶质 C、t1℃时,甲的饱和溶液升高温度后溶解度变大,溶质质量分数不变 D、甲物质的溶解度大于乙物质的溶解度14. 除去下列物质中的少量杂质,所选试剂及操作都正确的是( )物 质
杂 质
试 剂
操 作
A
MgCl2溶液
HCl
过量Mg(OH)2
过滤
B
CO2
H2O
NaOH固体
干燥
C
H2O
悬浮物
明矾
吸附
D
NaNO3溶液
NaCl
过量AgNO3溶液
过滤
A、A B、B C、C D、D15. 据悉,6063铝合金的主要成分是铝、镁、硅.为测定该合金中硅的含量,进行如下实验:取一定量该合金,向其中加入100g质量分数为14.6%的稀盐酸,恰好完全反应后过滤得中性溶液和滤渣,将中性溶液蒸干得18.4g 固体,将滤渣洗涤、干燥后称量质量为2.8g.则该合金中硅的含量为( )A、28% B、70% C、40% D、20%二、非选择题(共40分)
-
16.
如图是农民种植的大豆,请填写下列空白:
 (1)、大豆可以做成豆浆、豆腐等,是人体获取(填除水外的一种营养素)的主要来源之一,为了使豆浆喝起来更香甜,喝豆浆时经常加一些白糖,它对生命活动的主要作用是在人体内经氧化放出 , 供机体活动和维持恒定体温的需要.(2)、为了使大豆增产增收,在种植过程中有时需施加适量钾肥,钾肥能增强作物的、能力,硫酸钾是常用的钾肥之一,其化学式为 .17. 据报,2014年6月2日,瑞士帕耶讷,全球最大的太阳能飞机“阳光动力2号”首飞.据报道,这架飞机机翼上安装有1.7万块超薄且高效能的太阳能电池板,翼展长达72米.太阳能板在日间吸收能量,让飞机在晚间也可飞行,飞行时间不再受燃油量限制.请回答下列问题:(1)、制成该飞机的机体材料可以是;
(1)、大豆可以做成豆浆、豆腐等,是人体获取(填除水外的一种营养素)的主要来源之一,为了使豆浆喝起来更香甜,喝豆浆时经常加一些白糖,它对生命活动的主要作用是在人体内经氧化放出 , 供机体活动和维持恒定体温的需要.(2)、为了使大豆增产增收,在种植过程中有时需施加适量钾肥,钾肥能增强作物的、能力,硫酸钾是常用的钾肥之一,其化学式为 .17. 据报,2014年6月2日,瑞士帕耶讷,全球最大的太阳能飞机“阳光动力2号”首飞.据报道,这架飞机机翼上安装有1.7万块超薄且高效能的太阳能电池板,翼展长达72米.太阳能板在日间吸收能量,让飞机在晚间也可飞行,飞行时间不再受燃油量限制.请回答下列问题:(1)、制成该飞机的机体材料可以是;a.韧性好、硬度大的锰钢
b.强度好、密度小的铝合金
c.抗腐蚀性好的不锈钢
(2)、太阳能飞机工作过程中的能量转化是从能开始,最终转化为能.(3)、硅是太阳能电池中不可缺少的材料,硅生产过程中的一个重要化学反应为:在高温条件下,利用单质碳还原二氧化硅,同时生成一种可燃性气体.则发生化学反应的方程式是 , 该反应前后硅元素的化合价分别为
.
 18.
18.用“
 ”和“
”和“  ”分别表示氮原子和氧原子,如图是氮气与氧气在放电条件下发生反应的微观模拟图.
”分别表示氮原子和氧原子,如图是氮气与氧气在放电条件下发生反应的微观模拟图.
请回答下列问题:
(1)、在B图中将相关粒子图形补充完整:(2)、此变化中不发生改变的粒子是(填名称);(3)、结合该图示从微观角度解释由B到C变化的实质是 .
19. 分类、类比是学习化学常用的方法.请回答:(1)、燃烧是人类最早利用的化学反应之一,火善用之为福,不善用之为祸.下面是一些常用的灭火方法:①熄灭液化气灶火焰时,关闭阀门;②木材着火时,用泡沫灭火器灭火;
③油锅着火时,用锅盖盖灭; ④熄灭酒精灯时,用灯帽盖灭;
⑤房屋着火时,用高压水枪灭火; ⑥森林着火时,将大火蔓延线路前的一片树木砍掉.
请你从灭火原理角度,选择一种分类标准进行分类:
分类标准 , 包括事例 (填序号)
(2)、查阅资料可知:过氧化钠(Na2O2)能与水发生如下反应:2Na2O2+2H2O═4NaOH+O2↑,而过氧化钙(CaO2)与过氧化钠类似也能与水反应,写出该反应的化学方程式 .
20.如图是某同学在实验室加热高锰酸钾制取氧气的装置图.
请回答下列问题:
 (1)、在图中标出仪器A的名称,并将实验装置图补充完整;(2)、写出制取氧气的化学方程式;(3)、仪器A在该实验中的作用是;(4)、停止加热时,先要把导管移出水面,然后再熄灭酒精灯,防止因试管内温度 , 气体压强外界,水槽中的水倒吸入试管,使试管因骤然冷却而炸裂.21.
(1)、在图中标出仪器A的名称,并将实验装置图补充完整;(2)、写出制取氧气的化学方程式;(3)、仪器A在该实验中的作用是;(4)、停止加热时,先要把导管移出水面,然后再熄灭酒精灯,防止因试管内温度 , 气体压强外界,水槽中的水倒吸入试管,使试管因骤然冷却而炸裂.21.如图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.请回答:
 (1)、写出乙和丙的化学式:
(1)、写出乙和丙的化学式:乙 , 丙;
(2)、写出甲和乙反应的化学方程式:;(3)、丙和丁反应的现象为 .22. 某同学发现,做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.【提出问题】溶液中的溶质是什么?
【猜想与假设】
A同学:该溶液没有变质,只含有NaOH
B同学:该溶液全部变质,只含有Na2CO3
C同学:该溶液部分变质,含有NaOH和Na2CO3
【查阅资料】Na2CO3溶液呈碱性
【实验探究】B同学为了验证自己的猜想,取少量溶液于试管中,向其中滴加少量的稀盐酸,观察到无明显现象.由此B同学得出结论:自己的猜想不成立,A同学的猜想成立.
(1)、【评价与交流】请你评价B同学的结论: .同学们经过讨论后一致认为:B同学在验证自己的猜想时,若将所加试剂调换成足量的另一种试剂(填化学式),观察到有产生,待不继续反应后,继续滴加 , 既能验证自己的猜想.也能确定溶液中溶质的成分.
C同学通过该方案进行实验,最终确定了溶液中的溶质成分.
(2)、【归纳与总结】通过上述实验我们能够总结出:在确定氢氧化钠的变质程度时,一般先 , 再在就可以确定溶液中的溶质成分.23. 石灰石的主要成分是碳酸钙.欲测定某石灰石样品中碳酸钙的质量分数,请回答下列问题:(1)、欲配制100g的7.3%的稀盐酸,需36.5%的浓盐酸的质量是;(2)、将石灰石粉碎,加入稀盐酸后发生反应的化学方程式是;(3)、若称取12.5g 石灰石粉末放在烧杯里,然后往烧杯中加入刚配制的稀盐酸100g,恰好完全反应后,称得反应剩余物为108.1g.(假设其他物质不与盐酸反应),求解石灰石中碳酸钙质量(X)的比例式为;(4)、此石灰石样品中碳酸钙的质量分数为;(5)、向反应后过滤所得滤液中加入5.4g 水,则最终溶液中溶质的质量分数是;(6)、若某建筑工地需要含杂质5%的生石灰2240t,用煅烧石灰石的方法制取,则需这种石灰石的质量是(假设制取过程中石灰石的利用率为95%).