黑龙江省大庆市肇源县2016-2017学年五四制九年级上学期化学期中考试试卷
试卷更新日期:2017-09-13 类型:期中考试
一、选择题
-
1. 下列物质的化学名称与俗名,对应错误的是( )A、汞——水银 B、氧化钙——熟石灰、消石灰 C、碳酸氢钠——小苏打 D、氢氧化钠——烧碱、火碱、苛性钠2. 观察和实验是学习科学的重要方式,下列实验中观察到的颜色正确的是( )A、铁锈放入稀盐酸中溶液变黄色 B、酚酞试液滴入硫酸溶液中变红色 C、硫在氧气中燃烧发出微弱的淡蓝色火焰 D、铁片放入硫酸铜溶液中一段时间,溶液一定浅绿色。3. 下列实验操作正确的是( )A、
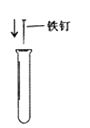 B、
B、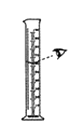 C、
C、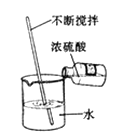 D、
D、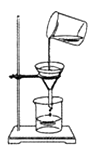 4. 反应MnO2+4HCl(浓) △ MnCl2+2H2O+Cl2↑,常用于实验室制取氯气。在该反应的反应物和生成物中,不存在的物质种类是( )A、酸 B、碱 C、盐 D、单质5. 配制溶质质量分数为5%的下列溶液,能达到目的是( )
4. 反应MnO2+4HCl(浓) △ MnCl2+2H2O+Cl2↑,常用于实验室制取氯气。在该反应的反应物和生成物中,不存在的物质种类是( )A、酸 B、碱 C、盐 D、单质5. 配制溶质质量分数为5%的下列溶液,能达到目的是( )
A、称取5.0g氯化钾,溶解在95mL.水中,充分搅拌 B、称取5.0g生石灰,放入95mL,水中,充分搅拌 C、量取5.0mL浓盐酸,倒入95mL.水中,充分搅拌 D、称取5.0g碳酸钙,放入95mL水中,充分搅拌6. 除去下列物质中含有的杂质所选用试剂或操作方法不正确的一组是( )物 质
所含杂质
除去杂质的试剂或方法
A
NaCl溶液
Na2CO3
过量盐酸,加热
B
CuO
Cu
灼烧
C
KCl
KClO3
MnO2 , 加热
D
O2
H2O
浓硫酸,干燥
A、A B、B C、C D、D7. “探险队员”--硫酸,不小心走进了有许多 “吃人野兽”(即能与硫酸发生化学反应的物质)的小山,逃生路线由许多种,有一条路线处处是陷阱,即为入口→③→⑤→⑦→⑨→出口,则该线路涉及的物质为( ) A、Zn、Fe(OH)3、Cu、Fe B、SO3、Cu、NaCl、HCl C、Na2CO3、Fe(OH)3、Zn、Fe D、SO3、Cu、NaCl、CuO8. 下列图像不能正确反映其对应变化关系的是( )
A、Zn、Fe(OH)3、Cu、Fe B、SO3、Cu、NaCl、HCl C、Na2CO3、Fe(OH)3、Zn、Fe D、SO3、Cu、NaCl、CuO8. 下列图像不能正确反映其对应变化关系的是( )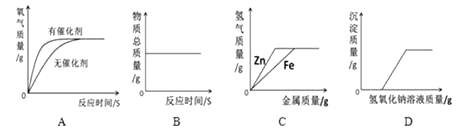 A、用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 B、一定质量的红磷在密闭容器中燃烧 C、向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 D、向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液9. 杯中加入10.2g碳酸镁和氧化镁的混合物,右边烧杯中加入8g铜,充分反应后,天平重新平衡,则所加入混合物中氧化镁的质量为( )
A、用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 B、一定质量的红磷在密闭容器中燃烧 C、向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 D、向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液9. 杯中加入10.2g碳酸镁和氧化镁的混合物,右边烧杯中加入8g铜,充分反应后,天平重新平衡,则所加入混合物中氧化镁的质量为( )
A、1.8g B、2.2g C、6g D、8g10. 根据你学过的化学知识,判断下列说法正确的是( )A、经常用水冲洗自行车可以防锈 B、可用燃着的火柴检查液化气罐是否泄漏 C、在煤炉上放一壶水,可以防止一氧化碳中毒 D、用铁锅烹饪会在食物中留有人体需要的铁元素11. 下列有关实验现象的描述正确的是( )A、木炭在空气中燃烧,发出白光并放热 B、镁条在空气中燃烧,放出大量的白色烟雾,同时在石棉网上得到一种白色固体 C、CO通过灼热的氧化铁则固体由红棕色变为黑色 D、铁丝在空气中燃烧,火星四射,发光放热12. 下列叙述正确的是 ( )①分子是保持物质性质的一种微粒
②原子是不能再分的一种微粒
③有单质生成的反应一定是置换反应
④有盐和水生成的反应一定是中和反应
⑤含有氧元素的化合物一定是氧化物
⑥由不同种元素组成的纯净物一定是化合物
A、①③ B、②③⑥ C、⑤⑥ D、⑥13. R元素原子的最外层电子数为2,下列关于R原子和R离子的说法正确的是( )A、相对原子质量相同 B、电子层数相同 C、化学性质相同 D、最外层电子数相同14. 下列实验操作正确的是( )A、称量固体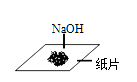 B、量取9.5mL液
B、量取9.5mL液 C、稀释浓硫酸
C、稀释浓硫酸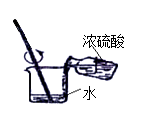 D、滴加液
D、滴加液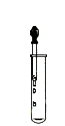 15. 久置于空气中的石灰水,表面会形成一层白膜.此时溶液的pH比变化前的pH( )A、偏大 B、偏小 C、一样 D、无法比较16. 对下列实验过程的评价,正确的是( )A、向某固体中滴加稀盐酸,有气泡产生,该固体一定是碳酸盐 B、在无色溶液中滴入酚酞试液,溶液变红色,该溶液一定是碱的溶液 C、生石灰块投入水中,水会沸腾,说明生石灰变成熟石灰的过程是放热反应 D、用小木棍蘸少量浓硫酸,小木棍变黑——浓硫酸有吸水性17. 航天科学技术测得,三氧化二碳(C2O3)是金星大气层的成分之一,化学性质与一氧化碳相似。下列有关三氧化二碳的说法不正确的是( )
15. 久置于空气中的石灰水,表面会形成一层白膜.此时溶液的pH比变化前的pH( )A、偏大 B、偏小 C、一样 D、无法比较16. 对下列实验过程的评价,正确的是( )A、向某固体中滴加稀盐酸,有气泡产生,该固体一定是碳酸盐 B、在无色溶液中滴入酚酞试液,溶液变红色,该溶液一定是碱的溶液 C、生石灰块投入水中,水会沸腾,说明生石灰变成熟石灰的过程是放热反应 D、用小木棍蘸少量浓硫酸,小木棍变黑——浓硫酸有吸水性17. 航天科学技术测得,三氧化二碳(C2O3)是金星大气层的成分之一,化学性质与一氧化碳相似。下列有关三氧化二碳的说法不正确的是( )
A、C2O3中碳元素的质量分数约为33.3% B、C2O3具有还原性 C、充分燃烧的产物是CO2 D、C2O3能使澄清石灰水变浑浊18. 在一定条件下,反应物溶液中溶质的质量分数越大,化学反应的速率越快。现有50g溶质质量分数为32%的硫酸溶液,与足量的锌粒反应,为了减缓化学反应的速率,而又不影响生成氢气的总质量,可向该溶液中加入适量的( )
A、氢氧化钾溶液 B、氯化钾溶液 C、碳酸钾溶液 D、水19. 向AgNO3、NaNO3、Cu(NO3)2混合液中加入一定量的锌粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,滤液中存在的阳离子一定有( )
A、Ag+、Cu2+ B、Cu2+、Zn2+ C、Zn2+、Na+ D、Zn2+、Ag+20. 下列所示的图像能反映相对应实验的是( )A、 向pH=12的Ca(OH)2溶液中不断加水稀释 B、 向碳酸钙固体中逐滴加入稀盐酸至过量
B、 向碳酸钙固体中逐滴加入稀盐酸至过量 C、在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
C、在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出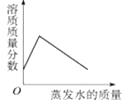 D、将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
D、将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
二、填空题
-
21. 一些食物的近似pH如下表:
食物
苹果
葡萄
牛奶
玉米
pH
2.9~3.3
3.5~4.5
6.3~6.6
6.8~8.0
(1)、苹果汁和葡萄汁相比较,酸性较强的是 , 它能使石蕊试液变色。(2)、人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用的食物是。(3)、鸡蛋壳中含有CaCO3 , 以前因胃酸过多导致胃痛时,有人吃鸡蛋壳粉。现今,许多冶疗胃酸过多的药品的有效成分是氢氧化铝,而不是CaCO3 , 提出一种理由说明为什么氢氧化铝优越于碳酸钙 , 写出氢氧化铝与胃酸反应的化学方程式。22. 根据问题填空:
(1)、洗洁精能清除油污,这是利用它的作用。(2)、上海世博园内安装的“直饮水”机,采用“活性炭+超滤膜+紫外线”净水工艺。活性炭在此起作用,净化后的水属于(选填“纯净物”或“混合物”)。(3)、在含有硫酸镁、硫酸铜的工业废水里加入过量的锌粉,充分反应后过滤,所得固体是(填写化学式)。(4)、化学为体育不仅雪中送炭,而且锦上添花。举重、体操等项目的运动员在比赛前常用白色的“镁粉”搓手,这是因为“镁粉”质轻、吸水性好,可做防滑剂。“镁粉”的有效成分是碱式碳酸镁,它不可燃,300℃即分解,其分解的化学方程式是:Mg5(OH)2(CO3)4 300℃ 5MgO+x+4CO2 , 则X的化学式是;根据这些信息,还能推出“镁粉”的另一种用途是。
23. 如图是a、b、c三种物质的溶解度曲线,请据图回答: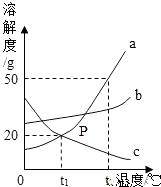 (1)、t2℃时,a、b、c三种物质的溶解度由大到小的顺序是(填序号,下同);(2)、t2℃时,将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为g;(3)、将t2℃时a、b、c三种物质的饱和溶液降低温度到 t1℃时,这三种溶液中溶质质量分数的大小关系是 .(4)、若要从a中含有少量b的混合溶液中提纯a,可用的方法是。24. 下图是实验室制取气体的装置图。回答下列问题:
(1)、t2℃时,a、b、c三种物质的溶解度由大到小的顺序是(填序号,下同);(2)、t2℃时,将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为g;(3)、将t2℃时a、b、c三种物质的饱和溶液降低温度到 t1℃时,这三种溶液中溶质质量分数的大小关系是 .(4)、若要从a中含有少量b的混合溶液中提纯a,可用的方法是。24. 下图是实验室制取气体的装置图。回答下列问题: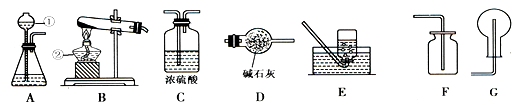 (1)、指出下列编号仪器名称:① ②。(2)、实验室用过氧化氢溶液和二氧化锰混合物制氧气时选用的发生装置是 , 反应的化学方程式为:。(3)、氨气是一种无色有刺激性气味的气体,极易溶于水,氨水显碱性。实验室用加热氯化铵和熟石灰两种固体的混合物的方法制取氨气,同时生成氯化钙和水。
(1)、指出下列编号仪器名称:① ②。(2)、实验室用过氧化氢溶液和二氧化锰混合物制氧气时选用的发生装置是 , 反应的化学方程式为:。(3)、氨气是一种无色有刺激性气味的气体,极易溶于水,氨水显碱性。实验室用加热氯化铵和熟石灰两种固体的混合物的方法制取氨气,同时生成氯化钙和水。①写出实验室制氨气的化学方程式。
②若实验室制取并收集干燥的氨气选择装置的连接顺序是(填序号)。
③按图(Ⅰ)连接,挤压胶头滴管使少量的水进入烧瓶,打开止水夹,烧瓶中就可以看到色的喷泉。按图(Ⅱ)连接,你怎样操作,才能引发喷泉:。
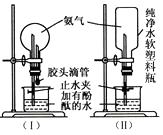 25. 新闻链接:2005年3月19日,某校3位学生在实验操作中不慎将钠与水接触,引发火灾…………
25. 新闻链接:2005年3月19日,某校3位学生在实验操作中不慎将钠与水接触,引发火灾…………阅读了上述新闻之后,好奇的唐唐猜测:金属钠能与水发生反应。她通过查找资料获得了以下信息:
常温下在空气中易氧化成氧化钠(Na2O),氧化钠可与水化合生成相应的碱;
钠能与水剧烈反应,放出大量的热,生成一种碱和氢气。
她在老师的指导下设计并进行了实验,并做了如下实验记录:
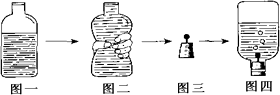
①取一空矿泉水瓶,加入纯净水,仅留一小段空隙,如上图一所示;
②用手挤压矿泉水瓶,除去里面的空气,如上图二所示;
③在胶塞上固定一根大头针,用针扎起一块金属钠,如上图三所示;
④迅速用胶塞塞住挤瘪的瓶口,倒置,如上图四所示;
⑤待完全反应后,打开瓶塞,检验产生的气体;
⑥在矿泉水瓶中滴入数滴A试剂,溶液呈红色。
请根据唐唐的实验过程与实验记录,回答以下问题:
(1)、写出试剂A的名称:;(2)、写出钠与水反应的化学方程式:;(3)、写出氧化钠与水反应的化学方程式(4)、为什么在实验步骤②中要除去矿泉水瓶中的空气? ;(5)、本实验中,对取用的金属钠的大小是否有要求,为什么?26. 请你参与实验室配制一定溶质质量分数的硝酸钾溶液的实验,并进行实验过程的探究:(1)、计算:配制50g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为g,所需蒸馏水的体积为mL(水的密度约为1g/mL).(2)、称量:分别在天平左右两盘放上纸片,调节平衡后,应 (填标号).A、先在托盘上放置所需的砝码,再添加硝酸钾直至天平平衡. B、先添加所需的硝酸钾,再添加砝码到所在的托盘直至天平平衡.(3)、【探究一】:在称量过程中,某同学的称量操作如图所示,你认为该操作对本次实验的数据处理的正确性(填“有”或“没有”)影响,理由是 .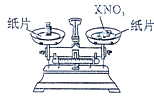 (4)、量取:准确量取所需蒸馏水要用到的仪器是(选填图中的标号).
(4)、量取:准确量取所需蒸馏水要用到的仪器是(选填图中的标号).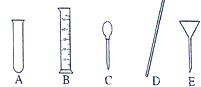
溶解:将称量好的硝酸钾和蒸馏水混合溶解.
(5)、【探究二】:20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出计算所需的数据为:g/mL.KNO3溶液的密度
温度℃
质量分数%
20
40
60
4
1.023
1.016
1.007
10
1.063
1.054
1.044
三、推断题
-
27. 如图所示A~G是初中化学常见的物质。图中 “→”表示转化关系,“—”表示相互能反应。已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物。请回答:
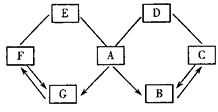 (1)、G的化学式为 , E与F发生化学反应的基本类型是 。写出物质B的一种用途;(2)、C、D发生反应的化学方程式可能为。28. 有A、B、C三种化合物,已知A是强酸,B是硝酸盐,C是 强碱,它们都溶于水,能发生以下反应,B、C混合,生成蓝色沉淀;A、C混合,生成难溶于稀硝酸的白色沉淀E。试推断:B的化学式为 ,C的化学式为 , E的化学式为 。
(1)、G的化学式为 , E与F发生化学反应的基本类型是 。写出物质B的一种用途;(2)、C、D发生反应的化学方程式可能为。28. 有A、B、C三种化合物,已知A是强酸,B是硝酸盐,C是 强碱,它们都溶于水,能发生以下反应,B、C混合,生成蓝色沉淀;A、C混合,生成难溶于稀硝酸的白色沉淀E。试推断:B的化学式为 ,C的化学式为 , E的化学式为 。四、计算题
-
29. 在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题:
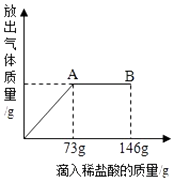 (1)、当滴加了73g稀盐酸时,放出气体的总质量为 g(2)、当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式).(3)、当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中溶质的质量分数.(计算结果保留一位小数)
(1)、当滴加了73g稀盐酸时,放出气体的总质量为 g(2)、当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式).(3)、当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中溶质的质量分数.(计算结果保留一位小数)