2020年中考化学实验专题复习 专题六 粗盐提纯
试卷更新日期:2020-04-27 类型:二轮复习
一、单选题
-
1. 在“粗盐中难溶性杂质的去除”实验中,不需要进行的操作是()A、溶解 B、过滤 C、蒸发 D、蒸馏2. 除去下列各物质中的少量杂质,所用方法不可行的是()
选项
物质
杂质
除去杂质的方法
A
CO2
CO
将混合气体通过灼热的CuO
B
NaCl
泥沙
加水溶解、过滤、蒸发
C
Cu粉
Fe粉
用磁铁吸出
D
KCl
KClO3
加入少量MnO2 , 加热
A、A B、B C、C D、D3. 将粗盐溶解、过滤,除去泥沙后,溶液中仍含有少量的CaCl2、MgCl2、Na2SO4 , 为除去这些杂质,需用到①BaCl2溶液 ②Na2CO3溶液 ③NaOH溶液三种试剂(为将杂质除尽所加试剂均稍过量,且过量物质须在后续操作中被除去),充分反应后,过滤,再向滤液中加入适量的稀盐酸,加热蒸发,即可获得较为纯净的NaCl固体。以上三种试剂的加入顺序错误的是( )A、①②③ B、①③② C、②③① D、③①②4. 在“粗盐的初步提纯”实验中,下列操作正确的是()A、 取用粗盐
B、
取用粗盐
B、 溶解粗盐
C、
溶解粗盐
C、 过滤粗盐水
D、
过滤粗盐水
D、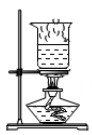 蒸干滤液
蒸干滤液
二、填空题
-
5. 精盐中含有较多的可溶性杂质(氯化镁、氯化钙)和不溶性杂质,进行粗盐提纯的实验:
①实验步骤包括:a 计算产率,b 过滤,c 溶解,d 蒸发,e 称量。实验步骤的正确顺序是:e, , a(填写编号)。
②最后得到的精盐属于(填“混合物”或“纯净物”。)
③已知:产率= ×100%,某实验小组计算出的产率比其他组的产率低,你认为有哪些原因:。
6. 为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:①a.计算产率,b.过滤,c.溶解,d.蒸发,e.称量粗盐,f.称量精盐。实验步骤的正确顺序是:、a(填编号)。
②称量时正确的操作次序是(填字母序号)。
a.校正,b.去皮,c.放称量纸,d.放食盐,e.读数
③过滤时用到的玻璃仪器有玻璃棒、烧杯、 , 其中玻璃棒的作用是。实验过程中发现过滤两次滤液仍然浑浊,可能的原因是(写一点)。
④最后得到的精盐属于(填“混合物”或“纯净物”)。
组别
1
2
3
4
产率
75%
65%
88%
72%
教师评价
偏低
偏低
偏高
偏低
⑤已知:产率= ×100%。各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是。
A.第1组:烧杯里的食盐未溶解完就开始过滤
B.第2组:没有蒸发干,精盐中仍然有水分
C.第3组:滤液浑浊就开始蒸发
D.第4组:过滤时滤液高于滤纸的边缘
7. 海水晒盐得到的粗盐中往往含有少量泥沙,为了除去泥沙等不溶物。某小组设计了如图所示的实验: (1)、在粗盐提纯的操作中,正确的操作顺序为(填序号) , 玻璃棒在C中的作用是。(2)、其中A的操作名称为 , 目的是为了除去(填化学式)。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还应采取的措施是。(3)、其中B的操作名称为 , 该操作中雨要将圆形滤纸折叠处理,下列图示中不该出现的情形是(填编号):
(1)、在粗盐提纯的操作中,正确的操作顺序为(填序号) , 玻璃棒在C中的作用是。(2)、其中A的操作名称为 , 目的是为了除去(填化学式)。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还应采取的措施是。(3)、其中B的操作名称为 , 该操作中雨要将圆形滤纸折叠处理,下列图示中不该出现的情形是(填编号): (4)、若在实验B过程中发现速度较慢。可能的原因是(________)A、固体颗粒阻碍了液体通过滤纸孔隙 B、滤纸有破损 C、滤纸没有紧贴漏斗内壁 D、滤纸高度超过了漏斗边缘(5)、实验结束后称量获得的精盐,并计算其纯度。发现结果偏高,其可能的原因是(填编号)。
(4)、若在实验B过程中发现速度较慢。可能的原因是(________)A、固体颗粒阻碍了液体通过滤纸孔隙 B、滤纸有破损 C、滤纸没有紧贴漏斗内壁 D、滤纸高度超过了漏斗边缘(5)、实验结束后称量获得的精盐,并计算其纯度。发现结果偏高,其可能的原因是(填编号)。A食盐没有全部溶解即过滤 B蒸发时食盐飞溅剧烈
C蒸发后,所得精盐很潮湿 D器皿上沾有的精盐没全部转移到称量纸上
三、实验探究题
-
8. 根据如图所示实验装置,回答问题。
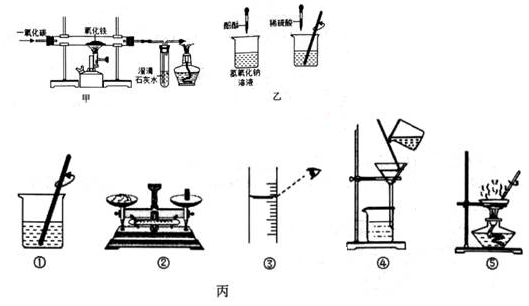 (1)、甲实验中,实验前先通入CO的目的是 , 该反应的化学方程式为。(2)、乙实验中,观察到 ,说明稀硫酸与氢氧化钠发生了反应。(3)、丙实验中,若要除去粗盐中难溶性的杂质,其正确的操作步骤为(填序号),若按照②③①的步骤配制50g16%的氯化钠溶液,所配制溶液的溶质质量分数 (选填“偏大”或“偏小”)9. 某同学通过下列实验步骤测定粗盐中(假定只含不溶性杂质)氯化钠的百分含量,请根据实验步骤回答下列问题。(1)、将电子天平放在水平桌面上。
(1)、甲实验中,实验前先通入CO的目的是 , 该反应的化学方程式为。(2)、乙实验中,观察到 ,说明稀硫酸与氢氧化钠发生了反应。(3)、丙实验中,若要除去粗盐中难溶性的杂质,其正确的操作步骤为(填序号),若按照②③①的步骤配制50g16%的氯化钠溶液,所配制溶液的溶质质量分数 (选填“偏大”或“偏小”)9. 某同学通过下列实验步骤测定粗盐中(假定只含不溶性杂质)氯化钠的百分含量,请根据实验步骤回答下列问题。(1)、将电子天平放在水平桌面上。称取粗盐样品W克,称量时应在托盘上各先后(填“放称量纸”、“按去皮键”)。
(2)、将粗盐溶于适量蒸馏水,溶解时应在(填名称)里进行,用玻璃棒搅拌,玻璃棒的作用是。(3)、过滤。开始时学生的操作如图所示,请按从上向下顺序指出图中的错误:①过滤时没有使用引流,②没有紧靠烧杯内壁。学生纠正错误后,进行正确过滤。 (4)、将滤液加热蒸发,加热蒸发滤液应在(填仪器名称)中进行,使用玻璃棒的作用是。(5)、计算粗盐的纯度,蒸发后得到纯净NaCl固体W1克,则盐的纯度为×100%(写计算式)。10. 实验课上,老师知道某兴趣小组进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。
(4)、将滤液加热蒸发,加热蒸发滤液应在(填仪器名称)中进行,使用玻璃棒的作用是。(5)、计算粗盐的纯度,蒸发后得到纯净NaCl固体W1克,则盐的纯度为×100%(写计算式)。10. 实验课上,老师知道某兴趣小组进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。(实验名称)粗盐的提纯
(查阅资料)
①粗盐中含有泥沙及少量可溶性MgCl2、CaCl2、Na2SO4等杂质。
②Ba(OH)2是一种易溶于水的强碱。
(主要玻璃仪器)量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯
(主要试剂)粗盐样品、稀盐酸、BaCl2溶液,NaOH溶液,Na2CO3溶液,蒸馏水
(1)、(实验过程)步骤及目的
过程及说明
一、去除粗盐
中的泥沙
1.称取粗盐样品10.0g,用蒸馏水充分溶解
2.过滤去除泥沙的溶液I
以上两步操作中均需要使用到玻璃棒,玻璃棒的作用分别是:溶解时:;
过滤时:。
二、去除可溶
性杂质
将溶液I按如图流程图进行处理:

1、加入“过量NaOH溶液时”,发生反应的化学方程式是。
2、过滤后,所得的滤渣成分有种。
3、判断“稀盐酸适量”的方法是。
三、获得产品
将溶液Ⅱ注入(填仪器名称)中,蒸发结晶,观察到 , 停止加热,利用余热蒸干。装置完全冷却后,获得干燥的产品9.4g。
四、数据处理
该粗盐样品中氯化钠的质量分数是94%
(2)、(结果与反思)实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是。
(3)、小明提出,如果步骤二中只调换“过量的NaOH溶液”与“过量的BaCl2溶液”的加入顺序,对除杂结果也不会产生影响,你(填“同意”或“不同意”)小明的观点。11. 化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题: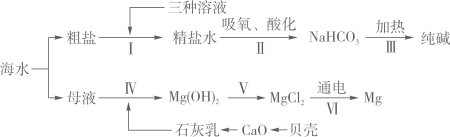 (1)、提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为(填字母序号);
(1)、提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为(填字母序号);a.稍过量的Na2CO3溶液
b.稍过量的BaCl2溶液
c.稍过量的NaOH溶液
(2)、母液中有MgCl2 , 却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是;(3)、步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是 , 写出该反应的化学方程式;(4)、化学变化是改造物质的重要途径。上述流程图中没有涉及的基本反应类型是。