2020年中考化学实验专题复习 专题五 酸碱中和
试卷更新日期:2020-04-27 类型:二轮复习
一、单选题
-
1. 向滴有酚酞的盐酸溶液中逐滴加入氢氧化钠溶液,所得溶液的pH与加入溶液体积关系如图所示。下列说法正确是( )
 A、反应过程中溶液温度降低 B、A点对应溶液的溶质为NaOH、NaCl C、恰好完全反应时溶液显中性 D、反应过程中溶液的颜色由红色变为无色2. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应 时,利用数字化传感器测得烧杯中溶液 pH 的变化,其图象如图所示,下列说法正确的是( )
A、反应过程中溶液温度降低 B、A点对应溶液的溶质为NaOH、NaCl C、恰好完全反应时溶液显中性 D、反应过程中溶液的颜色由红色变为无色2. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应 时,利用数字化传感器测得烧杯中溶液 pH 的变化,其图象如图所示,下列说法正确的是( ) A、图中 c点所示溶液呈碱性 B、图中 a点所示溶液中,含有的溶质是 Na2SO4 和 H2SO4 C、该实验是将氢氧化钠溶液逐滴滴加到盛有硫酸的烧杯中 D、由 a 点到 b点的 pH 变化过程证明酸和碱发生了中和反应3. 如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是( )
A、图中 c点所示溶液呈碱性 B、图中 a点所示溶液中,含有的溶质是 Na2SO4 和 H2SO4 C、该实验是将氢氧化钠溶液逐滴滴加到盛有硫酸的烧杯中 D、由 a 点到 b点的 pH 变化过程证明酸和碱发生了中和反应3. 如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是( ) A、反应后溶液中的粒子只有Na+、Cl﹣和H2O B、该反应属于复分解反应,反应前后溶剂质量不变 C、该反应的实质是HCl+NaOH=H2O+NaCl D、反应前后阴、阳离子的总数不变4. 某同学对证明氢氧化钠溶液与稀盐酸恰好完全中和,设计了下图所示的四种实验方案。通过对四个实验方案的评价,你认为最佳的实验方案是( )
A、反应后溶液中的粒子只有Na+、Cl﹣和H2O B、该反应属于复分解反应,反应前后溶剂质量不变 C、该反应的实质是HCl+NaOH=H2O+NaCl D、反应前后阴、阳离子的总数不变4. 某同学对证明氢氧化钠溶液与稀盐酸恰好完全中和,设计了下图所示的四种实验方案。通过对四个实验方案的评价,你认为最佳的实验方案是( ) A、A B、B C、C D、D5. 海水中镁元素的总储量约为2.1×1015t,可用于生产金属镁,目前世界生产的镁60%来自海水。利川用海水提取镁的工业流程如图所示。下列说法错误的是( )
A、A B、B C、C D、D5. 海水中镁元素的总储量约为2.1×1015t,可用于生产金属镁,目前世界生产的镁60%来自海水。利川用海水提取镁的工业流程如图所示。下列说法错误的是( ) A、沉淀槽中总的化学方程式为:MgCl2+CaO+H2O=Mg(OH)2↓+CaCl2 B、在上述流程中,元素的化合价均没有发生变化 C、反应器中发生的化学反应类型为中和反应 D、由贝壳制取生石灰的反应条件是高温6. 向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如下图所示。下列说法错误的是()
A、沉淀槽中总的化学方程式为:MgCl2+CaO+H2O=Mg(OH)2↓+CaCl2 B、在上述流程中,元素的化合价均没有发生变化 C、反应器中发生的化学反应类型为中和反应 D、由贝壳制取生石灰的反应条件是高温6. 向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如下图所示。下列说法错误的是() A、A点溶液中的溶质有2种 B、E点溶液中的溶质有3种 C、AB段有沉淀生成 D、F点溶液的pH>7
A、A点溶液中的溶质有2种 B、E点溶液中的溶质有3种 C、AB段有沉淀生成 D、F点溶液的pH>7二、填空题
-
7. 向盐酸溶液中滴NaOH溶液时pH变化如图所示
 (1)、中和反应实质是;(2)、A点溶液中的阳离子有。8. 下图是有关稀盐酸和氢氧化钠溶液发生化学反应的微观示意图.请回答下列问题:
(1)、中和反应实质是;(2)、A点溶液中的阳离子有。8. 下图是有关稀盐酸和氢氧化钠溶液发生化学反应的微观示意图.请回答下列问题: (1)、A中溶液能使紫色石蕊溶液显色,因为其中含有较多的(填粒子符号);B中溶液能使无色酚酞溶液显色,因为其中含有较多的(填粒子符号) .(2)、将50g 7.3% 的A中的溶液与50g 8% 的B中的溶液混合,得到C中的溶液,其中主要含有的粒子是(填粒子符号);C中的溶液中溶质的质量分数是 .
(1)、A中溶液能使紫色石蕊溶液显色,因为其中含有较多的(填粒子符号);B中溶液能使无色酚酞溶液显色,因为其中含有较多的(填粒子符号) .(2)、将50g 7.3% 的A中的溶液与50g 8% 的B中的溶液混合,得到C中的溶液,其中主要含有的粒子是(填粒子符号);C中的溶液中溶质的质量分数是 .三、实验探究题
-
9.(1)、酸与碱之间发生中和反应,其实质是酸溶液中大量自由移动的(填离子符号)和碱溶液中大量自由移动的(填离子符号)结合成生成水分子的过程请根据以下氢氧化钠溶液与稀硫酸反应的实验,回答问题。(2)、【实验1】用酚酞试液,向一锥形瓶中倾倒20g氢氧化钠溶液,滴入2滴酚酞试液,振荡,再逐滴滴入稀硫酸,边滴加边振荡,直至溶液为止,说明酸碱恰好完全反应,此时溶液中的主要溶质是。(3)、【实验2】用pH计,向一锥形瓶中倾倒20g氢氧化钠溶液,再逐滴滴入稀盐酸,振荡,读出pH.当pH═ , 说明酸碱恰好完全反应。(4)、【小结】除了用酸碱指示剂、pH试纸、pH计等外,还可用(填方法)检测中和反应是否发生。(5)、【拓展】中和反应属于复分解反应,复分解反应实质是某些阴、阳离子,结合生成气体、沉淀或水。请你分析:
①硫酸铜溶液与烧碱溶液混合后实际参加反应的离子(填离子符号下同);
②碳酸钾溶液与稀硫酸混合后实际参加反应的离子是。
(6)、【计算】25℃时,10g 19.6%的稀硫酸恰好和60克某浓度的氢氧化钠溶液完全反应,将反应后的溶液冷却到0℃时,溶液恰好达到饱和。求:原氢氧化钠溶液中溶质的质量分数。
(7)、反应后硫酸钠溶液中溶质的质量分数(不考虑水蒸发,保留小数点后一位)。(8)、求0℃时,硫酸钠的溶解度(保留小数点后一位)。10. 兴趣小组的同学探究盐酸与氢氧化钠溶液能发生中和反应,以及反应后溶液的成分,进行了如右下图所示的实验,并绘制了反应过程中烧杯内溶液的pH随加入溶液体积的变化曲线图。请你参与学习并填写空格: (1)、烧杯中盛放的是溶液;(2)、曲线上b点坐标为(18,7),该点所表示的意义是。(3)、同学们对反应后溶液的成分进行探究如下:
(1)、烧杯中盛放的是溶液;(2)、曲线上b点坐标为(18,7),该点所表示的意义是。(3)、同学们对反应后溶液的成分进行探究如下:【提出问题】反应后溶液中的微粒有什么?
【假设猜想】依据曲线上的点和已学
知识分析,提出了以下四种猜想:
猜想一:只有Na+、Cl-、H2O;
猜想二:有Na+、Cl-、H2O、H+;
猜想三:有Na+、Cl-、H2O、OH-
猜想四:有Na+、Cl-、H2O、H+、OH-。
小红同学认为猜想是不合理的,理由是 。
(4)、【实验探究】①小芳同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,说明猜想 不成立;
②小君同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,认为猜想一成立。小明同学认为小君同学的判断不科学,理由是 。
③小兰同学取烧杯中的溶液少量于试管中,滴加几滴碳酸钠溶液,观察到有气泡产生,由此断定猜想二成立。该实验中发生反应的化学方程式是。
【实验拓展】
请你用与①、②、③不同类别的试剂,设计另一种方案验证猜想二成立。
实验操作
实验现象
实验结论
猜想二成立
11. 现有如下药品:NaOH溶液、浓H2SO4、Na2CO3溶液、Fe、Mg、酚酞试液、蒸馏水,用来进行酸碱中和实验。请回答:(1)、实验时涉及了如图所示的实验操作,其中错误的是______(填序号);A、稀释浓硫酸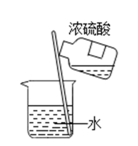 B、倾倒氢氧化钠溶液
B、倾倒氢氧化钠溶液 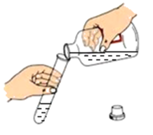 C、滴加酚酞试液
C、滴加酚酞试液  (2)、小明进行酸碱中和实验:在一支试管中加入NaOH溶液,再向其中滴加稀硫酸,振荡,最后滴加2滴酚酞试液,振荡,溶液不变色。小明据此判断酸和碱恰好完全反应。
(2)、小明进行酸碱中和实验:在一支试管中加入NaOH溶液,再向其中滴加稀硫酸,振荡,最后滴加2滴酚酞试液,振荡,溶液不变色。小明据此判断酸和碱恰好完全反应。①小红认为小明的结论不一定正确,理由是;
②请在小明实验的基础上,选用提供的药品继续实验,判断酸和碱是否恰好完全反应,实验方案为。
12.(1)、用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程溶液pH变化曲线如图所示:
①该反应的化学方程式是;
②该实验操作是将(写溶质的化学式)溶液逐滴加入到另一种溶液中。
(2)、若用稀硫酸代替(1)中的稀盐酸,将稀硫酸逐滴加入至盛有氢氧化钠溶液的烧杯中,当滴加到一定量并充分反应时,请对烧杯中溶质成分进行探究。(提出问题)此时烧杯中的溶液成分是什么?
(猜想与假设)I:Na2SO4 II: III:Na2SO4和NaOH
(实验与探究)
实验步骤
实验现象
实验结论
取少量上述烧杯中的溶液于试管中,滴加溶液
猜想III正确