浙江省丽水市2020年中考科学复习卷(一)
试卷更新日期:2020-04-24 类型:中考模拟
一、选择题(本大题共有15小题,1~5小题每题4分,6~15小题每题3分,共50分。每小题只有一个选项是正确的,不选、多选、错选均不得分)
-
1. “杂交水稻之父”袁隆平领衔的技术团队培育出了最新一批“海水稻”,是耐盐碱水稻的形象化称呼,是在海边滩涂等盐碱地生长的特殊水稻。这使得中国3亿亩盐碱地有望变成大粮仓!决定海水稻耐盐碱这一性状是( )A、基因 B、DNA C、染色体 D、细胞核2. 如图,平静秀丽的湖面上出现了数只天鹅,或俯冲嬉戏,或悠闲漂浮。下列关于天鹅在水中的倒影的说法正确的是( )
 A、是光折射形成的 B、与天鹅是等大的实像 C、悠闲漂浮的天鹅相对于自身倒影是运动的 D、天鹅从空中俯冲向水面,水中的倒影大小不变3. 2019年12月以来,湖北省武汉市发现多起病毒性肺炎病例,世界卫生组织将造成武汉肺炎疫情的新型冠状病毒临时命名为“2019新型冠状病毒”。从传染病角度看,“2019新型冠状病毒”是( )A、 传染源 B、传播途径 C、易感人群 D、病原体4. 热播影片《流浪地球》给我们描绘了一个场景:经历了漫长的时光后,太阳也终将走向尽头。下列有关说法中正确的是( )A、太阳表面发生的反应类型与原子弹爆炸相同 B、太阳的晚年演化:红巨星→白矮星→黑矮星 C、太阳大气的最里层是色球层,主要活动是出现耀斑 D、太阳黑子爆发时,地球上一定会发生剧烈的地壳运动5. 从微观视角看物质的变化是化学特有的思维方式。如图描述了NaOH溶液与盐酸反应的微观实质,C处应填入的物质化学式( )
A、是光折射形成的 B、与天鹅是等大的实像 C、悠闲漂浮的天鹅相对于自身倒影是运动的 D、天鹅从空中俯冲向水面,水中的倒影大小不变3. 2019年12月以来,湖北省武汉市发现多起病毒性肺炎病例,世界卫生组织将造成武汉肺炎疫情的新型冠状病毒临时命名为“2019新型冠状病毒”。从传染病角度看,“2019新型冠状病毒”是( )A、 传染源 B、传播途径 C、易感人群 D、病原体4. 热播影片《流浪地球》给我们描绘了一个场景:经历了漫长的时光后,太阳也终将走向尽头。下列有关说法中正确的是( )A、太阳表面发生的反应类型与原子弹爆炸相同 B、太阳的晚年演化:红巨星→白矮星→黑矮星 C、太阳大气的最里层是色球层,主要活动是出现耀斑 D、太阳黑子爆发时,地球上一定会发生剧烈的地壳运动5. 从微观视角看物质的变化是化学特有的思维方式。如图描述了NaOH溶液与盐酸反应的微观实质,C处应填入的物质化学式( ) A、NaCl B、NaOH C、HCl D、H2O6. 在4月25日,北部战区空军航空兵某旅进行超低空山谷飞行训练,提升飞行员突防突击能力。有关该场景的描述中正确的是( )
A、NaCl B、NaOH C、HCl D、H2O6. 在4月25日,北部战区空军航空兵某旅进行超低空山谷飞行训练,提升飞行员突防突击能力。有关该场景的描述中正确的是( ) A、以座位为参照物,飞行员是运动的 B、该款飞机使用的空气喷气发动机,属于热机 C、飞机在空中运动速度越快,具有的惯性也越大 D、飞机匀速飞行时,飞机所受的浮力和重力相等7. “类比法”“控制变量法”“推理法”“转换法”“建模法”等是科学实验中常用的研究方法。以下实例和其对应的科学研究方法不正确的是( )
A、以座位为参照物,飞行员是运动的 B、该款飞机使用的空气喷气发动机,属于热机 C、飞机在空中运动速度越快,具有的惯性也越大 D、飞机匀速飞行时,飞机所受的浮力和重力相等7. “类比法”“控制变量法”“推理法”“转换法”“建模法”等是科学实验中常用的研究方法。以下实例和其对应的科学研究方法不正确的是( )选项
科学实验
科学研究方法
A
研究牛顿第一定律
推理法
B
用磁感线描述磁场的强弱和方向
转换法
C
研究压力作用效果与压力大小有关
控制变量法
D
把电流比作水流,电压比作水压
类比法
A、A B、B C、C D、D8. 在其它条件不改变的情况下,对硝酸钾溶液进行如下处理,溶液的溶质质量分数大小比较正确的是( ) A、①>②>③ B、①=②>③ C、①=②<③ D、①=②=③9. 下列各项叙述中,属于种群的是( )A、人体内全部的微生物 B、校园里所有的植物 C、一个池塘里所有的草鱼 D、一块水稻田里的所有蝌蚪10. 如何从外部检测植物含水量的变化呢?科学家用条状石墨烯制成的湿敏电阻Rx附着在叶片上,植物含水量变低,Rx变小,电表示数变小;植物含水量变高,Rx变大,电表示数变大,电源电压恒定,R0为定值电阻,下列电路图中符合要求的是( )A、
A、①>②>③ B、①=②>③ C、①=②<③ D、①=②=③9. 下列各项叙述中,属于种群的是( )A、人体内全部的微生物 B、校园里所有的植物 C、一个池塘里所有的草鱼 D、一块水稻田里的所有蝌蚪10. 如何从外部检测植物含水量的变化呢?科学家用条状石墨烯制成的湿敏电阻Rx附着在叶片上,植物含水量变低,Rx变小,电表示数变小;植物含水量变高,Rx变大,电表示数变大,电源电压恒定,R0为定值电阻,下列电路图中符合要求的是( )A、 B、
B、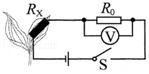 C、
C、 D、
D、 11. 小科用锌、氧化铜和足量的稀硫酸为原料制取单质铜,实验装置如图所示。下列有关分析正确的是( )
11. 小科用锌、氧化铜和足量的稀硫酸为原料制取单质铜,实验装置如图所示。下列有关分析正确的是( ) A、实验中,浓硫酸起到干燥氢气的作用 B、实验中,要得到6.4克铜,需要6.5克锌参加反应 C、实验时,应该先点酒精灯,再加入稀硫酸 D、实验时,可观察到试管内红色粉末变黑12. 为了提高自身的免疫力,可以注射免疫球蛋白,这一免疫反应和免疫球蛋白分别是( )A、特异性免疫、抗原 B、特异性免疫、抗体 C、非特异性免疫、抗原 D、非特异性免疫、抗体13. 在实验室,某同学将氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。加入氢氧化钠溶液的质量(横轴)与混合液中溶质质量(纵轴)的关系如图所示。以下说法不正确的是( )
A、实验中,浓硫酸起到干燥氢气的作用 B、实验中,要得到6.4克铜,需要6.5克锌参加反应 C、实验时,应该先点酒精灯,再加入稀硫酸 D、实验时,可观察到试管内红色粉末变黑12. 为了提高自身的免疫力,可以注射免疫球蛋白,这一免疫反应和免疫球蛋白分别是( )A、特异性免疫、抗原 B、特异性免疫、抗体 C、非特异性免疫、抗原 D、非特异性免疫、抗体13. 在实验室,某同学将氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。加入氢氧化钠溶液的质量(横轴)与混合液中溶质质量(纵轴)的关系如图所示。以下说法不正确的是( ) A、AB段反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O B、B点的溶质有3种 C、BC段质量减少的原因是因为生成了沉淀 D、CD段氢氧化钠溶液过量14. 抗生素作为治疗细菌感染的特效药被广泛使用。近年来,出现了一些“超级细菌”,多种抗生素对它们不起作用。下列说法正确的是( )A、“超级细菌”细胞核大,繁殖能力超强 B、“超级细菌”接触了抗生素后逐渐产生了抗药性 C、抗生素质量与前几年相比有所下降 D、“超级细菌”的形成是抗生素不断选择的结果15. 小朋友从滑梯匀速下滑的过程中,下列说法正确的是( )A、动能不变,重力势能减小,机械能减小 B、动能不变,重力势力增大,机械能不变 C、动能减小,重力势能增大,机械能不变 D、动能减小,重力势能减小,机械能减小
A、AB段反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O B、B点的溶质有3种 C、BC段质量减少的原因是因为生成了沉淀 D、CD段氢氧化钠溶液过量14. 抗生素作为治疗细菌感染的特效药被广泛使用。近年来,出现了一些“超级细菌”,多种抗生素对它们不起作用。下列说法正确的是( )A、“超级细菌”细胞核大,繁殖能力超强 B、“超级细菌”接触了抗生素后逐渐产生了抗药性 C、抗生素质量与前几年相比有所下降 D、“超级细菌”的形成是抗生素不断选择的结果15. 小朋友从滑梯匀速下滑的过程中,下列说法正确的是( )A、动能不变,重力势能减小,机械能减小 B、动能不变,重力势力增大,机械能不变 C、动能减小,重力势能增大,机械能不变 D、动能减小,重力势能减小,机械能减小二、填空题(本大题共有10小题,每空2分,共40分)
-
16. 空气是一种宝贵的自然资源,如图是以空气、天然气等为原料合成尿素[CO(NH)2]的流程。
 (1)、第一步先从空气中分离出X和O2 , 请写出X的化学式: 。(2)、请写出合成尿素的化学方程式为:。17. 图甲为显微镜结构图,图乙为显微镜下观察到小鱼尾鳍内血液流动的情况(箭头表示血流的方向)。
(1)、第一步先从空气中分离出X和O2 , 请写出X的化学式: 。(2)、请写出合成尿素的化学方程式为:。17. 图甲为显微镜结构图,图乙为显微镜下观察到小鱼尾鳍内血液流动的情况(箭头表示血流的方向)。 (1)、通常情况下,使用(选填“高倍”或“低倍”)显微镜观察尾鳍血管内血液的流动情况。(2)、血管(选填“①”或“②”)是小鱼尾鳍内的小动脉。18. 将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况下(约20℃,1.01x105Pa)的体积。同学们拟选用下列实验装置完成这个实验。请回答:
(1)、通常情况下,使用(选填“高倍”或“低倍”)显微镜观察尾鳍血管内血液的流动情况。(2)、血管(选填“①”或“②”)是小鱼尾鳍内的小动脉。18. 将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况下(约20℃,1.01x105Pa)的体积。同学们拟选用下列实验装置完成这个实验。请回答: (1)、实验中,最简易的装置连接顺序是①→ →⑥(填接口的数字)。(2)、实验中,如果用止水夹夹住导管a,打开分液漏斗时,稀硫酸较难滴下,而且测得的气体体积(选填“偏大”“偏小”或“不变”)。19. 兔子全身都是宝,现在有许多农户以养兔子发家致富。(1)、兔子的运动方式主要是奔跑和跳跃,主要靠骨骼和组成的运动系统来完成。(2)、“兔子不吃窝边草”是为了隐蔽洞穴,这是生物对环境的(选填“影响”或“适应”)。20. 如图甲是学校重大活动时常用的伸缩隔离柱。均质底座呈圆盘形,厚度不计,正中有一立柱杆身,顶端伸缩头中有可收宿的布带,内部有弹性装置固定,松手后布带会自动收回伸缩头中。其模型结构如图乙,A为伸缩头固定位置,B为杆身和底座连接处(杆身直径和布带宽度不计,除底座外其余部件质量均不计),AB长75cm,底座直径30cm,标配底座质量4.5kg。收缩布带的拉力与伸长量成正比。
(1)、实验中,最简易的装置连接顺序是①→ →⑥(填接口的数字)。(2)、实验中,如果用止水夹夹住导管a,打开分液漏斗时,稀硫酸较难滴下,而且测得的气体体积(选填“偏大”“偏小”或“不变”)。19. 兔子全身都是宝,现在有许多农户以养兔子发家致富。(1)、兔子的运动方式主要是奔跑和跳跃,主要靠骨骼和组成的运动系统来完成。(2)、“兔子不吃窝边草”是为了隐蔽洞穴,这是生物对环境的(选填“影响”或“适应”)。20. 如图甲是学校重大活动时常用的伸缩隔离柱。均质底座呈圆盘形,厚度不计,正中有一立柱杆身,顶端伸缩头中有可收宿的布带,内部有弹性装置固定,松手后布带会自动收回伸缩头中。其模型结构如图乙,A为伸缩头固定位置,B为杆身和底座连接处(杆身直径和布带宽度不计,除底座外其余部件质量均不计),AB长75cm,底座直径30cm,标配底座质量4.5kg。收缩布带的拉力与伸长量成正比。 (1)、将图甲中的收缩布带向右拉出时,可将隔离柱整体看成是一根杠杆,请在乙图上画出隔离柱受到的拉力和拉力的力臂。(2)、在使用“标配底座”时,布带可承受的拉力为N。21. 思维导图是激发大脑潜能、练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“一”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
(1)、将图甲中的收缩布带向右拉出时,可将隔离柱整体看成是一根杠杆,请在乙图上画出隔离柱受到的拉力和拉力的力臂。(2)、在使用“标配底座”时,布带可承受的拉力为N。21. 思维导图是激发大脑潜能、练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“一”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题: (1)、物质D的类别是:。(2)、请写出:“B→E”的化学方程式:。22. 如图所示,A是悬挂在弹簧下的铁块,B是螺丝管的铁芯,P是滑动变阻器的滑片。
(1)、物质D的类别是:。(2)、请写出:“B→E”的化学方程式:。22. 如图所示,A是悬挂在弹簧下的铁块,B是螺丝管的铁芯,P是滑动变阻器的滑片。 (1)、闭合开关后的电磁铁的下端是极(选填“N”或“S”)。(2)、若将变阻器的滑片P向右移动,弹簧的长度会(选填“变长”或“变短”)。23. 有一包固体,可能含有NaCl、NaOH、Na2CO3、Na2SO4、MgCl2中的一种或几种。为确定其组成,取少量固体加足量水溶解得到无色溶液M,进行如图实验。
(1)、闭合开关后的电磁铁的下端是极(选填“N”或“S”)。(2)、若将变阻器的滑片P向右移动,弹簧的长度会(选填“变长”或“变短”)。23. 有一包固体,可能含有NaCl、NaOH、Na2CO3、Na2SO4、MgCl2中的一种或几种。为确定其组成,取少量固体加足量水溶解得到无色溶液M,进行如图实验。
试推断:
(1)、无色滤液2中的阳离子至少有种。(2)、原固体中一定含有的物质是。三、实验探究题(本大题共有5小题,每小题8分,共40分)
-
24. 科学家通过研究得知:细胞分裂素能抑制叶绿素、核酸和蛋白质的降解,抑制叶片衰老,所以在生产中可利用细胞分裂素作保鲜剂。请完成下列实验设计,证明细胞分裂素有延缓叶片衰老的作用。(1)、选取的叶片20片,平分成两组,分别标记为甲、乙。(2)、在甲组叶片的局部位置涂上一定浓度的细胞分裂素,乙组叶片处涂上等量的蒸馏水。(3)、观察记录。(4)、若细胞分裂素确有延缓叶片衰老的作用,则实验结果应该是。25. 如图1,“食品蒸汽加热器”常用于野外加热食物。加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热。实验小组针对放热过程中的反应原理展开探究。

【查阅资料】
①常温下镁粉能与水反应放热而铁粉不能;②氢氧化镁是难溶于水的白色固体。
【进行实验】
同学们用如图2所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:(实验时的室温为22.7℃;除B外,其余实验中镁粉的质量均为1.0g)
实验序号
A
B
C
D
E
F
固体成分
Mg
Fe
Mg+Fe
Mg+NaCl
Fe+NaCl
Mg+Fe+NaCl
乙中现象
少量肥皂泡,难以点燃
无肥皂泡
少量肥皂泡,难以点燃
较多肥皂泡,点燃有爆鸣声
无肥皂泡
大量肥皂泡,点燃有爆鸣声
混合物温度
23.1℃
22.8℃
23.1℃
24.2℃
22.8℃
27.2℃
【获得结论】
(1)、实验A证明了镁粉与水能反应,反应的化学方程式为。(2)、使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入。(3)、分析实验数据发现,升高的温度不足以加热食物,其可能的原因是。(4)、同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中的固液混合物中仍然含有NaCl和铁粉,通过补充实验证明了上述猜测。补充验证铁粉的实验方案是:取少量固液混合物,。26. 为探究浸没在水中的物体对容器底的压力与哪些因素有关,某小组同学利用DIS数据采集系统及若干重力G和密度ρ已知的实心物体等器材进行实验。他们将实心物体放入盛水的平底容器中(如图所示),测出物体对容器底的压力F,并将实验数据记录在表一中。表一
实验序号
1
2
3
4
5
6
7
8
9

密度ρ(g/cm)
2.0
2.5
3.0
重力G(N)
4
8
12
4
8
12
3
6
9
压力F(N)
2.0
4.0
6.0
2.4
4.8
7.2
2.0
4.0
6.0
(1)、分析表一中实验序号1与4(或2与5,或3与6)中的数据及相关条件可初步得出:当物体的重力相同时,浸没在水中的物体对容器底的压力随的增大而增大。(2)、分析表一中实验序号1、2、3(或4、5、6,或7、8、9)中的数据及相关条件可初步得出:。(3)、小组同学进一步综合分析表一中的数据有了新发现,他们将经计算得到的部分数据记录在表二中。表二
(ρ-ρ水):ρ
1:2
3:5
2:3
F:G
▲
①表二中划线处的数据为。
②按表二中数据反映的规律推理:若浸没在水中某实心物体的密度ρ=4g/cm3 , 重力G=12N,则物体对容器底的压力F=N。
27. 某科学兴趣小组的同学用如图装置, 进行木炭还原CuO的探究实验,生成物是红色固体和无色气体。他们查阅资料后得知氧化亚铜(Cu2O)为红色固体,猜测反应物比例不同,产物也会不同。生成物中有CO2、CO和Cu,固体还可能有Cu2O,Cu2O能和常见的酸(HNO3除外)反应生成Cu²+和Cu,微量的CO气体能使湿润的黄色氯化钯试纸变蓝色。为此,请你和他们一起进行如下探究。 (1)、该兴趣小组同学设计的木炭还原CuO实验装置有何不足之处?
(1)、该兴趣小组同学设计的木炭还原CuO实验装置有何不足之处?
(2)、为验证产生的气体是CO2和CO的混合物,将混合气体进行如下操作:
实验中观察到现象则证明是CO2和CO的混合气体。
(3)、探究红色固体中是否有Cu2O。设计一个简便的实验方案,如下表所示。实验步骤
向剩余固体中加入稀盐酸反应后,静置
实验现象与结论
现象;结论:红色固体中有Cu2O
化学反应方程式
28. 为了研究导体两端电压一定的情况下,通过导体的电流与导体电阻的关系,小金根据图甲所示的电路图,将实验器材连接成如图乙所示的实验电路。 (1)、经检查,该实验电路中一根导线连接错误。请在错误导线上打“×”并补上正确连接的导线。(2)、改正错误后,小金继续实验。第一次实验用的定值电阻R的阻值为10Ω,闭合开关后,记下电流表的示数为I1;第二次实验仅将电阻R换成5Ω的定值电阻,闭合开关后,记下电流表的示数为I2。此时I2 2I1(选填“<”“=”或“>”),然后移动滑片使电压表示数不变,进行后续实验。(3)、小金将阻值为5Ω、10Ω、15Ω、20Ω、25Ω的定值电阻分别接在AB间,电源电压恒为6V,闭合开关,调节滑动变阻器的滑片,记下电流表示数,得到如图丙所示的电流Ⅰ随电阻R变化的图像。实验中,小金控制AB电压不变为Ⅴ。为了完成整个实验,应该选取最大阻值至少Ω的滑动变阻器。
(1)、经检查,该实验电路中一根导线连接错误。请在错误导线上打“×”并补上正确连接的导线。(2)、改正错误后,小金继续实验。第一次实验用的定值电阻R的阻值为10Ω,闭合开关后,记下电流表的示数为I1;第二次实验仅将电阻R换成5Ω的定值电阻,闭合开关后,记下电流表的示数为I2。此时I2 2I1(选填“<”“=”或“>”),然后移动滑片使电压表示数不变,进行后续实验。(3)、小金将阻值为5Ω、10Ω、15Ω、20Ω、25Ω的定值电阻分别接在AB间,电源电压恒为6V,闭合开关,调节滑动变阻器的滑片,记下电流表示数,得到如图丙所示的电流Ⅰ随电阻R变化的图像。实验中,小金控制AB电压不变为Ⅴ。为了完成整个实验,应该选取最大阻值至少Ω的滑动变阻器。四、解答题(本大题共有5小题,31、33题11分,34题12分,32、35题8分,共50分)
-
29. 如图一表示某生态系统食物网简图,图二是某生态系统中物质循环和能量流动示意图。请据此图回答:
 (1)、若用图一表示某生态系统中的生物,其中起决定性作用的生物是 , 图中未表示出的生态系统成分是。(2)、图一中有条食物链,写出该生态系统中鹰获得能量较少的食物链。(3)、图二中表示蛇的呼吸作用从外界吸收氧气呼出二氧化碳的途径是(填数字序号)(4)、生态系统的各种成分通过联系成了一个统一的整体。30. 如图甲是一种车载空气净化器,其工作过程如图乙所示:受污染的空气被吸入后,颗粒物进入电离区带上正电荷,然后在集尘器上被带负电的金属网“捕获”。该车载空气净化器的额定功率为4.8W,额定电压为12V。请分析回答:
(1)、若用图一表示某生态系统中的生物,其中起决定性作用的生物是 , 图中未表示出的生态系统成分是。(2)、图一中有条食物链,写出该生态系统中鹰获得能量较少的食物链。(3)、图二中表示蛇的呼吸作用从外界吸收氧气呼出二氧化碳的途径是(填数字序号)(4)、生态系统的各种成分通过联系成了一个统一的整体。30. 如图甲是一种车载空气净化器,其工作过程如图乙所示:受污染的空气被吸入后,颗粒物进入电离区带上正电荷,然后在集尘器上被带负电的金属网“捕获”。该车载空气净化器的额定功率为4.8W,额定电压为12V。请分析回答: (1)、带电金属网能“捕获”颗粒物,这是运用了的原理。(2)、计算该车载空气净化器正常工作时的电流为多大?正常工作10分钟电流所做的功为多大?31. 如图为一款高科技智能双轮电动平衡车,它利用了动态平衡原理控制前进及后退,因其体积较小、操控新颖方便等优点深受年轻人的喜爱。下表是该双轮电动平衡车的部分技术参数:
(1)、带电金属网能“捕获”颗粒物,这是运用了的原理。(2)、计算该车载空气净化器正常工作时的电流为多大?正常工作10分钟电流所做的功为多大?31. 如图为一款高科技智能双轮电动平衡车,它利用了动态平衡原理控制前进及后退,因其体积较小、操控新颖方便等优点深受年轻人的喜爱。下表是该双轮电动平衡车的部分技术参数:车身自重
最高速度
轮子与地面总接触面积
200N
5m/s
20cm2
 (1)、该电动平衡车在水平直路面上以最高速度匀速行驶30分钟时,通过的路程为多少?(2)、质量为60kg的小科同学站在该双轮电动平衡车上,则地面受到的压强是多大?(3)、若该双轮电动平衡车以最高速度匀速行驶时受到的阻力为总重的0.2倍,小科骑着它在水平路面上以最高速度匀速行驶30分钟,牵引力做功为多大?32. 学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,进行了如下实验:
(1)、该电动平衡车在水平直路面上以最高速度匀速行驶30分钟时,通过的路程为多少?(2)、质量为60kg的小科同学站在该双轮电动平衡车上,则地面受到的压强是多大?(3)、若该双轮电动平衡车以最高速度匀速行驶时受到的阻力为总重的0.2倍,小科骑着它在水平路面上以最高速度匀速行驶30分钟,牵引力做功为多大?32. 学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中都加入11g样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;
③将充分反应后生成的沉淀过滤、洗涤、干燥得到wg的白色固体。实验数据如下:
烧杯Ⅰ
烧杯Ⅱ
烧杯Ⅲ
加入CaCl2的质量/g
5.55
12
15
白色固体w/g
5
10
10
回答下列问题:
(1)、碳酸钠与CaCl2的反应,基本反应类型为:。(2)、求样品中碳酸钠的质量分数是多少?(结果保留2位小数)(3)、将烧杯Ⅲ的滤液蒸干,得到的固体成分是什么?各多少克?33. 如图为一款利用高温水蒸气熨烫衣服的挂烫机,它的正常工作电压为220V,水箱最多装水0.3kg,加热功率有大小两个档位。设计师最初设计的内部电路有甲、乙两种接法,其中电热丝R1=56Ω、R2=44Ω。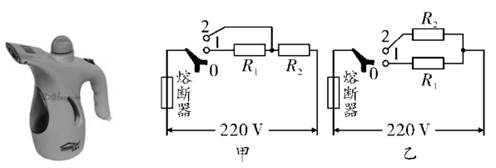 (1)、使用挂烫机时,要插入三孔插座,是为了将金属外壳与相连。(2)、高温水蒸气熨烫衣服时,水蒸气遇到衣服迅速(填物态变化名称)成小水珠,放出热量将衣服熨平,所以使用时要避免烫伤。(3)、已知熔断器里的保险丝允许通过的最大电流为8.2A,请通过计算说明设计师应该选择哪个电路。
(1)、使用挂烫机时,要插入三孔插座,是为了将金属外壳与相连。(2)、高温水蒸气熨烫衣服时,水蒸气遇到衣服迅速(填物态变化名称)成小水珠,放出热量将衣服熨平,所以使用时要避免烫伤。(3)、已知熔断器里的保险丝允许通过的最大电流为8.2A,请通过计算说明设计师应该选择哪个电路。