广东省潮安县金石中学等五校2016-2017学年九年级下学期化学期中联考考试试卷
试卷更新日期:2017-09-11 类型:期中考试
一、选择题
-
1. 生活中有太多的变化,下列“变”中涉及化学变化的是( )A、树根“变”根雕 B、牛奶“变”酸奶 C、玉石“变”印章 D、机器人“变”形2. 有人通过闻茶的方法就能判断出茶的产地,人们能够闻到茶香的原因是( )A、分子间有间隔 B、分子在不断地运动 C、分子的质量和体积都很小 D、分子是由原子构成的3. 按酸、碱、盐、氧化物的顺序排列的一组物质是( )A、H2SO4、Na2CO3、NaCl、CuO B、H2O、Ca(OH)2、HCl、Na2SO4 C、H2SO4、NaOH、Na2CO3、Fe2O3 D、NaOH、H2CO3、NaCl、CO24. 农作物在缺氮的情况下,生长迟缓、叶色发黄.这时需施用的化肥是( )A、KCl B、NH4HCO3 C、K2SO4 D、Ca(H2PO4)25. 下列实验操作能达到预期目的的是( )A、用10mL的量筒量取9.0mL水 B、用向下排空气法收集纯净的氢气 C、用托盘天平称取10.58g碳酸钠粉末 D、用150mL酒精和50mL水精确配制200mL医用消毒酒精6.
利用下图所示装置,能完成实验室制取气体的是( )
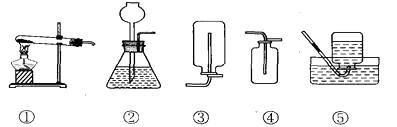 A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳7. 实验室四瓶失去标签的无色溶液分别为氯化钠溶液、稀盐酸、氢氧化钠溶液和稀硫酸.以下说法正确的是( )A、打开试剂瓶塞就可以判断出稀盐酸------瓶口有“白雾” B、观察试剂瓶的瓶塞可以判断出氢氧化钠溶液-------是胶塞 C、打开试剂瓶塞尝味道可以判断出氯化钠溶液------有咸味 D、将pH试纸伸入试剂瓶中可以判断出稀硫酸-------pH小于78. 下列关于钠原子和钠离子的说法中,正确的是( )A、Na比Na+稳定 B、Na得到一个电子变成Na+ C、Na和Na+化学性质相同 D、Na和Na+都属于钠元素9. 在学习化学的过程中,我们会发现许多具有规律性的知识。下列叙述中不正确的是( )
A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳7. 实验室四瓶失去标签的无色溶液分别为氯化钠溶液、稀盐酸、氢氧化钠溶液和稀硫酸.以下说法正确的是( )A、打开试剂瓶塞就可以判断出稀盐酸------瓶口有“白雾” B、观察试剂瓶的瓶塞可以判断出氢氧化钠溶液-------是胶塞 C、打开试剂瓶塞尝味道可以判断出氯化钠溶液------有咸味 D、将pH试纸伸入试剂瓶中可以判断出稀硫酸-------pH小于78. 下列关于钠原子和钠离子的说法中,正确的是( )A、Na比Na+稳定 B、Na得到一个电子变成Na+ C、Na和Na+化学性质相同 D、Na和Na+都属于钠元素9. 在学习化学的过程中,我们会发现许多具有规律性的知识。下列叙述中不正确的是( )
A、对难溶于水的气体可用排水集气法收集 B、碱溶液中都含有相同的OH- C、含碳元素的物质完全燃烧会产生二氧化碳 D、金属都能与酸反应产生氢气10. 科学家用第72号元素铪(音:hā)和第74号元素钨,精确测出月球比地球至少早700万年形成。下列决定元素种类的是( )A、核内中子数 B、核内质子数 C、最外层电子数 D、相对原子质量11. 大多数作物适宜在中性或接近中性的土壤中生长。经测定某土壤的pH为5.5,为使其更适宜植物生长,应在土壤中施加适量的( )A、氢氧化钠 B、熟石灰 C、食盐 D、盐酸12. 下图所示的四个图象,能正确表示对应变化关系的是( )A、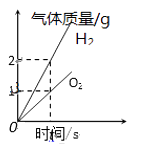 水的电解
B、
水的电解
B、 木炭在密闭的容器内燃烧
C、
木炭在密闭的容器内燃烧
C、 加热一定量的氯酸钾制氧气
D、
加热一定量的氯酸钾制氧气
D、 20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
二、选择填充题
-
13. 绿茶是安徽的特产,种类很多,绿茶是将新鲜的茶叶炒熬,破坏其中酵素再经搓揉、烘焙而成。茶叶的化学成分主要是茶碱(C8H10N4O2),还有鞣酸及芳香油等,下列说法错误的是( )A、茶碱由四种元素组成 B、一个茶碱分子中含24个原子 C、茶叶是混合物 D、茶碱中氧元素的质量分数最大14. 某同学对所学部分化学知识归纳如下,其中有错误的一组是( )A、物质性质与用途:衣服上圆珠笔油——用汽油或酒精搓洗;区别棉和羊毛织物——取少量,点燃闻气味 B、日常生活经验:O2助燃——气焊切割金属;H2O2:分解放出O2——实验室制O2 C、安全常识:煤气泄漏——打110电话报警;皮肤沾上浓硫酸——用水冲洗,再涂稀硫酸 D、化学与生活:维生素C——缺乏时引起坏血病;糖类、蛋白质——人类必须摄取的营养素
三、信息分析题
-
15. 根据问题填空:(1)、在①氧气、②水、③石墨、④二氧化碳、⑤一氧化碳、⑥天然气、⑦生铁、 ⑧石油、⑨不锈钢等物质中:(填序号)
属于单质的是 , 属于合金的是 , 极易与血红蛋白结合使人中毒的气体是。
(2)、写出相应的化学符号:氢氧根离子;澄清石灰水中的溶质。16. 高纯度的单质硅是信息产业的核心材料,没有硅就没有你喜欢的计算机。请用你学过的知识回答下列问题:(1)、地壳中含有大量的硅元素,它的含量仅次于元素。(2)、SiO2是沙子的主要成分,工业上制取粗硅的化学方程式为:SiO2+2C Si+2R,R的化学式为;该化学反应的基本类型是。
(3)、硅在O2中燃烧生成SiO2 , 并放出大量的热,有科学家正研究将硅作为新能源。与化石能源相比较,硅燃烧不排放CO2 , 因而有助于解决的环境问题是。17.根据下图所示, 回答有关问题:
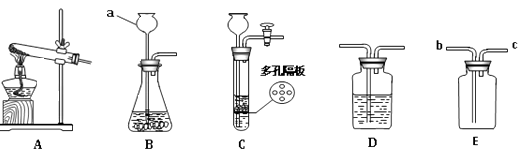 (1)、写出图中标有字母的仪器名称:a。(2)、实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母),实验时该装置试管口应放一团棉花,其目的是;反应的化学方程式为。(3)、实验室制取二氧化碳气体,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,装置 中的液体是(填写试剂名称)。如果用E装置收集该气体,则气体应从端进入(填b或c)。通常用澄清石灰水来检验二氧化碳,反应的化学方程式为。(4)、
(1)、写出图中标有字母的仪器名称:a。(2)、实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母),实验时该装置试管口应放一团棉花,其目的是;反应的化学方程式为。(3)、实验室制取二氧化碳气体,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,装置 中的液体是(填写试剂名称)。如果用E装置收集该气体,则气体应从端进入(填b或c)。通常用澄清石灰水来检验二氧化碳,反应的化学方程式为。(4)、下图是以锌粒和稀硫酸反应制备H2 , 并用排水法收集.请把图补画完整。
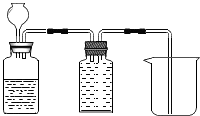
四、填空题
-
18.
下图A是某元素在元素周期表中的相关信息, B是其原子结构示意图。
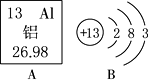 (1)、该元素的相对原子质量为;(2)、该元素属于元素(选填 “金属”或“非金属”);(3)、该原子在化学反应中容易电子(选填 “得到”或“失去”)。19. 查阅资料可知,米酒味道变酸是因为米酒中产生的醋酸杆菌使乙醇(C2H5OH)和氧气发生反应生成了醋酸(CH3COOH)和另一种常见的液体。回答下列问题:(1)、食物变质是一种氧化反应(填“剧烈”、“缓慢”)。(2)、米酒味道变酸的化学反应方程式为;可用验证米酒味道变酸却是生成了醋酸。20.
(1)、该元素的相对原子质量为;(2)、该元素属于元素(选填 “金属”或“非金属”);(3)、该原子在化学反应中容易电子(选填 “得到”或“失去”)。19. 查阅资料可知,米酒味道变酸是因为米酒中产生的醋酸杆菌使乙醇(C2H5OH)和氧气发生反应生成了醋酸(CH3COOH)和另一种常见的液体。回答下列问题:(1)、食物变质是一种氧化反应(填“剧烈”、“缓慢”)。(2)、米酒味道变酸的化学反应方程式为;可用验证米酒味道变酸却是生成了醋酸。20.下图甲是A,B,C三种固体物质的溶解度曲线图。
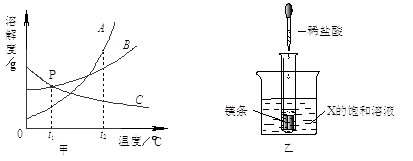 (1)、甲图中,t2℃时,A,B,C三种物质中,溶解度最大的是。P点所表示的含义为 。(2)、保持t2℃温度不变,将B物质的不饱和溶液转变成饱和溶液可采取的方法有。(3)、如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A,B,C三种固体物质中的 。21.
(1)、甲图中,t2℃时,A,B,C三种物质中,溶解度最大的是。P点所表示的含义为 。(2)、保持t2℃温度不变,将B物质的不饱和溶液转变成饱和溶液可采取的方法有。(3)、如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A,B,C三种固体物质中的 。21.如图是实验室常用的两个气体制备、收集、净化的多功能装置.
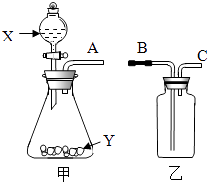 (1)、若用于制氢气,且产生的气体中不含酸性杂质气体,则试剂X常用 , 用图示放置的乙装置收集氢气,A应与 (填“B”或“C”)相连.(2)、若X是稀盐酸、Y是石灰石,用甲、乙两装置可组成发生、净化、收集CO2气体的系列装置.若乙中放入饱和NaHCO3溶液,则该溶液的作用是除去;若乙中放入浓硫酸,浓硫酸的作用是 .(3)、若X是水,Y是CaC2固体,则从A中放出乙炔(化学式:C2H2)气体,同时还生成一种碱.乙炔微溶于水,密度与空气接近.若用乙装置收集乙炔,则乙中还应该装入;生成乙炔的化学方程式是 .22. 一定条件下用NH3捕捉CO2的反应为2NH3+3CO2
(1)、若用于制氢气,且产生的气体中不含酸性杂质气体,则试剂X常用 , 用图示放置的乙装置收集氢气,A应与 (填“B”或“C”)相连.(2)、若X是稀盐酸、Y是石灰石,用甲、乙两装置可组成发生、净化、收集CO2气体的系列装置.若乙中放入饱和NaHCO3溶液,则该溶液的作用是除去;若乙中放入浓硫酸,浓硫酸的作用是 .(3)、若X是水,Y是CaC2固体,则从A中放出乙炔(化学式:C2H2)气体,同时还生成一种碱.乙炔微溶于水,密度与空气接近.若用乙装置收集乙炔,则乙中还应该装入;生成乙炔的化学方程式是 .22. 一定条件下用NH3捕捉CO2的反应为2NH3+3CO2——C3H3N3O3+3H2O,生成的三聚氰胺(C3H3N3O3 , 相对分子质量为129)是重要的化工产品。请回答下列问题:(1)、三聚氰胺中C,H,N,O四种元素的质量之比为。(2)、每生产25.8 kg三聚氰酸,可以捕捉CO2的质量为。(3)、Na2CO3溶液同样能用于“捕捉”CO2 , 反应为Na2CO3+H2O+CO2——2□,□中物质的化学式为。五、探究题
-
23.
甲班学生做完实验室制备氧气和还原金属氧化物的实验后,剩余物质倒入同一废液缸里。乙班课外兴趣小组同学进行了如图所示的探究。请回答:
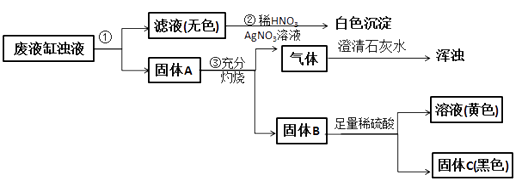 (1)、步骤①的操作名称是 , 所用到的玻璃仪器有漏斗、玻璃棒和。(2)、由步骤②实验现象推知,甲班同学制取氧气所用的固体反应物是(写化学式)。(3)、由步骤④所得溶液加入氢氧化钠可得红棕色沉淀,该反应的化学方程式为。(4)、由步骤③产生的气体判断固体A中一定含有(写名称);综合步骤③④现象推理,固体A中还可能含有的物质是(写至少两种物质的化学式)。(5)、根据上述实验和分析判断固体是(写化学式)。24. 化学兴趣小组欲探究自己使用的某品牌牙膏的主要成分。(1)、【查阅资料】
(1)、步骤①的操作名称是 , 所用到的玻璃仪器有漏斗、玻璃棒和。(2)、由步骤②实验现象推知,甲班同学制取氧气所用的固体反应物是(写化学式)。(3)、由步骤④所得溶液加入氢氧化钠可得红棕色沉淀,该反应的化学方程式为。(4)、由步骤③产生的气体判断固体A中一定含有(写名称);综合步骤③④现象推理,固体A中还可能含有的物质是(写至少两种物质的化学式)。(5)、根据上述实验和分析判断固体是(写化学式)。24. 化学兴趣小组欲探究自己使用的某品牌牙膏的主要成分。(1)、【查阅资料】①牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质。
②常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2。
③牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
④SiO2不溶于水,也不与盐酸反应。
Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为。
(2)、偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应。
相关物质的溶解性表:
物质
Al(OH)3
NaAlO2
AlCl3
溶解性
不溶
溶
溶
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3 .
猜想2:摩擦剂的成分为 .
猜想3:摩擦剂的成分为SiO2和Al(OH)3 .
【设计实验】
实验步骤
预期实验现象
预期实验结论
组装下图装置进行实验.取少量摩擦剂于锥形瓶中,加入适量的 .

固体全部溶解,有气泡,石灰水变浑浊
则猜想1成立
锥形瓶中发生的化学反应方程式为
摩擦剂部分溶解
石灰水无明显变化
则猜想3成立
【实验结论】经过实验验证,猜想1成立.
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为 , 依据该现象可以判断摩擦剂中一定含有氢氧化铝.
六、简答题
-
25.
某腐蚀印刷电路板的废液中含有CuCl2和FeCl2 , 为了分析该废液的组成,取1000g废液,设计如下实验方案进行探究:
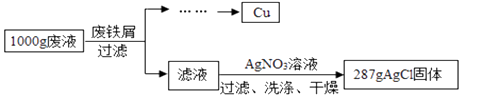
实验过程中加入废铁屑的质量、析出Cu的质量的数据记录如下表:
废铁屑的质量/g
20
40
60
80
析出Cu的质量/g
12.8
25.6
32
32
(注:废铁屑中的杂质不溶于废液也不与废液反应,不考虑过滤中的损失。)
(1)、1000g废液与足量废铁屑完全反应,析出Cu的质量为 g。(2)、废铁屑中单质Fe的质量分数为。(3)、计算1000g废液中CuCl2的质量分数。(写出计算过程,结果保留小数点后一位)(4)、1000g废液中FeCl2的质量分数为。(结果保留小数点后一位)