辽宁省营口市鲅鱼圈区2019年中考化学5月模拟试卷
试卷更新日期:2020-04-17 类型:中考模拟
一、选择题
-
1. 日常生活中见到下列现象,其中发生了化学变化的是( )A、冬天的早晨,玻璃窗上出现美丽的冰花 B、牛奶放置时间过长变质 C、自行车轮胎在烈日下爆裂 D、玻璃杯被打碎2. 如图中“
 ”和“
”和“  ””表示两种不同元素的原子,下列方框中表示混合物的是() A、
””表示两种不同元素的原子,下列方框中表示混合物的是() A、 B、
B、 C、
C、 D、
D、 3. 下列实验操作正确是( )A、
3. 下列实验操作正确是( )A、 测定未知溶液的 pH
B、
测定未知溶液的 pH
B、 检查装置气密性
C、
检查装置气密性
C、 检验 CO2
D、
检验 CO2
D、 称量食盐
4. “吃的营养”和“吃的健康”是人们普遍的饮食追求。下列说法正确是( )A、多吃烧烤食品对成长大为有利 B、过量摄入微量元素对身体有益 C、常吃蔬菜和水果可以补充维生素 D、食用甲醛浸泡过的海产品有利于健康5. 下列关于下列实验现象,描述不正确是( )A、氢气在空气中燃烧,产生淡蓝色火焰,放出大量的热 B、镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 D、光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡6. 下列溶液在空气中敞口放置后,溶液质量是因发生化学变化而减小的是( )A、石灰水 B、浓硫酸 C、浓盐酸 D、烧碱溶液7. 鱼胆弄破后,会使鱼肉粘上一种叫胆汁液(一种酸)的物质,它难溶于水,使鱼肉变苦,要消除这种苦味,可用下列何种溶液冲洗最适宜( )A、纯碱溶液 B、醋酸 C、食盐水 D、氢氧化钠溶液8. 食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”,下列物质可以作“双吸剂”的是( )A、炭粉 B、铁粉 C、氯化钙 D、生石灰9. 能一次性鉴别稀盐酸、硝酸钾溶液、澄清石灰水的物质是( )A、硫酸钾溶液 B、二氧化碳 C、酚酞溶液 D、碳酸钠溶液10. 将一定质量的甲、乙、丙、丁四种物质放入一密封容器中,在你一定条件下反应一段时间,测得反应前后各物质的质量如表,则下列说法中不正确是( )
称量食盐
4. “吃的营养”和“吃的健康”是人们普遍的饮食追求。下列说法正确是( )A、多吃烧烤食品对成长大为有利 B、过量摄入微量元素对身体有益 C、常吃蔬菜和水果可以补充维生素 D、食用甲醛浸泡过的海产品有利于健康5. 下列关于下列实验现象,描述不正确是( )A、氢气在空气中燃烧,产生淡蓝色火焰,放出大量的热 B、镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 D、光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡6. 下列溶液在空气中敞口放置后,溶液质量是因发生化学变化而减小的是( )A、石灰水 B、浓硫酸 C、浓盐酸 D、烧碱溶液7. 鱼胆弄破后,会使鱼肉粘上一种叫胆汁液(一种酸)的物质,它难溶于水,使鱼肉变苦,要消除这种苦味,可用下列何种溶液冲洗最适宜( )A、纯碱溶液 B、醋酸 C、食盐水 D、氢氧化钠溶液8. 食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”,下列物质可以作“双吸剂”的是( )A、炭粉 B、铁粉 C、氯化钙 D、生石灰9. 能一次性鉴别稀盐酸、硝酸钾溶液、澄清石灰水的物质是( )A、硫酸钾溶液 B、二氧化碳 C、酚酞溶液 D、碳酸钠溶液10. 将一定质量的甲、乙、丙、丁四种物质放入一密封容器中,在你一定条件下反应一段时间,测得反应前后各物质的质量如表,则下列说法中不正确是( )物质
甲
乙
丙
丁
反应前质量(g)
7.6
2.0
0.2
0
反应后质量(g)
3.2
X
5.8
0.4
A、X=0.4 B、丁一定是单质 C、甲和乙是反应物 D、参加反应的甲、丙质量之比是11:1411. 将一定量的木炭在盛有32g氧气的密闭容器中燃烧(氧气完全反应),将生成的气体通入足量的澄清石灰水中,生成50g沉淀.生成气体中碳元素的质量分数为( )A、12% B、24% C、36% D、50%12. 烈性炸药TNT(化学式为C7H5N3O6)广泛用于开矿、修路、兴修水利等,下列关于TNT的说法不正确是( )A、TNT是一种有机物 B、TNT爆炸后会产生二氧化硫 C、TNT由四种元素组成 D、每个TNT分子含有21个原子13. 推理是化学学习中常用的思维方法。下列推理正确是( )A、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 B、分子、原子可以构成物质,则物质都是由分子、原子构成的 C、铝表面的氧化铝薄膜能起到保护作用,则铁表面的铁锈也能起到保护作用 D、碱性溶液能使酚酞变红,则使酚酞变红的溶液一定呈碱性14. 下列各组物质,能在pH=1的溶液中大量共存,且形成无色溶液的是( )A、NaNO3HCl Na2SO4 B、NaNO3 NaCl CuSO4 C、NaCl Na2SO4Na2CO3 D、NaOH BaCl2 Na2SO415. 除去下列各组物质中的杂质,所用试剂和方法均正确是( )选项
物质
杂质
除杂所用的试剂和方法
A
CaO固体
CaCO3固体
加入适量的稀盐酸
B
NaOH溶液
Ca(OH)2溶液
先加入过量的Na2CO3溶液,再过滤
C
CO2气体
CO气体
点燃
D
H2气体
HCl气体
先通过NaOH溶液,再通过浓硫酸
A、A B、B C、C D、D二、填空题(本大题包括4道小题,每空1分,共20分)
-
16. 用化学用语填空:(1)、2个氦原子(2)、亚铁离子(3)、3个氨气分子(4)、氧化铝中铝元素显+3价17. 根据图中提供的信息,请回答下列问题:
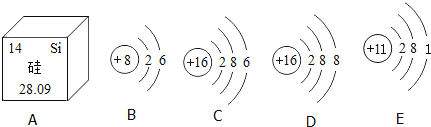 (1)、由A图可知,硅的相对原子质量为;(2)、B,C,D,E中属于同种元素的是;(3)、B、C元素化学性质相似的原因是相同;(4)、C、E两种元素组成化合物的化学式为 .18. 水是生命之源,爱护水资源是每个公民应尽的责任。请回答下列有关问题:(1)、硬水给生活和生产带来很多麻烦,生活中可用来区分硬水和软水;(2)、下列是一些净水的方法,其中可使硬水变成软水的是:(填序号)。
(1)、由A图可知,硅的相对原子质量为;(2)、B,C,D,E中属于同种元素的是;(3)、B、C元素化学性质相似的原因是相同;(4)、C、E两种元素组成化合物的化学式为 .18. 水是生命之源,爱护水资源是每个公民应尽的责任。请回答下列有关问题:(1)、硬水给生活和生产带来很多麻烦,生活中可用来区分硬水和软水;(2)、下列是一些净水的方法,其中可使硬水变成软水的是:(填序号)。①过滤 ②蒸馏 ③沉淀 ④煮沸
(3)、我国是淡水资源非常有限的国家,爱护水资源是每个公民的责任和义务。下列行为属于浪费水的是(填字母编号);A.洗手擦香皂时不关上水龙头 B.用洗菜水浇花
C.用洗衣水冲厕所 D.用自来水不断为西瓜冲水降温
(4)、如图为甲、乙、丙三种物质的溶解度曲线图,请回答:
①t2℃时,将30g甲物质放入到50g水中,充分搅拌,所得溶液的质量是;
②将t2℃时甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所 得溶液中溶质质量分数由大到小的顺序是;
③在t3℃要配成等质量的甲、丙两种饱和溶液需要甲和丙的质量为甲丙 (填<>=)
19. 化学与人类生活、生产活动息息相关。请根据所学化学知识回答下列问题:(1)、生活中“高钙牛奶”,其中的“钙”应理解为(填“元素”或“单质”)(2)、“84”消毒液的主要成分是次氯酸钠(NaClO),可由反应2NaOH+X=NaClO+NaCl+H2O制得,则X的化学式为。(3)、使用洗洁精洗去铁锅上的油污,这是利用洗洁精的(选填“溶解”或“乳化”)作用。为了防止铁锅生锈可以采取的措施是。(4)、向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,滤液中一定含有的阳离子和滤渣中一定含有的金属是(填化学符号),当滤渣中有Ag和Cu时,滤液中的溶质可能有的情况是(填化学式)。三、简答题(本大题包括2道小题,共14分)
-
20. 在人们担心化石能源将被耗尽时,科学家发现海底埋藏着大量可以燃烧的“冰”﹣﹣“可燃冰”。可燃冰外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等气体。可燃冰在低温和高压条件下形成。1体积可燃冰可储载100~200倍体积的甲烷气体,具有能量高,燃烧值大等优点。可燃冰将成为未来新能源。目前,我国在可燃冰的开采技术上处于世界领先水平。回答下列问题:(1)、可燃冰属于 (填字母序号)A、纯净物 B、混合物(2)、甲烷在空气中完全燃烧的化学方程式为。(3)、甲烷中氢为+l价,碳为价。(4)、从环境保护的角度考虑,下列燃料中最理想的是 。 (填字母序号)A、氢气 B、可燃冰 C、酒精 D、汽油(5)、可燃冰作为未来新能源,与煤、石油相比其优点是。(答一点即可)(6)、可燃冰在海底不燃烧的原因是;21. A,B,C,D,E,F分别是由两种或三种元素组成的常见化合物。B是人类利用最广泛的一种氧化物,生活中可用来灭火;D广泛用于玻璃、造纸、纺织、洗涤剂的生产;人体胃酸中含有F,可帮助消化。它们之间的一部分关系如图所示,(图中“﹣”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系。部分反应物或生成物已略去)请回答下列问题:
 (1)、B物质的化学式为;F物质的化学式为。(2)、C与D反应的基本反应类型是(3)、D→E反应的化学反应方程式为。(4)、A→C反应的化学反应方程式为。
(1)、B物质的化学式为;F物质的化学式为。(2)、C与D反应的基本反应类型是(3)、D→E反应的化学反应方程式为。(4)、A→C反应的化学反应方程式为。四、实验与探究题(本大题包括3道小题,共20分)
-
22. 某化学小组欲配制49g溶质质量分数为20%的稀硫酸来进行实验,老师为他们提供了溶质质量分数为98%的浓硫酸(密度为1.84g/cm3).(1)、通过计算,需要用到溶质质量分数为98%的浓硫酸的质量是g.(2)、量取浓硫酸时仰视读数(其他操作正确),则配制的稀硫酸的溶质质量分数(填“大于”、“小于”或“等于”)20%.(3)、A和B是两个同学稀释浓硫酸操作的示意图,正确是(填“A”或“B”).
 (4)、玻璃棒搅拌的作用是 .23. 某研究性学习小组利用下列装置进行气体的制取实验,请分析回答下列问题。
(4)、玻璃棒搅拌的作用是 .23. 某研究性学习小组利用下列装置进行气体的制取实验,请分析回答下列问题。 (1)、写出标号①仪器的名称。(2)、选用A装置用高锰酸钾制取氧气的化学方程式。(3)、A、E连接,制取的氧气不纯的原因是(写一点即可)。(4)、选用锌粒和稀硫酸制取氢气的发生装置选择(填字母)(5)、若用F装置收集二氧化碳,则气体应从端通入(填“a”或“b”)。若用F装置检验制得的气体是否为二氧化碳,则在F装置中放入一量 , 气体应从端通入(填“a”或“b”)。24. 化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。
(1)、写出标号①仪器的名称。(2)、选用A装置用高锰酸钾制取氧气的化学方程式。(3)、A、E连接,制取的氧气不纯的原因是(写一点即可)。(4)、选用锌粒和稀硫酸制取氢气的发生装置选择(填字母)(5)、若用F装置收集二氧化碳,则气体应从端通入(填“a”或“b”)。若用F装置检验制得的气体是否为二氧化碳,则在F装置中放入一量 , 气体应从端通入(填“a”或“b”)。24. 化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。【提出问题】固体样品的成分是什么?
【查阅资料】
(1)、碱石灰干燥剂是CaO和NaOH的混合物。(2)CaCl2溶液显中性。【猜想与假设】固体样品中可能含有 Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和等七种物质。
(2)、【进行实验】
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作
实验现象
实验结论及化学方程式
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中
①
②
结论:滤渣B中有 Fe2O3 , CaCO3。
实验操作中Fe2O3与稀盐酸反应的化学方程式为:
(3)、乙组同学对滤液C的成分进行探究,记录如下:实验操作
实验现象
实验结论及化学方程式
取少量滤液C于试管中,加入过量CaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡
①有白色沉淀生成
②酚酞试液由无色变成红色
滤液C中有;
滤液C中的物质与CaCl2反应的化学方程式是
(4)、【解释与结论】①乙组同学实验中加入过量CaCl2溶液的目的是
②通过以上实验探究,该固体样品中能确定一定含有的成分是。
五、计算题(共1个小题,共6分):
-
25. 某样品硝酸钾中含有一定质量的氯化钾.为了测定其中硝酸钾的质量分数做如下实验:取10g该样品加入58.87g水使其完全溶解,向溶液中逐滴加入硝酸银溶液至恰好完全反应,共用去34g硝酸银溶液;过滤、烘干称得沉淀为2.87g.根据实验计算:(1)、样品中硝酸钾的质量分数为多少?(2)、反应后所得溶液中溶质的质最分数为多少?