2016届广东省广州市龙文教育九年级上学期教学质检化学试卷
试卷更新日期:2016-04-20 类型:期末考试
一、选择题
-
1. 下列著名诗句中隐含有化学变化的是( )
A、白玉做床,金做马 B、千里冰封,万里雪飘 C、野火烧不尽,春风吹又生 D、夜来风雨声,花落知多少2. 如图所示的实验操作中正确的是( )
A、加热液体 B、移走蒸发皿
B、移走蒸发皿 C、倾倒液体
C、倾倒液体 D、读取液体体积
D、读取液体体积 3. 下列生活中的常见材料,属于有机合成高分子材料的是( )
3. 下列生活中的常见材料,属于有机合成高分子材料的是( )
A、钢筋混凝土 B、陶瓷 C、塑料 D、油脂4. 月球土壤含有大量氦3原子,它可能成为未来核能的重要原料.氦3原子核内有2个质子和1个中子,氦3原子结构示意图是( )
A、 B、
B、 C、
C、 D、
D、 5. 人体缺少钙、铁等元素会影响身体健康.下列补充化学元素的做法错误的是( )
5. 人体缺少钙、铁等元素会影响身体健康.下列补充化学元素的做法错误的是( )
A、大量服用含碘药物预防甲状腺肿大 B、使用铁制炊具防治缺铁性贫血 C、进食牛奶、豆制品等富钙食物预防幼儿佝偻病 D、食用牡蛎等含锌海产品防治因缺锌引起的食欲不振、发育不良6. 古语道:“人要实、火要虚”,此话的意思是:“做人必须脚踏实地,事业才能有成”,燃烧固体燃料时需要将其架空,燃烧才能更旺.从充分燃烧的条件看,“火要虚”的实质是( )
A、增大可燃物的热值 B、提高空气中氧气的含量 C、降低可燃物的着火点 D、增大可燃物与空气的接触面积7. 根据如图的溶解度曲线,判断下列说法中不正确的是( )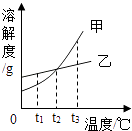 A、t1℃时,甲物质的溶解度小于乙物质的溶解度 B、t2℃时,甲、乙两物质的饱和溶液中含甲、乙两物质的质量相等 C、将t3℃的甲、乙两物质的饱和溶液降温至t2℃时,都会析出晶体 D、当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲8.
A、t1℃时,甲物质的溶解度小于乙物质的溶解度 B、t2℃时,甲、乙两物质的饱和溶液中含甲、乙两物质的质量相等 C、将t3℃的甲、乙两物质的饱和溶液降温至t2℃时,都会析出晶体 D、当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲8.如图,在杠杆的两端分别挂着质量相同的铜球和锌球,这时杠杆平衡.然后将两球分别浸在稀H2SO4和CuSO4溶液中片刻,下列说法正确的是( )
 A、只有左边烧杯中溶液的质量增加 B、只有右边烧杯中溶液的质量增加 C、两边烧杯中溶液的质量都增加 D、取掉烧杯后,杠杆仍然保持平衡9. 推理是化学学习中常用的思维方法.下列推理正确的是( )
A、只有左边烧杯中溶液的质量增加 B、只有右边烧杯中溶液的质量增加 C、两边烧杯中溶液的质量都增加 D、取掉烧杯后,杠杆仍然保持平衡9. 推理是化学学习中常用的思维方法.下列推理正确的是( )
A、置换反应一定有单质生成,所以有单质生成的反应一定是置换反应 B、有机物完全燃烧都产生二氧化碳,所以有机物中一定含有碳元素 C、燃烧都伴随发光、放热,所以有发光、放热现象的就是燃烧 D、氧化物中都含有氧元素,所以含有氧元素的化合物一定是氧化物10. 防止金属锈蚀是保护金属资源的有效途径,锌铬黄(化学式为ZnCrO4)常用于制防锈涂料.锌铬黄中铬元素的化合价为( )
A、+1 B、+2 C、+6 D、+711. 掌握化学用语是学好化学的关键,下列化学用语与含义相符的是( )
A、Fe3O4﹣﹣四氧化三铁 B、2H﹣﹣2个氢元素 C、O2﹣﹣2个氧原子 D、﹣﹣钠离子12. 把40g5%的CaCl2溶液溶质质量分数增大到10%,应采用的方法是( )
A、把溶剂蒸发掉一半 B、加入2gCaCl2固体 C、加入20g15%的CaCl2溶液 D、把溶剂蒸发掉20g13. 无土栽培是现代农业的一项新技术,其营养液是多种化合物的混合溶液,含有植物生长所需的营养元素.某种植物进行无土栽培时,需含氮、钾等元素的中性或弱酸性营养液,下列能用来配制营养液的一组化合物是( )
A、KCl、(NH4)2SO4 , NaOH B、NH4Cl、K2SO4 C、KNO3 , H2SO4 D、K2CO3 , CaCl214.把分别充满红棕色NO2气体和无色H2的集气瓶,按照图A,B两种方式放置,然后把两瓶中间的玻璃片抽走,使两瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需很长时间才能达到同样的效果.不能由此现象直接得出的结论是( )
 A、分子是不断运动的 B、分子间有间隔 C、氢气的密度比二氧化氮的密度小 D、分子由原子构成15. 某同学郊游时不慎被蜜蜂蜇伤,蜜蜂分泌出的液体呈酸性,该同学随身携带的下列物品中可以用来涂抹在蜇伤处以减轻疼痛的是( )
A、分子是不断运动的 B、分子间有间隔 C、氢气的密度比二氧化氮的密度小 D、分子由原子构成15. 某同学郊游时不慎被蜜蜂蜇伤,蜜蜂分泌出的液体呈酸性,该同学随身携带的下列物品中可以用来涂抹在蜇伤处以减轻疼痛的是( )
A、苹果汁(pH约为3) B、肥皂水(pH约为10) C、矿泉水(pH约为7) D、牛奶(pH约为6.5)16. 在四支试管中分别加入2mL稀盐酸,并滴入几滴酚酞试液,如果分别不断加入下列物质直至过量,其中能使溶液显红色的是( )
A、CuO B、CaCO3 C、NaOH D、Fe17. 下列各组各有两种物质,它们的化学式和所属的物质类别都正确的一组是( )物质1
物质2
名称
化学式
物质类别
名称
化学式
物质类别
A
氮气
N
非金属单质
氧化亚铁
Fe2O2
碱
B
碳酸氢钠
NaHCO3
盐
硝酸
HNO3
酸
C
硫酸钾
K2SO4
盐
五氧化二磷
P2O5
金属氧化物
D
锰
Mm
金属单质
氢氧化镁
Mg(OH)2
碱
A、A B、B C、C D、D18. 熟石灰在日常生活中和工农业生产中有广泛的用途.下列关于熟石灰的用途中,说法不正确的是( )A、作建筑材料 B、改良酸性土壤 C、中和化工厂的酸性废水 D、治疗胃酸过多19.化学反应2H2O2
 2H2O+O2↑属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应20. A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀盐酸反应.相同条件下,C、D能与稀盐酸反应产生H2 , 且D比C反应剧烈.则四种金属的活动性由强到弱的顺序是( )
2H2O+O2↑属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应20. A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀盐酸反应.相同条件下,C、D能与稀盐酸反应产生H2 , 且D比C反应剧烈.则四种金属的活动性由强到弱的顺序是( )
A、A—B—C—D B、B—A—C—D C、D—C—A—B D、D—C—B—A二、填空题
-
21. 用化学用语填空:
①一个甲烷分子 ;
②2个氢离子 ;
③氧化铁 ;
④硫酸铵 ;
22.如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
 (1)、在℃时,甲与丙的溶解度相等.(2)、t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为 .(3)、t1℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是(用“甲”、“乙”、“丙”及“>”、“<”或“=”表示).(4)、从如图你能获得的信息有(写两条) .23. 将下列两组中的两种反应物混合,回答下列问题:
(1)、在℃时,甲与丙的溶解度相等.(2)、t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为 .(3)、t1℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是(用“甲”、“乙”、“丙”及“>”、“<”或“=”表示).(4)、从如图你能获得的信息有(写两条) .23. 将下列两组中的两种反应物混合,回答下列问题:
(1)、根据实验事实完成下表(没有发生反应的,化学方程式一栏“/”)编号
反应物1
反应物2
现象
化学方程式
1
稀盐酸
氢氧化铜
2
稀硫酸
氢氧化钡溶液
有白色沉淀生成
3
稀硝酸
澄清石灰水
没有明显现象
(2)、分析上述实验,反应能够发生的共同原因是:反应物1中都含有(填化学用语,下同) , 反应物2中都含有 .24. 碳酸钠用途非常广泛,是工业生产中重要的化工原料.在1921年我国科学家侯德榜创造了一种著名的纯碱生产方法﹣﹣“联合制碱法”.“联合制碱法”生产过程:(1)、第一步主要反应为NH3+CO2+H2O═NH4HCO3该反应属于反应(基本反应类型).(2)、第二步用食盐与NH4HCO3反应.食盐来源于某盐田,该粗盐主要含有氯化钠,此外还含有少量硫酸钠,氯化钙和氯化镁.经净化、精制得到生产碳酸钠所需要的食盐水,其主要流程如图1:

①通过降温使硫酸钠从粗盐水中析出,其原理是氯化钠和硫酸钠的溶解度与温度的变化差异较大,请在溶解度图(如图2)中简单画出氯化钠和硫酸钠的溶解度曲线变化趋势图.
②“精制I”操作中,加入过量含钙元素的碱的化学式是 .
其反应化学方程示为 .
③“精制II”操作中,加入B盐的有关反应方程式为 .
④为保证“精制II”操作中过量B盐把杂质全部除去,请在下表中写出检验溶液中B盐是否过量的实验报告.
实验操作
实验现象
实验结论
⑤查阅资料得知NaCl、NH4HCO3、NaHCO3、NH4Cl在30℃时的溶解度如下表所示:
温度
NH4Cl
NH4HCO3
NaHCO3
NaCl
30℃
41.1g
27.0g
11.1g
36.3g
请根据溶解度表所提供的信息,写出“联合制碱法”中的第二步属于复分解反应的化学方程式: .
第三步处理制得碳酸钠,反应原理为2NaHCO3
 Na2CO3+H2O+CO2↑25. 根据所学知识回答下列问题:
Na2CO3+H2O+CO2↑25. 根据所学知识回答下列问题:
(1)、用pH试纸测定液体的pH值时,所需用品除了玻璃棒,pH试纸外,还需要;(2)、用量筒量取一定体积液体时,需要注意的事项是 .26.某同学设计了一套验证碳酸具有酸性而二氧化碳没有酸性的实验.他首先用紫色石蕊试液浸泡滤纸,晒干后折成纸花,然后按如图所示分别进行:
 (1)、紫色石蕊纸花遇到酸性溶液显色.(2)、在B实验中,当加入水后,紫色石蕊纸花显色,B实验的作用是 .(3)、在C实验中,紫色石蕊纸花变色,用化学方程式解释 .(4)、通过以上实验,还缺少一个对比实验,你的改进方法是 .27.
(1)、紫色石蕊纸花遇到酸性溶液显色.(2)、在B实验中,当加入水后,紫色石蕊纸花显色,B实验的作用是 .(3)、在C实验中,紫色石蕊纸花变色,用化学方程式解释 .(4)、通过以上实验,还缺少一个对比实验,你的改进方法是 .27.小强和小明两位同学在实验室用下列装置制取几种气体.
 (1)、小强想用高锰酸钾制取一瓶尽可能纯净的氧气,他应选择上述装置中的A和(填装置序号)进行组装,而小明认为A装置中还缺少;(2)、在装入药品前,应先检查装置;(3)、小强用15.8g高锰酸钾(化学式KMnO4)制取氧气,完全反应后理论上可以生成氧气的质量为g;(4)、当氧气收集满并取出集气瓶后,停止制取氧气实验的正确操作步骤是先 , 后 .(5)、小明要制取少量CO2 , 他选用的气体发生装置是(填装置序号) , 收集CO2的装置是(填装置序号) , 选用该收集装置的理由是 , 检验集气瓶中是否收集满CO2的方法是 .(6)、C装置中长颈漏斗的作用是便于 . 为了防止生成的气体从长颈漏斗逸出,必须使长颈漏斗 .28. 有三种白色粉末,分别是碳酸钠、氯化铁和氯化钠中的一种.请设计一个实验方案,把这三种粉末区分开来.叙述实验操作、预期现象和结论.
(1)、小强想用高锰酸钾制取一瓶尽可能纯净的氧气,他应选择上述装置中的A和(填装置序号)进行组装,而小明认为A装置中还缺少;(2)、在装入药品前,应先检查装置;(3)、小强用15.8g高锰酸钾(化学式KMnO4)制取氧气,完全反应后理论上可以生成氧气的质量为g;(4)、当氧气收集满并取出集气瓶后,停止制取氧气实验的正确操作步骤是先 , 后 .(5)、小明要制取少量CO2 , 他选用的气体发生装置是(填装置序号) , 收集CO2的装置是(填装置序号) , 选用该收集装置的理由是 , 检验集气瓶中是否收集满CO2的方法是 .(6)、C装置中长颈漏斗的作用是便于 . 为了防止生成的气体从长颈漏斗逸出,必须使长颈漏斗 .28. 有三种白色粉末,分别是碳酸钠、氯化铁和氯化钠中的一种.请设计一个实验方案,把这三种粉末区分开来.叙述实验操作、预期现象和结论.实验操作
预期现象与结论
三、推断题
-
29. 现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液,分别编号为A、B、C、D.每次取少量溶液两两混合,所观察到的现象记录在下表中(“﹣”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成).
A
B
C
D
A
﹣
↑
↓
﹣
B
↑
﹣
↓
↑
C
↓
↓
﹣
﹣
D
﹣
↑
﹣
﹣
(1)、由此推断4瓶溶液中的溶质的化学式分别为:A.;B.;C.;D.
(2)、写出上述实验过程的有关反应方程式:A+B、C+D .