浙教版科学九年级上册第二章第二节 金属的化学性质 同步训练
试卷更新日期:2017-09-06 类型:同步测试
一、单选题
-
1. 下列物质与稀硫酸反应不能产生氢气的是( )A、镁 B、银 C、铁 D、铝2.
如图为某文化衫图案,你的美(Mg)偷走我的心(Zn)能发生,是由于镁的( )
 A、延展性好 B、导电性好 C、导热性好 D、金属活动性比锌强3. 在柠檬中插入两种不同的金属可以制得水果电池。相同条件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠檬电池的两种金属,活动性差异最大的是( )
A、延展性好 B、导电性好 C、导热性好 D、金属活动性比锌强3. 在柠檬中插入两种不同的金属可以制得水果电池。相同条件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠檬电池的两种金属,活动性差异最大的是( )
A、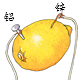 B、
B、 C、
C、 D、
D、 4. 相等质量的镁、锌、铁与足量稀硫酸反应情况如图所示,则Z表示的金属是( )
4. 相等质量的镁、锌、铁与足量稀硫酸反应情况如图所示,则Z表示的金属是( ) A、Zn B、Fe C、Mg D、无法判断5. 金属与盐酸的反应的示意图如图所示,下列说法正确的是( )
A、Zn B、Fe C、Mg D、无法判断5. 金属与盐酸的反应的示意图如图所示,下列说法正确的是( )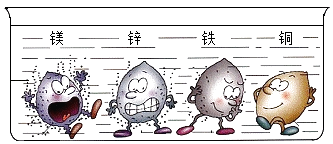 A、四种金属中活动性最强的是铜 B、实验室可用锌和稀硫酸制氢气 C、铁可以把镁从硫酸镁溶液中置换出来 D、铁与稀盐酸反应的化学方程式为:2Fe+6HCl═2FeCl3+3H2↑6. 下列各组物质,加水混合搅拌,待充分反应后过滤,滤纸上留下两种金属单质的是( )A、CuSO4(过量)、Al、Na2SO4 B、Fe(过量)、Cu(NO3)2、AgNO3 C、Zn(过量)、KNO3、AgNO3 D、Cu(过量)、FeSO4、H2SO47. 在以下四种金属中,有一种金属元素形成的化合物的溶液与其他三种金属单质都能发生置换反应,这种金属是( )A、Fe B、Cu C、Zn D、Ag8. 有X、Y、Z三种金属,将X、Y和Z分别浸入稀盐酸中,只有Y表面产生气泡.将Z浸入X的硝酸盐溶液中,在z的表面有X析出.则X、Y、Z三种金属的活动性由强到弱的顺序是( )A、X Y Z B、X Z Y C、Y Z X D、Y X Z9. 金属活动性顺序表在化学学习中有重要作用,下列说法正确的是( )A、Zn不能置换出稀硫酸中的氢 B、Ag能将硫酸铜溶液中的铜置换出来 C、“真金不怕火炼”说明金在高温时也不与氧气反应 D、在Al、Mg、Fe中金属活动性最强的是Al10. 用实验比较铜、锌、铁的金属活动性,最好的方法是选用下列试剂中的( )A、硫酸锌溶液 B、硫酸亚铁 C、硫酸铜溶液 D、硝酸银溶液11. X、Y两金属都能跟硝酸银溶液起反应,置换出银;X跟稀硫酸不反应,Y跟稀硫酸起反应生成氢气.由此判断X、Y两金属可能依次是( )A、Fe Hg B、Fe Zn C、Cu Hg D、Cu Zn12. 为验证Fe、Cu、Ag 3种金属的活动性顺序,某小组同学设计了如图所示的4种实验方案(不做其他实验).其中不能达到目的是( )A、
A、四种金属中活动性最强的是铜 B、实验室可用锌和稀硫酸制氢气 C、铁可以把镁从硫酸镁溶液中置换出来 D、铁与稀盐酸反应的化学方程式为:2Fe+6HCl═2FeCl3+3H2↑6. 下列各组物质,加水混合搅拌,待充分反应后过滤,滤纸上留下两种金属单质的是( )A、CuSO4(过量)、Al、Na2SO4 B、Fe(过量)、Cu(NO3)2、AgNO3 C、Zn(过量)、KNO3、AgNO3 D、Cu(过量)、FeSO4、H2SO47. 在以下四种金属中,有一种金属元素形成的化合物的溶液与其他三种金属单质都能发生置换反应,这种金属是( )A、Fe B、Cu C、Zn D、Ag8. 有X、Y、Z三种金属,将X、Y和Z分别浸入稀盐酸中,只有Y表面产生气泡.将Z浸入X的硝酸盐溶液中,在z的表面有X析出.则X、Y、Z三种金属的活动性由强到弱的顺序是( )A、X Y Z B、X Z Y C、Y Z X D、Y X Z9. 金属活动性顺序表在化学学习中有重要作用,下列说法正确的是( )A、Zn不能置换出稀硫酸中的氢 B、Ag能将硫酸铜溶液中的铜置换出来 C、“真金不怕火炼”说明金在高温时也不与氧气反应 D、在Al、Mg、Fe中金属活动性最强的是Al10. 用实验比较铜、锌、铁的金属活动性,最好的方法是选用下列试剂中的( )A、硫酸锌溶液 B、硫酸亚铁 C、硫酸铜溶液 D、硝酸银溶液11. X、Y两金属都能跟硝酸银溶液起反应,置换出银;X跟稀硫酸不反应,Y跟稀硫酸起反应生成氢气.由此判断X、Y两金属可能依次是( )A、Fe Hg B、Fe Zn C、Cu Hg D、Cu Zn12. 为验证Fe、Cu、Ag 3种金属的活动性顺序,某小组同学设计了如图所示的4种实验方案(不做其他实验).其中不能达到目的是( )A、 B、
B、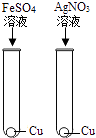 C、
C、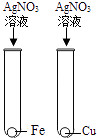 D、
D、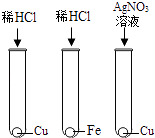 13. 被雨水淋湿的自行车,应( )A、先用布擦干,再用带油的布擦拭 B、在自行车表面刷一层油漆 C、用布擦干即可 D、晾干后,用盐酸除去锈层14. 已知铁锈的主要成分为Fe2O3•xH2O,下列是某同学探究铁生锈所设计的实验方案.其中不需要做的实验是( )
13. 被雨水淋湿的自行车,应( )A、先用布擦干,再用带油的布擦拭 B、在自行车表面刷一层油漆 C、用布擦干即可 D、晾干后,用盐酸除去锈层14. 已知铁锈的主要成分为Fe2O3•xH2O,下列是某同学探究铁生锈所设计的实验方案.其中不需要做的实验是( )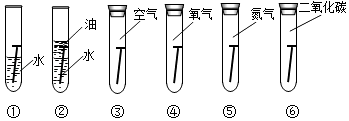 A、①② B、③④ C、⑤⑥ D、④⑤15. 下列物品需采取防锈措施的是( )A、铁制防盗网 B、不锈钢汤勺 C、铝合金门窗 D、银项链16. 铁锈是( )A、氧化铁 B、含铁化合物 C、氧化亚铁 D、混合物,主要是氧化铁
A、①② B、③④ C、⑤⑥ D、④⑤15. 下列物品需采取防锈措施的是( )A、铁制防盗网 B、不锈钢汤勺 C、铝合金门窗 D、银项链16. 铁锈是( )A、氧化铁 B、含铁化合物 C、氧化亚铁 D、混合物,主要是氧化铁二、填空题
-
17. 铁锈的主要成分是 , 其结构 , 不能阻碍里层的铁继续生锈,因此铁制品可以全部锈蚀.18. 向硝酸银、硝酸铜和硝酸镁的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中滴加稀盐酸,无明显现象,则滤液中一定含有的金属离子是什么? , 写出上述过程中一定发生反应的化学方程式。19. 防止铁制品生锈的常用措施有(写一点即可),也可在铁片表面镀上一层锌,表面会形成一层保护薄膜,其中含有Zn2(OH)2CO3 . 若该物质通过化合反应生成,试推断,反应物除了Zn、水和氧气外,还应有 .20.
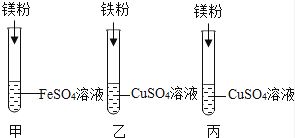
化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案.
(1)试管乙中观察到的现象是 , 反应的化学方程式为 .
(2)同学们经讨论后认为该方案可以优化,试管的实验是多余的.
(3)去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,
向滤渣中加入稀硫酸,有气泡产生,则滤渣的成分可能是 .
 21.
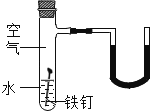
21.某同学做了一个有关铁生锈的趣味实验,过程如图所示:
(1)一段时间后,能观察到的现象是
(2)请用理化知识解释出现上述现象的原因 .
三、综合题
-
22. 根据下面部分金属的活动性顺序回答:
Mg Zn Fe (H) Cu Hg Ag
(1)、上述金属中活动性最强的是;(2)、按年代最早被广泛使用的金属是;(3)、Cu、Fe、Ag三种金属中,能与稀盐酸发生置换反应的是 .(4)、已知:①X+H2SO4=XSO4+H2↑ ②Y+2ZNO3=Y(NO3)2+2Z ③Y与稀硫酸不反应,则符合要求的X、Y、Z分别是 (填字母序号)A、Cu、Hg、Ag B、Fe、Cu、Ag C、Mg、Zn、Fe.23. 如图所示,在盛有自来水的试管中放一根洁净的铁钉,用带U形管的胶塞塞紧,U形管的水面处于同一高度,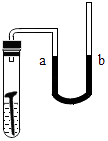 (1)、数天后观察到U形管内的水面 .A、a比b高 B、b比a高 C、一样高(2)、U型管液面变化的原因是 .
(1)、数天后观察到U形管内的水面 .A、a比b高 B、b比a高 C、一样高(2)、U型管液面变化的原因是 .四、探究题
-
24. 整理实验器材时,小柯将还在反应的锌和稀硫酸的残留物,倒入有少量硫酸铜溶液的废液缸中,观察到锌粒表面产生气泡的速度大大加快。对此,他十分好奇:与硫酸铜溶液混合怎么会加快锌和稀硫酸的反应速度?
查阅资料:①相互接触的两种活动性不同的金属,同时放入酸中,活动性较强的金属与酸反应产生氢气的速度会大大加快。 ②硫酸铜对锌和稀硫酸反应没有催化作用。
小柯根据下表进行实验,观察并记录现象。
组别
第一组
第二组
A
B
C
D
金属
锌片
绑有铜片的锌片
铁片
绑有铜片的铁片
30%硫酸溶液(mL)
20
?
20
20
产生气泡快慢
快
明显加快
慢
明显加快
(1)、第一组实验中“?”处的数据应为。(2)、为了定量比较产生气体的快慢,可以测量“收集相同体积的氢气所需的时间”或测量 , 然后进行比较。
(3)、请推测与废液缸中少量硫酸铜溶液混合后,锌料与稀硫酸反应速度加快的原因。25. 为验证锌、铁、铜三种金属的话动性顺序,张丽和王宇同学设计了不同的实验方案进行实验,都达到了实验目的.他们所用的试剂有锌片、铁片、铜片、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶液.实验方案如下:实验方案
方案一
方案二
实验操作
一种金属放入两种溶液中
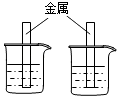
两种金属同时放入一种溶液中
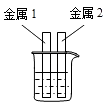 (1)、方案一中选择的金属是;(2)、方案二中能发生反应的化学方程式是;(3)、李军又设计了一个新的方案,也能达到实验目的.即将三种金属同时放入一种溶液中,该溶液中的溶质不是金属化合物,他选择的溶液是 .
(1)、方案一中选择的金属是;(2)、方案二中能发生反应的化学方程式是;(3)、李军又设计了一个新的方案,也能达到实验目的.即将三种金属同时放入一种溶液中,该溶液中的溶质不是金属化合物,他选择的溶液是 .