江苏省南通市2017年中考化学考试试卷
试卷更新日期:2017-08-30 类型:中考真卷
一、选择题
-
1. 2017年5月18日南海可燃冰试采成功,这是中国科学家勇攀世界科技高峰的又一标志性成就.1体积可燃冰可储载100~200倍体积的甲烷气体.甲烷属于( )
 A、有机物 B、单质 C、氧化物 D、混合物2. 下列有关物质的组成或分类说法正确的是( )A、金刚石、C60都是碳的化合物 B、水、过氧化氢都含有相同组成元素 C、碳酸氢铵、硫酸钾都是氮肥 D、钙、氧都是人体必需的微量元素3. “一定溶质质量分数的NaOH溶液的配制”实验操作示意图如下,其中正确的是( )A、
A、有机物 B、单质 C、氧化物 D、混合物2. 下列有关物质的组成或分类说法正确的是( )A、金刚石、C60都是碳的化合物 B、水、过氧化氢都含有相同组成元素 C、碳酸氢铵、硫酸钾都是氮肥 D、钙、氧都是人体必需的微量元素3. “一定溶质质量分数的NaOH溶液的配制”实验操作示意图如下,其中正确的是( )A、 取用NaOH
B、
取用NaOH
B、 称取NaOH
C、
称取NaOH
C、 量取一定体积的水
D、
量取一定体积的水
D、 溶解NaOH固体
4. 下列说法正确的是( )
溶解NaOH固体
4. 下列说法正确的是( ) A、乙醇、橡胶都属于合成高分子材料 B、蛋白质、糖类均属于基本营养素 C、如图试管Ⅰ中铁钉比试管Ⅱ中更容易绣蚀 D、物质由气态变成液态,分子间的间隔变大5. 下列有关物质的性质与用途具有对应关系的是( )A、石墨很软,因此可用作电池电极 B、H2具有还原性,因此可用于充氢气球 C、Al(OH)3能与盐酸反应,因此可用于治疗胃酸过多 D、N2不易溶于水,因此可用于焊接金属时的保护气6. 甲、乙、丙三种固体的溶解度曲线如图所示,下列说法正确的是( )
A、乙醇、橡胶都属于合成高分子材料 B、蛋白质、糖类均属于基本营养素 C、如图试管Ⅰ中铁钉比试管Ⅱ中更容易绣蚀 D、物质由气态变成液态,分子间的间隔变大5. 下列有关物质的性质与用途具有对应关系的是( )A、石墨很软,因此可用作电池电极 B、H2具有还原性,因此可用于充氢气球 C、Al(OH)3能与盐酸反应,因此可用于治疗胃酸过多 D、N2不易溶于水,因此可用于焊接金属时的保护气6. 甲、乙、丙三种固体的溶解度曲线如图所示,下列说法正确的是( ) A、三种物质的溶解度:甲>乙>丙 B、t1℃时,溶质的质量分数:甲=乙 C、t2℃时,乙、丙的饱和溶液降温均有溶质析出 D、甲中混有少量乙时,可通过溶解、加热浓缩、冷却结晶的方法提纯7. 人类的日常生活和工农业生产离不开水,下列说法正确的是( )A、无法用水鉴别硝酸铵、氢氧化钠两种固体 B、用水浇灭着火的纸箱,其原理是移除了可燃物 C、天然水经过自然沉降、过滤、吸附,即得纯水 D、使用加有洗涤剂的水可去除衣服上的油污8. 下列除杂所用试剂和主要实验操作均正确的是( )
A、三种物质的溶解度:甲>乙>丙 B、t1℃时,溶质的质量分数:甲=乙 C、t2℃时,乙、丙的饱和溶液降温均有溶质析出 D、甲中混有少量乙时,可通过溶解、加热浓缩、冷却结晶的方法提纯7. 人类的日常生活和工农业生产离不开水,下列说法正确的是( )A、无法用水鉴别硝酸铵、氢氧化钠两种固体 B、用水浇灭着火的纸箱,其原理是移除了可燃物 C、天然水经过自然沉降、过滤、吸附,即得纯水 D、使用加有洗涤剂的水可去除衣服上的油污8. 下列除杂所用试剂和主要实验操作均正确的是( )物质(括号内为杂质)
所用试剂
主要实验操作
A
MnO2(KCl)
H2O
溶解、过滤
B
NaCl (MgSO4)
NaOH
溶解、过滤、蒸发
C
SO2(CO)
盐酸
溶解、蒸发结晶
D
NH3(H2O)
浓H2SO4
洗气
A、A B、B C、C D、D9. 下列实验能达到实验目的是( )
A、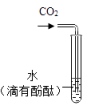 证明CO2水溶液呈酸性
B、
证明CO2水溶液呈酸性
B、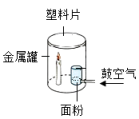 验证面粉粉尘能发生爆炸
C、
验证面粉粉尘能发生爆炸
C、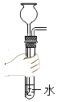 检验该装置的气密性
D、
检验该装置的气密性
D、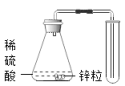 实验室制取并收集少量氢气
10. FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( )
实验室制取并收集少量氢气
10. FeCl3溶液常用于蚀刻印刷电路,反应原理为aFeCl3+bCu═cCuCl2+dX.向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法不正确的是( ) A、X为FeCl2 B、化学计量数c=1 C、方程式中a和b的比为1:2 D、完全反应后,生成X的质量为25.4g
A、X为FeCl2 B、化学计量数c=1 C、方程式中a和b的比为1:2 D、完全反应后,生成X的质量为25.4g二、非选择题
-
11. 宏观和微观相结合是认识物质结构的有效方法之一.(1)、已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表.
X
Y
Z
W
对应元素名称
氧
镁
铝
氯
核电荷数
8
12
13
17
电子层
第一层
2
2
2
2
第二层
a
8
8
8
第三层
3
8
请回答下列问题:
①若X表示原子,a= . 单质X2与单质Z的反应中,X原子(填“得到”或“失去”)电子.
②Y、W形成的化合物化学式为(用元素符号表示).
(2)、将稀硫酸与烧杯中Fe、Cu两种金属相混合,微观变化情况如下图:
未参加反应的金属: , 烧杯中发生反应的化学方程式: .
12. 实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
已知:①反应Ⅰ的化学方程式:MnO2+SO2═MnSO4;
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解.
(1)、反应Ⅰ属于基本反应类型中的反应.(2)、流程中“操作”的名称为 , 所需要的主要玻璃仪器有 .(3)、反应Ⅱ的化学方程式为 . 反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有(填化学式).(4)、验证MnCO3粗产品表面附着有Na2SO4杂质:取样品少许,向其中加入水,搅拌、过滤,向滤液中加入适量的(填化学式)溶液,有白色沉淀产生.(5)、为获得高纯MnCO3 , 需选择“低温”干燥的原因是 .13. 神舟十一号与天宫二号的成功对接增强了国人的民族自信,推动了相关领域的研究.(1)、合金材料的研发①合金的很多性能与组成它们的纯金属不同.图1能表示锡铅合金的是(填序号“a”“b”或“c”).

②镁合金被誉为“21世纪绿色金属结构材料”.Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是(任写一个化学方程式).该合金是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于(填“物理”或“化学”)变化.
(2)、合成材料的改良①碱式碳酸铝镁[MgaAlb[OH]c(CO3)d•xH2O]是一种新型塑料阻燃剂,其中a、b、c、d的代数关系式:2a+3b= .
②大部分塑料在自然环境中很难降解而造成“白色污染”,为缓解这一环境问题可采取的措施有(答出一点即可).
(3)、CO2的绿色利用①目前空间站处理CO2的一种方法是在催化剂作用下,利用H2使CO2转化为甲烷并得到生活用水.该反应的化学方程式为 .
②以“铁氧化物”为催化剂,利用太阳能将CO2热解为碳和氧气,这一转化过程(如图2)中化合价升高的非金属元素是 .
14. 实验探究和证据推理是提升认知的重要手段.化学兴趣小组对“CO还原Fe2O3粉末”的实验进行探究:(1)、Ⅰ探究CO与Fe2O3的反应产物(夹持仪器已略去)
【实验过程】步骤1 在通风橱中,按图Ⅰ连接装置并检验装置的气密性.
步骤2 装入试剂:玻璃管内装入Fe2O3粉末,试管Ⅰ中装入澄清石灰水.
步骤3 从a端通入CO一段时间,待 , 再点燃酒精灯.
(2)、【实验现象】反应一段时间后,玻璃管内粉末由色变成黑色,生成的黑色固体均能被玻璃管上方的磁铁吸引.试管Ⅰ中出现白色沉淀(用化学反应方程式表示: .(3)、【查阅资料】铁粉、FeO、Fe3O4均为黑色固体;铁粉、Fe3O4均能被磁铁吸引.【提出猜想】对磁铁吸引的黑色固体成分有以下三种猜想:
猜测Ⅰ:Fe;猜测Ⅱ:Fe3O4;猜测Ⅲ:Fe和Fe3O4
【实验验证】取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,观察到红色固体中混有黑色颗粒,说明(填“猜想Ⅰ”“猜想Ⅱ”或“猜想Ⅲ”)是正确的.
(4)、【拓展研究】进一步查阅资料,发现CO能溶于铜液[醋酸二氨合铜(Ⅰ)和氨水的混合液].因此可在装置Ⅰ后再连接下图装置Ⅱ,其目的是 , 装置Ⅰ、Ⅱ的连接顺序:b连接(填“c”或“d”).(5)、Ⅱ原料气CO的制备方法一:加热MgCO3、Zn的混合物可快速制备CO,同时还得到两种金属氧化物:、(填化学式).
方法二:加热草酸晶体(H2C2O4•2H2O)制备CO:
H2C2O4•2H2O CO↑+CO2↑+3H2O
已知:常压下,草酸晶体的熔点为101℃.比较草酸晶体的熔点和分解温度,
分析若选用装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是 .
15. 维生素C主要存在于蔬菜、水果中,其分子式为C6H8O6 , 在空气中易氧化变质.(1)、维生素C中C,H,O三种元素的质量比为(用最简比表示).(2)、为测定某鲜榨橙汁中维生素C的含量,兴趣小组进行如下实验:步骤1 取橙汁样品,加入活性炭,振荡、静置、过滤,滤液移至小烧杯中,盖上玻璃片.
步骤2 配制碘(I2)溶液,测得其浓度为1.27g/L(即1升碘溶液中含有1.27克I2).
步骤3 快速移取20.00mL处理后的橙汁样品置于锥形瓶中,滴入碘溶液,恰好完全反应时消耗碘溶液10.00mL.(测定原理:C6H8O6+I2═C6H6O6+2HI)
①步骤1中活性炭的作用是 .
②步骤3必须在步骤1、步骤2之后立即进行的原因是 .
③计算1L该橙汁样品中含有维生素C的质量:g.(请写出计算过程)